los alacalufes
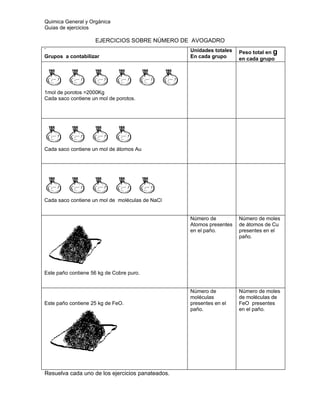
- 1. Quimica General y Orgánica Guias de ejercicios EJERCICIOS SOBRE NÚMERO DE AVOGADRO ` Unidades totales Peso total en g Grupos a contabilizar En cada grupo en cada grupo 1mol de porotos =2000Kg Cada saco contiene un mol de porotos. Cada saco contiene un mol de átomos Au Cada saco contiene un mol de moléculas de NaCl Número de Número de moles Atomos presentes de átomos de Cu en el paño. presentes en el paño. Este paño contiene 56 kg de Cobre puro. Número de Número de moles moléculas de moléculas de Este paño contiene 25 kg de FeO. presentes en el FeO presentes paño. en el paño. Resuelva cada uno de los ejercicios panateados.
- 2. Quimica General y Orgánica Guias de ejercicios Resuelva los siguientes ejercicios: 1 ¿Cuántos átomos hay en: a) 2,55 g de Na R = 6.68 × 1022 b) 8,3 g de Cl2 R = 1.42× 1023 d) 2,5 moles de K R = 1,5 × 1024 2. Determinar el número de moléculas que hay en : a) 5,0 g de NO2 R = 6.62 × 1022 b) 600 mg de I2 R = 1.42 × 1021 c) 3,5 moles de NaCN R = 2.11× 1024 e) 2,8 g de CaSO4 R = 1.24 × 1022 3. Determine el número de moles de átomos que hay en: a) 4,22 × 1020 átomos de K R = 7,01 × 10-4 b) 2,83 × 10-3 g de Ba R = 2,23 × 10-5 c) 7,45 g de Hg R = 0,0371 4. Determinar el número de moles en : a) 5,0 g de N2O4 R = 0,054 b) 2,8 × 1020 moléculas de Na2SO3 R = 4,7 × 10-4 c) 3,27 × 10-3 g de HNO3 R = 5.19 × 10-5 d) 1,00 g de Pb(C2H5)4 R = 3,10 × 10-3 5. ¿Cuántos átomos hay en 12 moléculas de glucosa, C6H12O6? 24 26 a) 24 b) 288 c) 2160 d) 7,22 x 10 e) 1,73 x10 R: b 6. ¿Cuàntos átomos estan presentes en 435 mg de KPF6 (MM = 184,1)? 21 21 22 24 25 a) 1,42 x 10 b) 9,96 x 10 c) 1,14 x 10 d) 1,42 x 10 e) 1,14x10 R: c