Mapas conceptuales enlaces quimicos
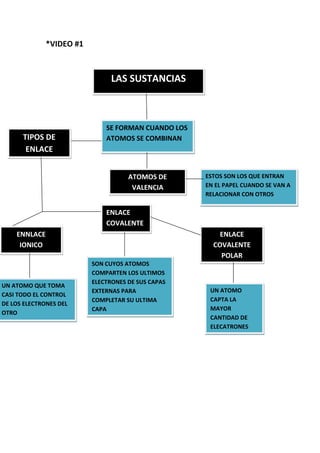
- 1. *VIDEO #1 LAS SUSTANCIAS SE FORMAN CUANDO LOS ATOMOS SE COMBINAN ATOMOS DE VALENCIA ESTOS SON LOS QUE ENTRAN EN EL PAPEL CUANDO SE VAN A RELACIONAR CON OTROS TIPOS DE ENLACE ENLACE COVALENTE SON CUYOS ATOMOS COMPARTEN LOS ULTIMOS ELECTRONES DE SUS CAPAS EXTERNAS PARA COMPLETAR SU ULTIMA CAPA ENLACE COVALENTE POLAR UN ATOMO CAPTA LA MAYOR CANTIDAD DE ELECATRONES QUE EL OTRO ENNLACE IONICO UN ATOMO QUE TOMA CASI TODO EL CONTROL DE LOS ELECTRONES DEL OTRO
- 2. *VIDEO #2 ENLACES QUIMICOS ES LA FUERZA QUE MANTIENE UNIDO A LOS ATOMOS DE LOS ELEMENTOS QUIMICOS CUANDO SE FORMA LA MOLECULA DE UN COMPUESTO LEY DEL OCTETO ES CUANDO LOS ATOMOS INTERCAMBIAN ELECTRONES HASTA COMPLETAR 8 EN SU ULTIMO NIVEL DE ENERGIA ENLACE IONICO ES LA UNION QUE RESULTA DE LA PRESENCIA DE FUERZA DE ATRACCION ELECTROESTATICA ENTRE LOS IONES DE DISTINTO SIGNO SE PRODUCE ENTRE UN ELEMENTO MUY ELECTROPOSITIVO Y OTRO MUY ELECTRONEGATIVO CARACTERISTICAS TIENEN CAPACIDAD DE CONDUCIR LA CORRIENTE ELECTRICA, ELEVADOS PUNTOS DE FUSION Y EBULLICION. ENLACE COVALENTE FUERZA ELECTROMAGNETICA QUE MANTIENE UNIDOS LOS ATOMOS QUE COMPARTEN ELCTRONES. LOS ATOMOS ENLAZADOS SE ENCUENTRAN EN ESTADO NEUTRO Y NO SON METALICOS ENLACE COVALENTE PURO ENLACE COVALENTE POLAR ENLACE COVALENTE TRIPLE
- 3. *VIDEO #3 ENLACE QUIMICO ES LA FUERZA DE NATURALEZA ELECTRICA Y MAGNETICA QUE MANTIENE UNIDOS A ATOMOS O MOLECULAS HASTA FORMAR UN SISTEMA ESTABLE. ELECTRONES DE VALENCIA SON AQUELLOS QUE SE ENCUENTRAN EN EL ULTIMO NIVEL DE ENERGIA LEY DEL OCTETO UN ATOMO AL PERDER O GANAR SUS ELECTRONES DE VALENCIA TIENDE A COMPLETAR CON 8 ELECTRONES SU ULTIMA CAPA, A ALCANZAR LA CONFIGURACION ELECTRONICA ESTABLE NOTACION DE LEWIS ES LA REPRESENTACION DE UN ELEMENTO CON SU SIMBOLO Y SUS ELECTRONES DE VALENCIA MEDIANTE PUNTOS O ASTAS. CLASIFICACION ENLACES INTERATOMICOS ENLACE IONICO ENLACE COVALENTE ENLACES INTERMOLECULAR
- 4. *VIDEO #4 ENLACE QUIMICO LA UNION DE LOS ELEMENTOS DE LA TABLA PERIODICA FORMAN PARTICULAS COMO RADICALES LIBRES O COMO MOLECULAS. RADICAL LIBRE POTENCIA NO SATURADA MOLECULA PARTICULA MAS PEQUEÑA DE UNA SUSTANCIA CAPAZ DE EXISTIR INDEPENDIENTEMENTE ION UNA PARTICULA CON CARGA ENLACE COVALENTE POLAR CUANDO LOS ATOMOS QUE SE JUNTAN TIENEN LA MISMA ELECTRONEGATIVIDAD COORDINADO LOS ATOMOS QUE SE UNEN COMPARTEN UN PAR ELECTRONICO PERO UNO DE ELLOS APORTA DICHO PAR
- 5. *VIDEO #5 TEORIA DE FORMACION DE ENLACES ENLACE VALENCIA ELECTRONES DEL ULTIMO NIVLE DE ENERGIA QUE PARTICIPAN EN LA FORMACIO9N DEL ENLACE COMPARTIDAS POR LOS ATOMOS ORBITAL MOLECULAR CONSIDERA QUE LOS ELECTRONESDE LOS ATOMOS ENLAZADOS PERTENECEN A LA MOLECULA COMO UN TODO ENLACE COVALENTE CUANDO LOS ATOMOS O LOS ELEMENTOS COMPARTEN EL MISMO NUMERO DE ELECTRONES ENLACE IONICO ES CUANDO UN ATOMO LE CEDE UN ELECTRON A OTRO CONVIRTIENDOLO CON ENERGIA NEGATIVA SE PRESENTA CUANDO LOS DOS ELEMENTOS TIENEN UNA GRAN DIFERENCIA DE ELECTRONEGATIVIDAD