Trabajo práctico unidad v saia c 2015-ii-
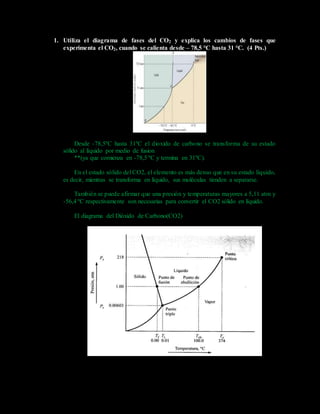
- 1. 1. Utiliza el diagrama de fases del CO2 y explica los cambios de fases que experimenta el CO2, cuando se calienta desde – 78,5 °C hasta 31 °C. (4 Pts.) Desde -78,5ºC hasta 31ºC el dioxido de carbono se transforma de su estado sólido al líquido por medio de fusion **(ya que comienza en -78,5 ºC y termina en 31ºC). En el estado sólido del CO2, el elemento es más denso que en su estado líquido, es decir, mientras se transforma en líquido, sus moléculas tienden a separarse. También se puede afirmar que una presión y temperaturas mayores a 5,11 atm y -56,4 ºC respectivamente son necesarias para convertir el CO2 sólido en líquido. El diagrama del Dióxido de Carbono(CO2)
- 2. Y es muy semejante al del agua, con excepción, que la pendiente de la curva entre la fase sólida y liquida es positiva (+). El agua se comporta de otra forma porque el hielo es menos denso que elagua líquida. El punto triple para el (CO2) es de 5,2 atm. Y – 57ºC. La fase liquida está muy por arriba de la presión atmosférica; es imposible que el dióxido de carbono sólido se funda a la presión de1atm., en cambio cuando el (CO2) sólido se calienta a -78ºC, se sublima (pasa directamente del estado sólido al de vapor). El agua (H2O) se utiliza agroindustrialmente como un disolvente deuna gran variedad de productos químicos, en la congelación de alimentos (forma de conservación) y para determinar la textura de los mismos; el dióxido de carbono (CO2) se emplea agroindustrialmente enla congelación de grasas de repostería para facilitar su mezcla y homogeneización con ingredientes secos, como se hace en la fabricación de pastas para la confección de empanadas y pasteles. Tambiénpara mezclar con las carnes de hamburguesas y salchichas antes de su picado, para conservar su color natural, impedir el ablandamiento de las especies. 2. Una solución se prepara disolviendo 2,638 x 10-3 libras de un compuesto orgánico con agua hasta completar 250 ml, tiene a 159 ºF una presión osmótica de 2,555 bar. Calcular la masa molecular del compuesto orgánico. (3 Pts.) solución 2,638 x 10 agua 250 ml159 ºF 2,555 orgánico.
- 3. 3. A 50 ºC se tiene una mezcla formada por 12,52 gramos de urea en 350 gramos de benceno. Calcular la presión de vapor de la solución en mmHg. Presión de vapor del benceno es 35,991 Kpa. (3 Pts.) alcular las fracciones molares de una mezcla de 12.6 gramos de benceno (C6H6) y 5.2 gramos de etanol (C2H5OH). Pesos Atomicos: C = 12g/mol; H = 1 g/mol y O = 16g/mol x Datos.- x g sto = 5.2 g g ste = 12.52 g Xsto = ? Xste = ? x Para poder calcular las fracciones molares, debemos tener los moles y para calcular los moles necesitamos los pesos moleculares. X PM sto (etanol) = [(12* 2) + (1*6) + (16*1)] g/mol = 46 g/mol x PM ste (benceno) = [(12* 6) + (1*6)] g/mol = 78 g/mol X Ahora calculamos los moles: x g sto 5.2 g mol sto = ---------- = ------------ = 0,11 mol PM sto 46 g/mol x g ste 12.52 g mol ste = ---------- = ------------ = 0,16 mol PM sto 78 g/mol x Ya podemos calcular los moles totales x mol totales = mol sto + mol ste x mol totales = (0,11+0,16) mol = 0,27 mol x Para finalizar calculamos las fracciones molares de ambos componentes de la solucion: x N° de moles sto 0,11mol Xsto = ------------------ = ------------- = 0,41
- 4. N° de moles totales 0,27 mol x N° de moles solv 0,16 mol Xsolv = --------------------- = --------- = 0,59 N° de moles totales 0,27 mol x Al sumar las dos fracciones molares, podemos verificar que es uno.