Acido nítrico método de ostwald
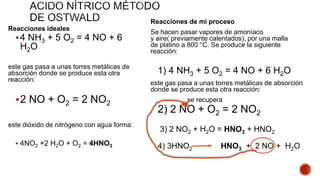
- 1. Reacciones ideales 4 NH3 + 5 O2 = 4 NO + 6 H2O este gas pasa a unas torres metálicas de absorción donde se produce esta otra reacción: 2 NO + O2 = 2 NO2 este dióxido de nitrógeno con agua forma: 4NO2 +2 H2O + O2 = 4HNO3 Reacciones de mi proceso Se hacen pasar vapores de amoníaco y aire( previamente calentados), por una malla de platino a 800 °C. Se produce la siguiente reacción: 1) 4 NH3 + 5 O2 = 4 NO + 6 H2O este gas pasa a unas torres metálicas de absorción donde se produce esta otra reacción: se recupera 2) 2 NO + O2 = 2 NO2 3) 2 NO2 + H2O = HNO3 + HNO2 4) 3HNO2 HNO3 + 2 NO + H2O
- 2. 1. Tanque de almacen 3. Camara de mezcla 2. Filtro 4. Hornos de contacto 700- 800ºc 5. Cambiador de calor 200`c 4. Hay una malla de platino 6.Caldera enfria los gases nitrosos 50ºc y aprovecha para generar vapor de agua 1 4 3 2 5 6 4 NH3(g) + 5 O2(g) = 4 NO + 6 H2O
- 3. 7 a,b,c .Torres de absorción 2 NO(g) + O2 = 2 NO2 2 NO2 + H2O = HNO3 + HNO2 8. refrigerantes 7 8 3HNO2 HNO3 + 2 NO+ H2O
- 4. 17. Acido nítrico diluido al 50% 16 Columna de destilación 20.Aci.nítrico 98% 19 Refrigente 21.Aci.sulfúrico 75% 18.Aci.sulfúrico 98% 17 16 19 21 20 18
- 5. 7 10 En la torre de absorción alcalina se presenta la siguiente reacción, que representa la conversión de los óxidos de nitrógeno a nitritos, en este caso de calcio, ya que la solución utilizada es una lechada de cal, pero se pueden utilizar otras soluciones. 8. 4NO2 + 2Ca(OH)2 →Ca(NO2)2 + 2H2O Este método consiste en pasar el ácido por torres de absorción rociadas con líquidos alcalinos, generalmente este lavado se hace con una suspensión de cal en una disolución de nitrato de calcio, esta solución reacciona con los óxidos de nitrógeno formando nitritos, los cuales se pueden recuperar por inyección de aire en una torre de inversión 3HNO2 HNO3 + 2 NO+ H2O 2 NO
- 6. Si se desean recuperar los nitratos producidos en la absorción alcalina, se les oxida a nitritos para que así puedan ser utilizados en la fabricación de otros compuestos, o de las nuevas lechadas a agregar en la torre. 9. 3Ca(NO2)2 + 4HNO3 3Ca(NO3)2 + 2H2O Este método de absorción alcalina disminuye en gran cantidad la posible contaminación de los óxidos de nitrógeno (NOx) y también evita que se entorpezcan las reacciones de producción de HNO3, aumentando un poco la concentración, de 50% que sale de la absorción ácida, a 60% después de la alcalina.
- 8. En la cámara con catalizador de platino reaccionan 4 NH3 + 5 O2 = 4 NO + 6 H2O En la cámara de oxidación: 2 NO + O2 = 2 NO2 En una torre de adsorción el dióxido de nitrógeno con agua forma: 4NO2 +2 H2O + O2 = 4HNO3 El proceso que se usa de manera general es el que explico el profe Refrigeran te enfría a 50`C Cámara de oxidación Torre de absorción Condiciones de la primera reacción T= 700-800`C P= 4-10 atmosferas exotérmica
- 9. Datos físicos: •Peso Molecular: 63g/mol •Punto de ebullición: 83ºC •Punto de fusión: -43ºC •Soluble en agua, en cualquier proporción y cantidad. •Densidad: 1,5 g/ml •Propiedades químicas: •Ácido inestable •De fácil disociación. •Fuertemente oxidante. •Ataca la materia orgánica, es tóxico y muy corrosivo, ataca las mucosas, en contacto con la piel la colorea de amarillo
- 10. HOJA DE SEGURIDAD VI ACIDO NITRICO FORMULA: HNO3 PESO MOLECULAR: 63.02 g/mol. COMPOSICION: H: 1.6 %; N: 22.23 % y O: 76.17 %. GENERALIDADES: El ácido nítrico es un líquido cuyo color varía de incoloro a amarillo pálido, de olor sofocante. Se utiliza en la síntesis de otros productos químicos como Colorantes fertilizantes Fibras plásticos Explosivos Es soluble en agua, generándose calor. No es combustible, pero puede acelerar el quemado de materiales combustibles y causar ignición. Es corrosivo de metales y tejidos. Si además, contiene NO2 disuelto, entonces se conoce como ácido nítrico fumante y su color es café-rojizo. Actualmente, se obtiene por oxidación catalítica de amoniaco.