termoquímica (mapa conceptual)
•Descargar como PPTX, PDF•
0 recomendaciones•3,377 vistas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
LÍQUIDOS PARCIALMENTE MISCIBLES-DIAGRAMAS TRIANGULARES (TRIÁNGULO DE GIBBS).

LÍQUIDOS PARCIALMENTE MISCIBLES-DIAGRAMAS TRIANGULARES (TRIÁNGULO DE GIBBS).Irvin de Jesús Rodríguez Martínez
Recomendados
LÍQUIDOS PARCIALMENTE MISCIBLES-DIAGRAMAS TRIANGULARES (TRIÁNGULO DE GIBBS).

LÍQUIDOS PARCIALMENTE MISCIBLES-DIAGRAMAS TRIANGULARES (TRIÁNGULO DE GIBBS).Irvin de Jesús Rodríguez Martínez
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Método pinch o método de pliegue - Transferencia de calor

Método pinch o método de pliegue - Transferencia de calor
Destacado
Destacado (20)
Mapa Conceptual Termoquímica Elvin Malpica 42 IUPSM Quimica I

Mapa Conceptual Termoquímica Elvin Malpica 42 IUPSM Quimica I
Similar a termoquímica (mapa conceptual)
Similar a termoquímica (mapa conceptual) (20)
Último
Desarrollo de habilidades del siglo XXI - Práctica Educativa en una Unidad-Ca...

Desarrollo de habilidades del siglo XXI - Práctica Educativa en una Unidad-Ca...Carol Andrea Eraso Guerrero
Contextualización y aproximación al objeto de estudio de investigación cualit...

Contextualización y aproximación al objeto de estudio de investigación cualit...Angélica Soledad Vega Ramírez
Último (20)
Desarrollo de habilidades del siglo XXI - Práctica Educativa en una Unidad-Ca...

Desarrollo de habilidades del siglo XXI - Práctica Educativa en una Unidad-Ca...
Amor o egoísmo, esa es la cuestión por definir.pdf

Amor o egoísmo, esa es la cuestión por definir.pdf
libro grafismo fonético guía de uso para el lenguaje

libro grafismo fonético guía de uso para el lenguaje
Contextualización y aproximación al objeto de estudio de investigación cualit...

Contextualización y aproximación al objeto de estudio de investigación cualit...
4° SES COM MAR 09 Leemos una noticia del dengue e identificamos sus partes (1...

4° SES COM MAR 09 Leemos una noticia del dengue e identificamos sus partes (1...
DIGNITAS INFINITA - DIGNIDAD HUMANA; Declaración del dicasterio para la doctr...

DIGNITAS INFINITA - DIGNIDAD HUMANA; Declaración del dicasterio para la doctr...
termoquímica (mapa conceptual)
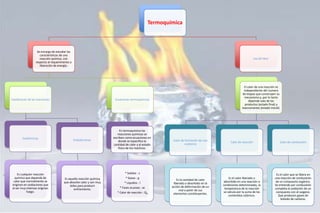
- 1. Termoquímica Se encarga de estudiar las características de una reacción química, con respecto al requerimiento o liberación de energía. Ley de Hess Clasificación de las reacciones Ecuaciones termoquímicas Exotérmicas En termoquímica las reacciones químicas se escriben como ecuaciones en donde se especifica la cantidad de calor y el estado físico de los reactivos. El calor de una reacción es independiente del numero de etapas que construyen su mecanismo y, por lo tanto depende solo de los productos (estado final) y reaccionantes (estado inicial). Es cualquier reacción química que dependa de calor que normalmente se originan en oxidaciones que al ser muy intensas originan fuego. Endotérmicas Calor de formación de una sustancia Calor de reacción Calor de combustión Es la cantidad de calor liberado o absorbido en la acción de deformación de un mol a partir de sus elementos constituyentes. Es el calor liberado o absorbido en una reacción a condiciones determinadas, la temperatura de la reacción se calcula por la suma de los contenidos calóricos. Es el calor que se libera en una reacción de combustión de un compuesto orgánico. Se entiende por combustión completa la oxidación de un compuesto con el oxigeno. Que producen gases de bióxido de carbono. * Solidos : s Es aquella reacción química que absorbe calor y son muy útiles para producir enfriamiento. * Gases : g * Líquidos : l * Fases acuosas : ac * Calor de reacción : QR
