Lek -saeure_basen_titration-1
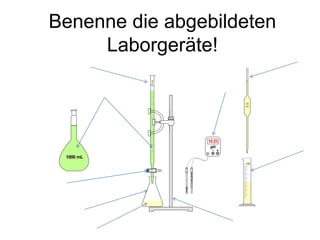
- 1. Benenne die abgebildeten Laborgeräte! 25mL 1000 mL mL 25 mL pH T B 10.23
- 2. Erstelle eine Titrationskurve mit der Achseneinteilung wie in Text II! Reaktionsgleichung: HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l) Hier wird eine bekannte Menge Base/ Lauge durch schrittweise Zugabe einer Säure mit bekannter Konzentration neutralisiert. Zugabe Titrant in [ml] pH-Wert Indikator: Phenolphthalein
- 3. Ermittle mit Hilfe von Quellen den Äquivalenzpunkt der Titrationskurve und zeichne diesen ein. Welche Bedingungen herrschen an diesem Punkt (chemisch, mathematisch)? Zugabe Titrant in [ml] pH-Wert HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l) Mathematisch: Der Äquivalenzpunkt ist der Wendepunkt der Titrationskurve einer Neutralisation. Chemisch: Am Äquivalenzpunkt wurde die entsprechende Stoffmenge an Säure zu einer Base gegeben (o.u.). Sie haben sich neutralisiert. Hier n(HCl) = n(NaOH) X
- 4. Recherchiere den Unterschied zwischen Äquivalenzpunkt und Neutralpunkt? Zeichne den Neutralpunkt ebenfalls ein! Zugabe Titrant in [ml] pH-Wert HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l) Der Neutralpunkt liegt immer bei pH=7. Er hat mit der Titrationskurve nichts zu tun.
- 5. Wieso verwenden wir ausgerechnet den Indikator Phenolphthalein für unsere Neutralisationstitration? Begründe anhand Abbildung III. Auswahlkriterium für einen Indikator Der passende Indikator für eine Neutralisationstitration hat einen Umschlagsbereich, der den Äquivalenzpunkt „umfasst“.
- 6. Berechne über die Reaktionsgleichung die Konzentration der unbekannten Natronlauge. HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l)
