Seguimiento presentación proteínas
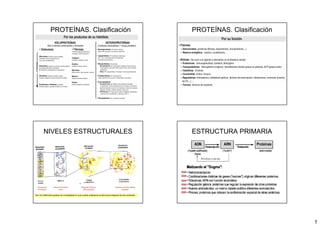
- 1. 1 PROTEÍNAS. Clasificación PROTEÍNAS. Clasificación NIVELES ESTRUCTURALES Son los diferentes grados de complejidad en que puede analizarse la estructura espacial de las proteínas Secuencia de aminoácidos Adopción de hélices y planos Plegamiento 3D de la cadena peptídica Asociación de varias cadenas peptídicas ESTRUCTURA PRIMARIA
- 2. 2 ESTRUCTURA PRIMARIA EFECTOS DE LOS CAMBIOS EN LA SECUENCIA GÉNICA: MUTACIONES ESTRUCTURA SECUNDARIA: α- HÉLICE ESTRUCTURA SECUNDARIA: α- HÉLICE ESTRUCTURA SECUNDARIA: HOJA β
- 3. 3 ESTRUCTURA SECUNDARIA: HÉLICE DE COLÁGENO ESTRUCTURA TERCIARIA FUERZAS QUE ESTABILIZAN LA CONFORMACIÓN NATIVA ESTRUCTURA TERCIARIA DESNATURALIZACIÓN IRREVERSIBLE: • La energía del estado nativo es mayor (menos estable) que la del estado desplegado. • La renaturalización no es posible ya que hay que superar una gran barrera de activación • (ej. Clara de huevo) Es la pérdida de la estructura terciaria (conformación nativa). Se manifiesta por: pérdida de funcionalidad (inactivación) y/o pérdida de solubilidad (precipitación) ESTRUCTURA TERCIARIA DESNATURALIZACIÓN Es la pérdida de la estructura terciaria (conformación nativa). Se manifiesta por: pérdida de funcionalidad (inactivación) y/o pérdida de solubilidad (precipitación) REVERSIBLE: • La energía del estado nativo es menor (más estable) que la del estado desplegado. • La renaturalización es espontánea –sin gasto energético- al retirar el agente desnaturalizante y rápida, debido al cooperativismo de los enlaces.
- 4. 4 TEMPERATURA Hasta los 40-50ºC, el aumento de T, favorece la solubilidad. Por encima de ese valor, se desnaturalizan. La Taq polimerasa usada en la RCP (reacción en cadena de la polimerasa) resiste los 95 ºC. ESTRUCTURA TERCIARIA FACTORES DESNATURALIZANTES pH Cuando el pH alcanza el punto isoeléctrico de la proteína, las moléculas proteicas adquieren cargas de diferente signo y se agregan, formando conglomerados de gran tamaño que precipitan. ESTRUCTURA TERCIARIA FACTORES DESNATURALIZANTES FUERZA IÓNICA (σσσσ) La fuerza iónica es una medida de la concentración de iones. A bajas concentraciones, los iones favorecen la solubilidad, pero, a medida que aumenta la fuerza iónica, los iones compiten con la proteína por el agua y la “secuestran”, con lo que la proteína precipita. ESTRUCTURA TERCIARIA FACTORES DESNATURALIZANTES ESTRUCTURA 3ª CHAPERONAS Y CHAPERONINAS En la célula, el plegamiento de las proteínas es facilitado por unas proteínas: las chaperonas. Los defectos se reparan en unos complejos proteicos: las chaperoninas
- 5. 5 ESTRUCTURA TERCIARIA DEDOS DE ZINC Son el motivo estructural más frecuente en los factores de transcripción, que han de encontrar un gen concreto entre los millones de nucleótidos del ADN. Consiste en bucles – ”dedos”-, estabilizados por átomos de Zn, cada uno de los cuales consta de una alfahélice y una hojabeta ESTRUCTURA TERCIARIA PRIONES En 1957, en tribus Fore de Nueva Guinea que practicaban el canibalismo ritual de los muertos y la endogamia, se descubre una enfermedad infantil del sistema nervioso a la que se denominó “kuru” (escalofrío). Se trataba de una enfermedad transmisible, tras una larga incubación de varios años. Los cerebros de estos individuos presentaban un aspecto espongiforme: neuronas hinchadas, con grandes vacuolas. Carleton Gajdusek Carleton Gajdusek obtuvo el Nobel en 1976 por su descubrimiento. Carleton Gajdusek ESTRUCTURA TERCIARIA PRIONES: Otras encefalopatías espongiformes Ya se conocía desde el siglo XVIII una enfermedad espongiforme similar que afectaba a los rebaños de carneros, denominada “tembladera” (scrapie), por los temblores y picazón intensa que presentan los animales. ESTRUCTURA TERCIARIA PRIONES: Otras encefalopatías espongiformes • A principios del siglo XX se describió la enfermedad de Creutzfeld-Jacob (ECJ), un tipo raro de demencia senil transmisible. • Entre 1985 y 1986 aparecieron numerosos casos en Francia, debido al tratamiento con hormona de crecimiento extraídas de hipófisis humanas procedentes de cadáveres
- 6. 6 ESTRUCTURA TERCIARIA PRIONES: Otras encefalopatías espongiformes • Entre 1988 y 1996 se desarrolló una epidemia de encefalopatía espongiforme bovina (EBB) en el Reino Unido, causada por incluirse en los piensos, harina de huesos y carnes procedentes de animales infectados. • Se produjeron casos de transmisión de la EEB desde los bóvidos al ser humano mediante una nueva variante de ECJ. ?? ESTRUCTURA TERCIARIA PRIONES: Las causas • Tenía carácter transmisible. • No se ajustaban a infecciones típicas al no existir procesos de inflamación o de respuesta inmune. • El agente “infeccioso” era sensible a proteasas y no a nucleasas, al contrario que los virus normales. ESTRUCTURA TERCIARIA PRIONES: Las causas En 1982 Stanley Prusiner propuso la hipótesis del PRIÓN: Proteinaceus Infectious Only. La causa de la enfermedad era una proteína normal, que se alteraba en los pacientes afectados y se acumulaba hasta valores 50 veces los normales en las terminaciones neuronales. La proteína normal tiene más hélices alfa que hojas beta y la anormal al revés, lo que hace que esté más replegada. Esto hace que la proteína patológica no se degrade y que se acumule, generando un efecto tóxico, induciendo la apoptosis en los tejidos nerviosos. ESTRUCTURA TERCIARIA PRIONES: Las causas
- 7. 7 ESTRUCTURA TERCIARIA PRIONES: Las causas El plegamiento anormal de la proteína era transmisible a las proteínas normales. Esto contradecía el dogma central de la biología molecular, ya que la estructura terciaria de una proteína no dependía sólo de su secuencia de aminoácidos. ESTRUCTURA CUATERNARIA La hemoglobina es una proteína oligomérica: un tetrámero ESTRUCTURA CUATERNARIA Anticuerpos ESTRUCTURA CUATERNARIA Ventajas de la Estructura cuaternaria: • Se minimizan los errores que se producirían si sólo existiera una cadena. • Se produce un ahorro de ADN: evolución por duplicación • Las proteínas oligoméricas son más versátiles al ser más regulable su acción que las que carecen de estructura cuaternaria (cooperatividad)
