Miocardiopatias 2014
- 1. MIOCARDIOPATÍAS DR. FREDDY FLORES MALPARTIDA 2014
- 2. LAS MIOCARDIOPATÍAS ♦ Son un importante y complejo grupo de enfermedades que afectan al músculo cardíaco con múltiples etiologías y una expresión fenotípica muy variada. El concepto de “enfermedad del músculo cardíaco” ha sufrido grandes cambios a lo largo de la historia. ♦ A mediados de 1850 las miocarditis crónicas eran las únicas causas reconocidas de enfermedad del músculo cardíaco. ♦ En 1900, fue introducida la denominación de “enfermedades primarias del miocardio”, y recién en1957 se usó el término miocardiopatía por primera vez, surgiendo varias definiciones de miocardiopatías en los siguientes 25 años. En 1968, la OMS, definía las miocardiopatías como “enfermedades de diferentes etiologías desconocidas en las que predomina la cardiomegalia y la insuficiencia cardiaca”.
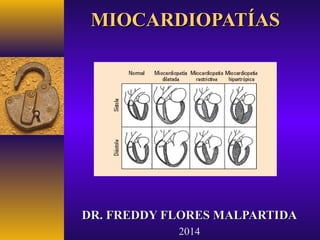
- 3. CARDIOMIOPATÍAS Clásicamente se describían 3 tipos clínicos que son: DILATADA HIPERTRÓFICA RESTRICTIVA Alteración primordial: SISTÓLICA (infiltración) DIASTÓLICA DIASTÓLICA
- 4. ♦ En 1995 define las miocardiopatías como “enfermedades del miocardio asociadas a disfunción cardiaca” y a las enfermedades específicas del músculo cardíaco las denomina miocardiopatías específicas, definiéndolas como “enfermedades del músculo cardíaco asociadas con trastornos específicos cardíacos o sistémicos” como la amiloidosis o la hemocromatosis. ♦ En esta nueva clasificación se recoge una nueva forma de miocardiopatía, con entidad propia, caracterizada por fibrosis e infiltración grasa del miocardio del ventrículo derecho que provoca muerte súbita en jóvenes y atletas, la miocardiopatía arritmogénica de ventrículo derecho. Otra nueva forma de miocardiopatía reconocida en esta clasificación es la miocardiopatía restrictiva idiopática, caracterizada por fibrosis intersticial y desorganización del miocardio en ausencia de enfermedad endomiocárdica. También dentro de las miocardiopatías no clasificadas, se introdujeron el miocardio no compactado, miocardiopatía ligeramente dilatada y la miocardiopatía mitocondrial. Las miocarditis asociadas a disfunción cardiaca fueron incluidas dentro de las miocardiopatías específicas y llamadas “miocardiopatías inflamatorias”. Los trastornos isquémicos, valvulares e hipertensivos, fueron considerados como “miocardiopatías específicas” cuando la severidad de la disfunción miocárdica excedía en gran parte al problema base (Tabla
- 11. CONTROVERSIAS: AHA 2006 vs SEC 2008 1. DIAGNÓSTICOGENÉTICO: – – SEC basada en un modelo genético; algunos conceptos genéticos son parecidos a los de la OMS de 1995. Clasifica en familiares (genéticas) y No familiares (no genéticas). AHA clasifica en Genéticas y No genéticas. 1. UTILIDAD CLÍNICA: No precisan en estrategias diagnósticas. 2. INCLUSIÓN DE LAS CANALOPATÍAS IÓNICAS: En el AHA 2006.
- 12. MIOCARDIOPATIA DILATADA Presentación Clinica Entre 20 a 50 años Embolia sistemica o Muerte subita Falla cardiaca (CF III-IV NYHA) Falla cardiaca izquierda Síntomas iniciales: disminución de la capacidad de ejercicio, disnea, palpitaciones, edema periférico Falla cardiaca derecha
- 15. La Miocardiopatía dilatada (MCD) es la forma más frecuente de miocardiopatía y se caracteriza por la dilatación y disfunción sistólica del ventrículo izquierdo (VI) en ausencia de otras enfermedades como la hipertensión (HTA), la enfermedad valvular, la cardiopatía isquémica o la cardiopatía congénita. Puede estar presente la dilatación y disfunción del ventrículo derecho (VD) pero no es necesario para el diagnóstico. Es la tercera causa más frecuente de insuficiencia cardiaca (IC) y la primera de trasplante cardiaco. Es más frecuente entre la tercera y cuarta década de la vida aunque puede aparecer a cualquier edad, en el sexo masculino y en la raza negra. Pueden ser primarias (2035% de los casos) si afectan predominantemente al miocardio, genéticas o adquiridas (80-65% restante) y secundarias a patologías sistémicas o de otros órganos. Es importante identificar las causas reversibles (Galve Basilio E, 2000; Maron BJ, 2006). Las formas genéticas o familiares suelen diagnosticarse más tempranamente que las adquiridas, que se identifican cuando ya existen signos de IC moderada o severa. La herencia de las formas familiares tiene una penetrancia incompleta y dependiente de la edad e incluye a más de 20 loci y genes. Aunque genéticamente heterogéneos, la herencia suele ser autosómica dominante (Maron BJ, 2006). La MCD puede ser secundaria a una multitud de enfermedades sistémicas, muchas de ellas muy poco frecuentes. Es importante tener en cuenta aquellas potencialmente reversibles, ya que su diagnóstico y tratamiento, implica la posible curación de la MCD.
- 16. ♦ ♦ En la MCD se observa dilatación ventricular, deterioro de la contractilidad y depresión de la fracción de eyección. Esto se produce por la degeneración de las células miocárdicas acompañada de fibrosis, necrosis de fibras musculares e infiltración celular. Además puede haber alteraciones de las proteínas estructurales o contráctiles: miosina, actina, troponina entre otras. Inicialmente puede mantenerse el gasto cardíaco debido al mecanismo de Frank-Starling y a que se compensa el aumento de volumen y presión telediastólicos intraventriculares con hipertrofia del miocardio, pero finalmente aparece congestión venosa retrógrada y fallo anterógrado con los síntomas clásicos de IC. Dada esta situación se inducirá retención hidrosalina y se activaran los mecanismos neurohormonales al igual que en la IC (Galve Basilio E, 2000).
- 17. CARDIOMIOPATÍA DILATADA ♦ Dilatación ventricular. ♦ Función sistólica ♦ Incidencia de 8/100 000 al año. ♦ Negros y hombres: 2.5+ riesgo.
- 18. PATOLOGÍA Macroscópicamente: Dilatación de 4 cámaras. Fcte: trombos murales. Válvulas: cicatrices y dilatación de anillos. Coronarias normales. Microscópicamente: Miocitos hipertrofiados y degenerados. Fibrosis intersticial. Ocasionalmente: grupos de linfocitos.
- 19. PATOGÉNESIS Injuria del miocito Contractilidad Volumen de eyección Pº de llenado Ventricular Congestión Pulmonar Congestión sistémica Dilatación de Ventrículo Izq Regurgitación Mitral Gasto Cardiaco Fatiga Debilidad
- 20. MIOCARDIOPATIA DILATADA Presentación Clínica Dolor torácico fibrilación atrial Arritmia ventricular
- 21. Examen físico ϕ Presión sistólica baja ϕ Presión de pulso estrecha ϕ Pulso alternante ϕ Venas Yugulares distendidas ϕ Hígado prominente y pulsátil ϕ Edema y ascitis
- 22. Examen físico ϕ En el precordio suele revelar impulso ϕ ϕ ϕ ϕ ϕ ventricular Izq, o Der Impulso apical desplazado Onda “a” pre sistólica palpable S2: normal o paradójico (BCRIHH) S4: casi universalmente presente Soplo sistólico
- 23. Historia clínica ♦ Historia familiar ♦ Enfermedades ligada al Cromosoma X – Duchenne o Becker – Steiner ♦ Mutaciones del DNA mitocondrial – DM familiar, sordera, epilepsia ♦ Desordenes metabólicos – Hemocromatosis
- 24. Historia clínica ♦ Deficiencias nutricionales – tiamina, deficiencia de carnitina, selenio, hipofosfatemia, hipocalcemia ♦ Enfermedades endocrinas ♦ Historia farmacologica completa – Antraciclyna, cocaina ♦ Exposicion a enfermedades virales – VIH o VHC
- 25. HISTORIA NATURAL: ♦ Curso variable: asintomáticos hasta sintomáticos. ♦ Sintomáticos: 25% mueren en un año. 50% en 5 años.
- 26. FACTORES ASOCIADOS A PEOR PRONÓSTICO: S3 Retraso del S. Conducción. Pº de llenado ventricular. Edad >55. Dilatación Cardiaca. GC FE Na Norepinefrina CF IC< 2.5L/min/m2. Hipotensión HTTP PVC Presión en cuña >20mmHg Síncope Dilatación de VD indep Arritmias Ventriculares Hallazgos en Bx Ventrículo esférico. Test de Ejercicio Cardiopulmonar (<1012mlO2/Kg/min)
- 27. CAUSAS ♦ IDIOPÁTICA ♦ Inflamatoria: – Infecciosa – No infecciosa • Enf del tjdo conectivo • CMP peripartum • Sarcoidosis ♦ Tóxica: – Ingestión crónica de OH – Agentes Quimioterápicos ♦ Metabólica: – Hipotiroidismo – Hipocalcemia o hipofosfatemia crónica ♦ Neuromuscular: – Distrofias musculares y miotónicas
- 28. FASE 1 Injuria Miocárdica Inicial FASE 2 Injuria Miocárdica Autoinmune FASE 3 Miocardiopatía Dilatada
- 29. Miocarditis viral y otros agentes citotóxicos: Bowles: presencia viral en CMD: 50%. Recientes estudios: 35%. A pesar de evidencia, no se ha demostrado patogénesis. Weiss: RNA enteroviral en otros desórdenes cardiacos y corazones normales.
- 30. EVALUACION DIAGNOSTICA Identificar causas reversibles: consumo de alcohol concentraciones séricas de fósforo (hipo) calcio sérico (hipo) Creatinina sérica y urea (uremia) función tiroidea (hipo e híper) estudio de Fe ( hemocromatosis) VIH
- 31. EVALUACION DIAGNOSTICA NO INVASIVAS ♦ Rx de tórax: – Cardiomegalia y redistribución pulmonar venosa son comunes – Edema alveolar o intersticial no es común
- 32. ECG Normal Cambios aislados la onda T Ondas Q Prolongación de la conducción AV Bloqueo de rama Taquicardia sinusal Arritmia supraventricular (FA) Taquicardia ventricular Pobre progresión de R
- 33. Criterios Diagnostico MD I ECOCARDIOGRAFIA ♦ Esencial ♦ Otras: scans radionúclido, RM ♦ Criterios eco cardiográficos para CMD idiopática Fracción de eyección <45% y/o disminución de la fracción en mas del 25% Dimensión ventricular izquierda diastólica final muy dilatada CRITERIOS DE EXCLUSION X Presencia de HTA (> 160/100 mm Hg) x Enf arterial coronaria (> 50% en uno o mas princ ramas) x consumo crónico de OH (> 40 g/d M,> 80 g/d H x mas de 5 años) x Enf sist conocida que cause MCD I x Enf pericárdica x Enf Cardiaca congénita x Cor pulmonale
- 34. ECOCARDIOGRAFIA
- 35. ECOCARDIOGRAFIA
- 36. VENTRICULOGRAFIA RADIONUCLIDA Revela el incremento del volumen diastolico/ sistolico final La reducción de la fracción de eyección Motilidad de las paredes
- 37. PRUEBA DE ESFUERZO ♦ Capacidad de ejercicio ♦ Evaluar la progresión de la enfermedad ♦ Evaluar pronostico ♦ Seleccionar pacientes para transplante cardiaco ♦ Distinguir de anormalidades metabolicas
- 38. SEROLOGIA VIRAL ♦ Cultivo viral ♦ Serologia viral – Aumento de titulos de anticuerpos neutralizadores – IgM especificos
- 39. Biopsia endomiocárdica ♦ Enfermedades miocárdicas ♦ Cardiomiopatía inflamatoria ♦ Hemocromatosis ♦ Enfermedad infiltrativa o maligna ♦ Inmunohistológico: – Incremento de cel T – Incremento de expresión de MCH
- 40. TRATAMIENTO El tratamiento especifico no es posible El tratamiento es el de ICC ♦ Control de los síntomas ♦ Prevenir la progresión a ICC ♦ Prevenir complicaciones Diuréticos : síntomas de congestión, pero no como monoterapia
- 41. TRATAMIENTO IECA Activación del SRAA: fisiopatología Independiente de la clase funcional Mejora -disnea -tolerancia al ejercicio -reduce el promedio de hospitalizaciones -reduce la mortalidad CV -previenen o mejoran la progresión de la enfermedad en pacientes asintomáticos
- 42. TRATAMIENTO ♦ Según el estadío de Falla Cardiaca
- 43. Nuevos potenciales Tx PEPTIDO NATRIDIURETICO Libera por distensión Induce: diuresis, natridiuresis, vasodilatación, supresión del SRAA Concentraciones elevadas en ICC PERO tolerancia se desarrolla durante administración IV Futuro: inhibición de endopeptidasa neutral
- 44. Nuevos potenciales Tx ANTAGONISTA DE CITOQUINA TNF: macrofagos, cel T act, miocardio TNF dañado – Edema pulmonar, cardiomiopatia, caquexia, reduce el flujo sanguíneo periférico TNF, IL6 Pentoxifilina, etarnecept ENDOTELINA
- 45. Nuevos potenciales Tx ANTICOAGULANTES Riesgo de tromboembolismo bajo En pacientes jovenes y con factores de riesgo de tromboembolismo No hay estudios que sustenten su uso Historia de tromboembolia, trombo IC
- 46. Manejo de Arritmias Limitaciones: efecto inotropico negativo efecto proarritmico Taquicardia ventricular no sostenida es alta La terapia farmacologica no mejora supervivencia
- 47. Nuevos tratamiento No farmacologicos VENTRICULOTOMIA PARCIAL IZQUIERDA Hipótesis basada en la Ley de LaPlace: tensión de la pared esta relacionada al diámetro ventricular izquierdo Limitado a centros con experiencia
- 48. Nuevos tratamiento No farmacologicos DISPOSITIVOS VENTRICULARES IZQ DE AYUDA Como puente para transplante cardiaco Mejora función ventricular izquierda
- 49. TERAPIA BASADA EN LA INFLAMACION Vacunacion contra virus cardiotropicos Inhibir la union virus-receptor 2do mensajeros alterados Mejora luego de infeccion viral (CMV) Plasmaferesis
- 50. TERAPIA BASADA EN LA INFLAMACION ♦ Globulina hiperinmune ♦ Terapia inmusupresora ♦ Anticitoquinas ♦ De acuerdo al estadio de la enfermedad
- 51. Transplante Cardiaco ♦ Principal indicación en niños y en adultos ♦ Mejora la calidad de vida
- 52. Formas secundarias de MCD: ♦ Alcohólica ♦ Farmacológica (RAM a Adriamicina o doxorubicina, Ciclofosfamida, Cocaina) ♦ Periparto ♦ Por enfermedades Neuromusculares ♦ VIH ♦ Conectivopatías (LES, PAN, Sarcoidosis)
- 53. ♦ La Miocardiopatía Hipertrófica (MCH) es una enfermedad con una importante heterogenicidad genética, clínica y pronóstica. Es la causa más común de muerte súbita durante el esfuerzo físico en gente joven, por lo que su diagnóstico es de gran importancia en los grupos de alto riesgo de muerte súbita. Es una enfermedad genética primaria del sarcómero cardíaco de transmisión autosómica dominante, causada por mutaciones en genes que codifican diferentes componentes del aparato contráctil, con manifestaciones clínicas, morfológicas, fisiopatológicas y genéticas moleculares especiales. La incidencia total de la MCH es baja, de un 0.2% de la población general (1:500) y de un 0.5% de los pacientes no seleccionados que se remiten para realizarles un ecocardiograma. Una considerable proporción de individuos portadores de la mutación genética para MCH no son descubiertos clínicamente. Probablemente sea la enfermedad cardíaca transmitida genéticamente más frecuente. La mortalidad global anual en pacientes con MCH es aproximadamente del 1% / año, y del 2% / al año en pacientes con MCHO. La incidencia de arritmias y muerte súbita se atribuye a las propiedades electrofisiológicas alteradas de los miocitos deformes.
- 54. CARDIOMIOPATÍA HIPERTRÓFICA Dx: Ecocardiografía bidimensional: Hipertrofia VI asimétrica, difuso o localizado. Asociado a un VI no dilatado e hiperdinámico. Con o sin obstrucción del tracto salida. Mayoría sin obstrucción al tracto de salida en condiciones basales (pueden ser provocadas).
- 55. 25% existe Obstrucción Al TSVI SAM: Mov. Sistólico Anterior
- 56. PATOLOGÍA MACROSCÓPICA: masa miocárdica. Cavidades ventriculares pequeñas. Aurículas dilatadas e hipertrofiadas. Mayor compromiso septal y anterolateral. Patrones: HAS, H. concéntrica, localiz. Inusuales, H. apical (1/4Japón, conf. en espada, -T gigantes en precordiales, no gradiente, st moderados).
- 57. HISTOLOGÍA: Bandas musculares hipertrofiadas y desorganizadas Arquitectura miofibrilar desorganizada. Fibrosis. Focos desorganizados entremezclados con áreas “sanas”. Desarreglos en >5%. Art coronarias intramurales: lumen pequeño, pared engrosada.
- 58. CARDIOMIOPATÍA HIPERTRÓFICA Obstrucción de Flujo De VI MIOCITO HIPERTROFIADO Desarreglo de Miofibrillas Arritmias Ventriculares HVI Relajación Disfx Diastólica Pª Sistólica Consumo de O2 Pª telediastólica ANGINA MUERTE SÍNCOPE SÚBITA DISNEA Rejurgitación Mitral GC Insufic con ejercicio
- 60. FISIOPATOLOGÍA Obstrucción al tracto de Salida. Murmullo de eyección sistólico apical. Hipertrofia de porción basal del septum. VM grande y alargada. Obstrucción SUBAÓRTICA: x SAM, cuya regurgitación se dirige posteriormente en AI. 5% por aposición muscular en región cavidad media (involucrando inserción anómala de m. papilar anterolateral o una excesiva hipertrofia)
- 61. Subgrupos hemodinámicos: Gdte obstructivo (en reposo) >=30mmHg. Latente (provocable), <30mmHg en CB y >=30mmHg en provocación. No obstructivo: en condiciones basales y provocables…<30mmHg. Maniobras inductoras: Nitrato, Valsalva, infusión de dobutamina o isoproterenol,postura de pie y ejercicio.
- 62. GENÉTICA Y DX MOLECULAR CMH herencia Auto. Dominante, por una mutación en uno de 10genes. Mutaciones +fcts (40%):Cadena pesada de Miosina (20%) Miosina-lig a prot C. (15%)Troponina T. (20%)a-Tropomiosina
- 63. MANIFESTACIONES CLÍNICAS Mayoría asintomáticos. Cdro varía. Identificada gralm entre 30-40a. En jóvenes, primera manif: muerte súbita; arritmias cardiacas. Pctes ancianos: hipertrofia moderada, gdts de Pº, st marcados>55a. St +común: disnea, tb angina, fatiga, pre y síncope. Palpitaciones, DPN e IC menos fcts.
- 64. MANIFESTACIONES CLÍNICAS Ejercicio tiende a exacerbar muchos st. Isquemia miocárdica. Alto riesgo de muerte súbita. Síntomas progresivos: disnea al ejercicio, dolor de pecho, conciencia ; con una fx sistólica del VI conservada. Progresión a una ICC c/remodelación y disfunción sistólica. Complicaciones atribuibles a FA.
- 65. EXAMEN FÍSICO Impulso ventricular apical desplazado lateralmente, reforzado y alargado. Impulso apical presistólico x contracción auricular… doble impulso apical. 3er impulso, cuando corazón está casi vacío. Onda “a” prominente. Pulso carotídeo:
- 66. EXAMEN FÍSICO S1 (N); S2 dividido y en los pcts c/gdts severas: desdob. paradójico. Sonido de eyección sistólica. SS, (mesosist), entre ápex y borde EI, holosist si se añade regurgitación mitral. SD, reflejando un regurgitación Mitral incrementada.
- 67. EKG ECG (N) en sólo 15%, en hipert localizadas. +comunes: segmentos ST y T anormales, HVI -T en precordiales en CMH apical. Q prominentes en 20 a 50% de pcts (II,III,aVF y en V2 a V6). Eje eléctrico anormal, usual desviación izq. P anormales. Arritmias Ventriculares son comunes (3/4) TV no sostenida (1/4), TVMS son poco comunes. Taquicardia supraventricular. FA en 10% de pcts.
- 68. Factores de Riesgo para muerte súbita en CMH CRITERIOS MAYORES: Arresto cardiaco (Fibrilación ventricular) TV sostenida espontánea. Hist. Familiar de una MS prematura. Síncope inexplicado. TV no sostenida (3lat o + y por lo menos 120x’). PA en ejercicio anormal. HVI >=30mm.
- 69. TRATAMIENTO: • MÉDICO: (FÁCIL, IC DIASTÓLICA Consistente en disminuir demanda de O2 por miocardio y relajar el miocardio) – – – – ELECCIÓN: Beta Bloqueantes (Si contraindicación, Ca antag no DHP) CUIDADO CON diuréticos CONTRAINDICADOS VD: IECAs y Digital Arritmias Ventriculares: Amiodarona, Dronedarona, DAI • OTROS: (si no responden a tratamiento Médico) – Miectomía septal de Morrow en los muy sintomáticos – Ablación septal con alcohol intraarterial – Marcapasos DDD (bicameral)
- 70. TRATAMIENTO: BETABLOQUEADORES MAL PRONOSTICO POR ARRITMIAS VENTRICULARES
- 71. 3. MIOCARDIOPATÍA RESTRICTIVA ETIOLOGÍA: a) Alteración de la distensibilidad miocárdica FALLO DIASTÓLICO – Depósito de material intramiocárdico: AMILOIDOSIS es la causa más frecuente (primaria) Otras (fibroelastosis endomiocárdica de Davis, Fibrosis endomiocárdica de Loeffler, Churg-Strauss, Glucogenosis…) – b) CLÍNICA DATOS QUE ORIENTAN A AMILOIDOSIS: • • • • • • • • > 50 años Tendencia a hTA (mareos por hTA ortostática) Edemas blandos en MMII Macroglosia Malabsorción Púrpura Proteinuria RIESGO DE INTOXICACIÓN DIGITÁLICA AUMENTADO GRAN RIESGO DE MS
- 72. ♦ La miocardiopatía restrictiva (MR) es una enfermedad del miocardio y/o endocardio que se caracteriza por un aumento de la rigidez ventricular, lo que produce alteraciones en la relajación cardiaca (disfunción diastólica). Es la menos frecuente de las miocardiopatías, constituyendo menos del 5% de todas ellas en nuestro medio (Galve E, 2000). La pérdida de distensibilidad cardiaca que la caracteriza se produce normalmente por enfermedad del miocardio o endomiocardio de diversas etiologías, que endurece el corazón por infiltración o fibrosis. ♦ Las MR primarias son enfermedades intrínsecas del corazón y se clasifican histopatológicamente. Incluyen la fibrosis endomiocárdica, la endocarditis de Löffler y la forma idiopática. Las secundarias son más frecuentes, e incluyen enfermedades multisistémicas en las que el corazón puede afectarse. Éstas se clasifican a su vez en no infiltrativas (por ejemplo, enfermedad carcinoide cardiaca, toxicidad por antraciclinas), infiltrativas (por ejemplo amiloidosis o sarcoidosis) o enfermedades de depósito (por ejemplo, hemocromatosis, enfermedad por depósito de glucógeno, enfermedad de Fabry). ♦ En las enfermedades intersticiales los infiltrados se localizan entre los miocitos, mientras que en las de depósito los acúmulos ocurren dentro de las células.
- 74. … MIOCARDIOPATÍA RESTRICTIVA c) DIAGNÓSTICO ♦ EF: – – – – Protodiástole CONSERVADA (a diferencia de Taponamiento Cardiaco (Pandiástole) Signo de Kussmaul (PVC en inspiración aumenta Puede haber Pulso Paradójico (disminución de > 10 mmHg de TAs en inspiración): menos que en Taponamiento Tonos Cardiacos apagados
- 75. … MIOCARDIOPATÍA RESTRICTIVA c) DIAGNÓSTICO ♦ ♦ ♦ Rx Tórax: No Cardiomegalia ECG: Bajo Voltaje de QRS ECOCARDIOGRAMA: Miocardio de aspecto MOTEADO Cateterismo: ♦ – Algo > P en cavs izqdas, aunque muy igualadas d) TRATAMIENTO ♦ ♦ Sintomático OJO Intoxicación Digitálica!!!
- 76. MIOCARDIOPATIA NO COMPACTADA ♦ ♦ ♦ ♦ La miocardiopatía no compactada (MNC), también conocida como “miocardiopatía espongiforme" (Olsen SR, 2005), consiste en una anomalía congénita muy infrecuente de la morfología del miocardio, con recesos intratrabeculares muy profundos comunicados libremente con la cavidad ventricular. De esta forma, el miocardio tiene dos capas: una subepicárdica fina (compactada), y otra gruesa subendocárdica y trabeculada (no compactada). La MNC se da como resultado de una detención del proceso normal de compactación de la pared ventricular que ocurre entre las 5 y 8 semanas de vida intrauterina (Freedom RM, 2005; Varnava AM, 2001). La miocardiopatia no compactada (MNC) se caracteriza por la presencia de trabeculaciones prominentes y profundos recesos que a menudo se localizan en segmentos hipertrofiados e hipoquinéticos del ventrículo izquierdo (VI). Por definición la MNC se presenta en ausencia de otras cardiopatías estructurales (Jenni R, 2001). Aunque en los últimos años se han realizado grandes avances en la comprensión de los orígenes genéticos y la biología de las miocardiopatías, la clasificación de las mismas sigue siendo compleja y controvertida. Según la clasificación WHO/ISFC (Richardson P, 1996), la MNC sería una miocardiopatía no clasificada, aunque recientemente ha sido clasificada como una miocardiopatía primaria (es decir, que afecta predominantemente al miocardio) y con base genética (Maron BJ, 2006; AHA 2006).
- 77. ♦ La MNC tiene una prevalencia en la población general del 0.05 % y del 0.014 % (Oechslin E, 2002).
- 78. DISPLASIA ARRITMOGENICA DEL VD ♦ La Miocardiopatía Arritmógena de Ventrículo Derecho (MAVD), también conocida como displasia arritmogénica del ventrículo derecho, es una enfermedad del músculo cardiaco de origen genético, caracterizada por una atrofia miocárdica ventricular derecha y reemplazo por fibrosis y grasa, que puede producir una inestabilidad eléctrica que desencadene arritmias ventriculares y muerte súbita (Gemayel C, , 2001; Sen-Chowdhry S, 2004). Inicialmente se producen alteraciones del movimiento de la pared regional, progresando más tarde con alteraciones globales y dilatación del VD. El tejido reemplazado puede afectar a áreas del VI, respetando el septum (Richardson P, 1996). Se estima una prevalencia de 1:1000 (Gemayel C, 2001). ♦ No se sabe si la existencia de un componente genético predispone a la enfermedad, o tiene un origen infeccioso o autoinmune. La MAVD sería de acuerdo a la clasificación WHO/ISFC (Richardson P, 1996), una miocardiopatía no clasificada, pero recientemente ha sido clasificada como una miocardiopatía primaria (es decir, que afecta predominantemente al miocardio) y con base genética (Maron BJ, 2006).
Notas del editor
- HDL as a Therapeutic Target
