Victoria valdes tablaexpos_eim_ich_2021-1 () (1)
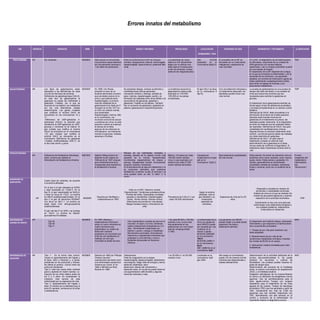
- 1. EIM HERENCIA VARIANTES OMIM HISTORIA SIGNOS Y SINTOMAS PREVALENCIA LOCALIZACION CROMOSOMIC Y GEN ESPERANZA DE VIDA DIAGNOSTICO Y TRATAMIENTO CLASIFICACION FRUCTOSEMIA AR Sin variantes. #226900 Dato exacto no encontrado. Los primeros casos descritos son de pacientes menores a 1 sin datos de publicación. Entre los síntomas de la IHF se incluyen vómitos, hipoglucemia, ictericia, hemorragias, hepatomegalia, hiperuricemia y potencial fallo renal. Los pacientes de mayor edad con IHF típicamente eligen por sí mismos una dieta baja en fructosa para evitar los síntomas, incluso antes de ser diagnosticados. Gen ALDOB localizado en el Cromosoma (9q22.3) El pronóstico de la IHF es favorable con un crecimiento, inteligencia y esperanza de vida normales. En la IHF, el diagnóstico de los heterocigotos es dificultoso, requiriendo de un cribado de ADN genómico con sondas alélicas específicas, o de un ensayo enzimático a partir de una biopsia de hígado. El tratamiento de la IHF depende de la etapa en la que se encuentra la enfermedad, y de la severidad de los síntomas. Los pacientes estables, sin eventos de intoxicación aguda se tratan planificando cuidadosamente la dieta para evitar la ingesta de fructosa y sus precursores metabólicos. TMP GALACTOSEMIA AR Los tipos de galactosemia están asociados a las deficiencias de cada uno de los tres tipos de enzimas. Deficiencia de galactoquinasa (GALK): en este tipo de galactosemia la galactosa no puede ser fosforilada a galactosa 1-fosfato, por lo que se acumula en los tejidos y se metaboliza por las vías alternativas citadas anteriormente. Los genes mutados que codifican el enzima GALK se encuentran en los cromosomas 15 y 17. Deficiencia de UDP-galactosa 4- epimerasa (GALE): la reacción que transforma la UDP-galactosa en UDP- glucosa y viceversa no se realiza. El gen mutado que codifica el enzima GALE se encuentra en el cromosoma 1.El gen mutado que codifica el enzima GALE se encuentra en el cromosoma Deficiencia de galactosa 1-fosfato uridiltransferasa (GALT): es el tipo más común y grave. #230400 En 1908, Von Ruess presentó el caso de un lactante alimentado al pecho que excretaba azúcar en la orina y que además tenia hepatomegalia, la primera mención detallada de la galactosemia fue dada por F. Groppert en el año 1917 en un niño con retardo mental, que presentaba hepatomegalia, ictericia, fallo en el crecimiento, con excreción anormal de azúcar y proteínas por orina; en este paciente cuando se sustituyó la lactosa de la dieta, algunos de los síntomas se normalizaron, con tolerancia normal a la glucosa, maltosa, sacarosa y fructosa Se presentan letargo, rechazo al alimento y manifestaciones tóxicas generales, incluyendo vómitos y diarreas, pérdida de peso, ictericia, hepatomegalia, ascitis y la formación de cataratas entre otros debido a la acumulación de galactosa, galactitol y galactosa 1-fosfato en los tejidos. También hay un aumento de galactosa y galactitol en plasma, galactosuria e hiperaminoaciduria. La incidencia anual de la galactosemia clásica está estimada en 1/40.000- 1/60.000 en los países occidentales. El gen GALT se situa en el cromosoma 9 (9p13) Con una detección temprana y un tratamiento adecuado, los afectados pueden llevar una vida normal. La prueba de galactosemia es una prueba de sangre (del talón del bebé) o una análisis de orina que busca tres enzimas que son necesarias para cambiar la galactosa en glucosa. El tratamiento de la galactosemia también se divide según el tipo de deficiencia enzimática, y se basa principalmente en un estricto control dietético. Deficiencia de GALK: debe procederse a la eliminación de la leche de la dieta (parecen tolerarse otras fuentes menores de galactosa).Si el tratamiento es precoz, las cataratas pueden resolverse. Si el diagnóstico es tardío es habitual que las cataratas deben ser operadas. Deficiencia de GALE: hay gran variabilidad de manifestaciones clínicas. Algunas formas no precisan tratamiento (solo control). Las formas graves deben ser tratadas con dieta restrictiva en galactosa. Deficiencia de GALT: en este caso el tratamiento consiste en eliminar toda administración de la galactosa en la dieta, incluso antes de confirmar el diagnóstico. El tratamiento debe mantenerse durante todo la vida TMP FENILCETONURIA AR Deficiencia de fenilalanina hidroxilasa (pah), enzima que cataliza la hidroxilación de fenilalanina a tirosina. #261600 Asbjörn fölling primero en describir la pku clásica en 1934.jervis en 1947 propuso que la fenilcetonuria es la incapacidad para transforma la fenilalanina a tirosina. Retraso de las habilidades mentales y sociales, tamaño de la cabeza mucho más pequeño de lo normal, hiperactividad, movimientos espasmódicos de brazos y piernas, discapacidad mental, convulsiones, erupción cutánea y temblores. Si la fenilcetonuria se deja sin tratamiento o si se consumen alimentos que contienen fenilalanina, el aliento, la piel, el cerumen y la orina pueden tener un olor "a ratón" o "a moho’’. México: 3.6 casos por cada 100,000 recién nacidos vivos, lo que equivale a un enfermo por cada 27,546 recién nacidos tamizados. Causada por mutaciones en el gen pah en el cromosoma 12q23.2. Bajo tratamiento posibilidades de vida normal. DIeta estricta: Se evitan los alimentos ricos en proteínas como carne, pescado, aves, huevos, queso, leche, frijoles secos y guisantes. En cambio, generalmente se recomiendan cantidades medidas de cereales, almidones, frutas y verduras, junto con un sustituto de la leche. Errores congénitos del metabolismo intermediario, tipo “intoxicación”. SINDROME DE SANFILIPPO AR Cuatro tipos de variantes, de acuerdo a la enzima afectada: En el tipo A el gen afectado es SGSH y está localizado en 17q25.3. En el tipo B, el gen responsable es NAGLU y tiene su locus en 17p21. La enzima es alfa-N acetilglucosaminidasa .En el tipo C el gen se denomina HGSNAT con locus en 8p11.1. La enzima es acetil acetil CoA: alfa-glucosamina acetiltransferasa. El gen del tipo D es GNS y se localiza en 12q14. La enzima es Nacetil- glucosamina-6-sulfatasa. #252900 Descrita por Sanfilippo y colaboradores en 1963 Daño en el SNC, Deterioro mental, Hiperactividad, Tendencias autodestructivas, Perdida del habla, Opacidades cornéales escasas o inexistentes, Hepatomegalia, Caries, Rinitis crónica, Diarrea crónica, Infecciones recurrentes en vías aéreas, Rasgos faciales toscos y Abundancia de vello. Prevalencia de 0.28 a 4.1 por cada 100,000 nacimientos. Según la enzima afectada, varia el gen afectado y su localización (apartado de variantes). Esperanza de vida de 8 a 25 años. Diagnostico prenatal por estudio de amniocitos o vellosidades coriónicas. Análisis de orina en el que se analizan los niveles de glucosaminoglicanos y examen especifico de la actividad enzimática. Actualmente no hay una cura para esa enfermedad; solo tratamientos dirigidos a los cuidados paliativos, tratamientos moleculares en desarrollo. TMP ENFERMEDAD JARABE DE MAPLE AR Tipo IA Tipo IB Tipo I1 #248600 En 1954, Menkes y colaboradores informaron sobre un nuevo síndrome en cuatro hermanos que presentaban un cuadro de disfunción cerebral progresiva con excreción por orina de una substancia no habitual con olor que recordaba al jarabe de arce. Olor característico a jarabe de arce en el cerumen, el sudor y la orina, Síntomas sutiles inespecíficos emergentes en 2-3 días, Alimentación inadecuada con biberón o pecho, Letargo e irritabilidad, Movimientos anormales, Somnolencia Hipertonía y espasticidad crecientes que progresan a convulsiones y coma y Episodios temporales de hipotonía extrema. 1 de cada 86.800 a 185.000 nacidos vivos, ocurre más frecuentemente en las poblaciones con una mayor tasa de consanguinidad (1:380) La enfermedad de la orina con jarabe de arce (MSUD) puede ser causada por una mutación en al menos 3 genes: BCKDHA (608348) en el cromosoma 19q13 BCKDHB (248611) en el cromosoma 6q14 DBT (248610) en el cromosoma 1p21 Las personas con MSUD pueden llegar a la edad adulta siguiendo una dieta y tratamiento estrictos. El tratamiento de la MSUD clásica, intermedia, intermitente y que responde a la tiamina tiene tres componentes principales: 1. Terapia de por vida para mantener una dieta aceptable. 2. Mantenimiento de por vida de las condiciones metabólicas normales, incluidos los niveles de BCAA en el cuerpo. 3. Intervención médica inmediata para crisis metabólicas. AMC ENFERMEDAD DE GAUCHER AR Tipo 1: Es la forma más común. Causa un agrandamiento del hígado y el bazo, dolor y fracturas y, a veces, problemas en los pulmones y riñones. No afecta al cerebro. Común entre los judíos de Ashkenazi. Tipo 2: este tipo causa daño cerebral grave y aparece en recién nacidos. La mayoría de los niños fallece antes de los 2 o 3 años. Es considerado la mutación más severa de esta enfermedad por su esperanza de vida. Tipo 3: Agrandamiento del hígado y bazo. El cerebro se ve afectado poco a poco.En general, comienza en la niñez o adolescencia. #230800 Descrito en 1882 por Philippe Charles Gaucher , caracterizda mas tarde como una enfermedad autosomica recesiva por Goren JF en 1948 y definida por Brdy Roscoe en 1965. Osteoporosis Falta de coagulación en la sangre hepatomegalia, esplenomegalia, desórdenes neurológicos, fatiga, falta de energía y ánimo, abdomen distendido, dolor abdominal, retardo del crecimiento y desarrollo óseo. En la piel se puede observar una pigmentación café-amarilla y algunas manchas redondas y lisas. 1 en 50.000 a 1 en 60.000 nacidos vivos. Localizado en el cromosoma 1q22 gen GBA Alto riesgo en el embarazo, puede vivir de manera normal mientras sea diagnosticada y tratada debidamente. Determinación de la actividad deficiente de la enzima glucocerebrosidasa ß. Se puede dosificar en leucocitos y cultivos de fibroblastos. Las pruebas pueden hacerse en gotas de sangre seca. Determinación del aumento de la Fosfatasa ácida, la enzima convertidora de angiotensina (ACE), y la fosfatasa alcalina. Imágenes radiológicas de los huesos.Reposo en cama y la utilización de analgésicos (nunca aspirina). Uso de antiinflamatorios para el dolor agudo-crónico Terapia con oxígeno hiperbárico para el tratamiento de las crisis agudas de los huesos. Terapia de reemplazo enzimático (TRE) que fue aprobada a partir de 1991. Actualmente son más de 3.500 los pacientes que han recibido tratamiento con TRE, demostrando una alta eficacia en el control y evolución de la enfermedad. Es importante realizar el diagnóstico precoz. AMC Errores innatos del metabolismo
- 2. HIPOTIROIDISMO CONGENITO AR 1) Primario: cuando hay alteraciones en la organogénesis de la tiroides o en su capacidad para sintetizar hormonas tiroideas. 2) Central: provocado por la deficiencia de otras hormonas sintetizadas en la adenohipófisis o en el hipotálamo. 3) Periférico: defectos en el transporte intracelular de las HT, alteraciones estructurales de los receptores de HT, o del metabolismo de las hormonas tiroideas, por la baja actividad de las desyodinasas. #275200 Es una enfermedad que se conoce desde el siglo 15, donde las personas que sufrían de esta condición eran llamados cretinos. Curling en 1850 describió el primer niño con manifestaciones de HC y la ausencia de la glándula tiroides. Bruchy y McCune en 1944 relataron el desarrollo mental de niños hipotiroideos con tratamiento adecuado. 95% de los RN con HC son asintomáticos o pueden presentar síntomas muy sutiles como fontanela posterior abierta (> 0.5 cm). Desarrollará en forma progresiva hipotonía, succión débil, hipotermia, ictericia persistente, piel seca, hernia umbilical, llanto ronco, Retraso en el neurodesarrollo, Facie mixedematosa: rasgos toscos, ensanchamiento del tabique nasal, párpados y labios tumefactos con macroglosia. 1: 3000 o 4000 recién nacidos vivos, es la más frecuente de las enfermedades endocrinas. GEN: TSH-R (activación de las vías metabólicas de tiroides) LOCUS: 14q31.1 El pronóstico es bueno para la vida; sin embargo, para el desarrollo neurológico dependerá de la edad de inicio del tratamiento. Relación inversa entre el coeficiente intelectual (CI) y la edad de inicio del tratamiento. El tratamiento con hormonas tiroideas debe iniciarse una vez obtenida la muestra de confirmación. El objetivo del tratamiento es normalizar los niveles de T4 en 2 semanas y los de TSH en un mes. Se administra levotiroxina, el comprimido debe ser triturado y disuelto en leche materna, fórmula o agua. Tratamiento con 10 a 15 ug/kg/ día de levotiroxina TMP ACIDEMIA ISOVALERICA AR 1. Forma aguda neonatal 2. Forma crónica intermitente 3. Forma lentamente progresiva #243500 Fue la primera acidemia orgánica en ser descrita a mediados de los años 60s por Tanaka, Efron y Budd. El primer paciente fue un neonato que presentaba acidosis metabólica y un olor característico a pies sudados o queso. Los síntomas iniciales de los altos niveles del ácido isovalérico en la sangre incluyen carencia de apetito, vómito y cansancio. Si los niveles de ácido isovalérico permanecen elevados, los síntomas pueden progresar a convulsiones, coma y aun en la muerte. 1 en 250 000 nacimientos Se encuentra localizado en el cromosoma 15q15.1 y contiene 12 exones y afecta al gen La esperanza de vida de personas que padecen acidemia isovalérica puede llegar a ser normal dependiendo de un diagnóstico y tratamiento temprano Los tratamientos se basan principalmente en la dieta, una medicación específica y el tratamiento de crisis metabólicas en caso de que el paciente lo presente. Los tratamientos son individualizados, en función de cada paciente, su tolerancia, respuesta a los cofactores, estado nutricional y las descompensaciones. TMP ENFERMEDAD DE TAY-SACHS AR Infantil: Forma clásica más común y grave. Los síntomas aparecen en los primeros meses de vida. Juvenil: Varios grados de gravedad. Síntomas entre los 2 y 5 años. Adultez: La forma menos grave, con síntomas que aparecen en la infancia tardía hasta la edad adulta #272800 En 1881 W. Tay describió las alteraciones oculares. Posteriormente B. Sachs en 1898 define el cuadro clínico: "Enfermedad heredodegenerativa de la infancia y que se caracteriza por una triada sintomática: detención de todos los procesos mentales; debilidad progresiva de todos los músculos del cuerpo, terminando en parálisis y ceguera rápidamente progresiva asociada a cambios en la mácula, la mancha rojo cereza y a atrofia óptica" Juventud: Los síntomas y la gravedad varían mucho. El deterioro neurológico es lentamente progresivo y puede causar torpeza y pérdida de coordinación, debilidad muscular, temblores, dificultad para hablar o tragar, y espasmos y movimientos musculares incontrolables. Adultez: Los síntomas y la gravedad varían mucho. El deterioro neurológico es lentamente progresivo y puede causar torpeza y pérdida de coordinación, debilidad muscular, temblores, dificultad para hablar o tragar, y espasmos y movimientos musculares incontrolables. Hay una especial incidencia en la población judía donde su frecuencia es de 12 x 100.000 nacimientos, comparada con 0,2 x 100.000 nacimientos en los no judios El gen HEXA se encuentra en el cromosoma 15q23 Pueden fallecer en la infancia tardía, en torno de 2 a 4 años después de su diagnóstico, y en otros casos pueden llegar hasta los 20 años de vida El proveedor de atención médica examinará al bebé y preguntará acerca de los antecedentes familiares. Los exámenes que se pueden hacer son: examen de enzimas en la sangre o tejido corporal para verificar los niveles de hexosaminidasa y examen ocular (revela un punto color rojo cereza en la mácula). No existe tratamiento para esta enfermedad en sí, solo formas para hacer la vida de la persona más cómoda. AMC DEFICIENCIA DE G6PD DLZ No las presenta. #300908 Hipótesis. Cáncer- frecuencia de la deficiencia G6PD. Stamatoyannopoulos y colaboradores en 1966: Viciafaba: induce a la hemolisis.Beutler (1970) sugirió que la DOPA- quinona Fiebre, orina oscura, dolor abdominal y de espalda, fatiga, palidez cutánea. ictericia neonatal, nauseas, vómitos, vértigo, hepatomegalia leve y hemoglobinuria. Menos de 400 millones, el 7% de la población mundial Cromosoma XQ28 y afecta a los genes G6PD Los afectados mantienen una vida normal. Se inicia un tratamiento con ácido fólico y Seguimiento en consultas. Transfusión sanguínea. En adultos la esplenectomía y terapia intravenosa con cefotaxima. TMP ENFERMEDAD DE POMPE AR Temprana o clásica Se manifiesta de forma grave en los primeros meses de vida con un cuadro progresivo y mortal alrededor de los dos años de edad. #232300 Enfermedad descrita en 1932 por el patólogo holandés Joannes Cassianus Pompe Describió el caso de una niña de siete meses con hipertrofia miocárdica idiopática y debilidad muscular Después en 1963 Hers, H. G. describió, por medio de microscopia electrónica, que el glucógeno se acumulaba en los lisosomas Debilidad muscular. Tono muscular pobre. Hígado agrandado. Insuficiencia en ganar peso y de crecimiento al ritmo esperado (insuficiencia de crecimiento) Problemas para respirar. Problemas de alimentación. Infecciones en el sistema respiratorio. Problemas de oído. 1 de cada 40.000 nacimientos vivos mundialmente. El gen de la alfa- glucosidasa se encuentra en el cromosoma 17 (17q25.2-q25.3) La esperanza varía desde normal con debilidad muscular generalizada a progresión lenta que acaba produciendo la muerte en los primeros meses de vida o antes de la tercera década de vida por insuficiencia cardiaca o respiratoria Tratamiento de α-glucosidasa ácida humana obtenida mediante ADN recombinante a partir de células CHO. Este tratamiento se utilizó por primera vez en el año 2000, consiguiendo mejoría clínica en todos los pacientes tratados. Posteriormente en 2006 se aprobó para su uso en etapa tardía. TMP GANGLIOSIDOSIS GMI AR GM1-GANGLIOSIDOSIS TIPO I - Forma infantil GM1-GANGLIOSIDOSIS TIPO II - Forma infantil/juvenil GM1-GANGLIOSIDOSIS TIPO III - Forma adulta/crónica #230500 1951 Dr. John Patrick Caffeyfue el priemero en describir la enfermedad, en 1964 Landing reconoció los tipos de gangliosidosis y en 1969 O'Brien identifico la deficiencia de la enzima beta galactosidasa Degeneración cerebral, acumulación de gangliósido en neuronas, hepático, esplénico y otros histiocitos, y en epitelio glomerular renal, deterioro psicomotor a partir de los 6 meses, afectación generalizada del sistema nervioso central, hepatosplenomegalia, dimorfismo facial, manchas rojas de cereza macular, displasia esquelética y muerte temprana. 1 de cada 100.000 a 200.0000 nacidos vivos Cromosoma Afectado 3p22.3 (GLB1; 611458) Oscila entre los 3 y los 30 años El tratamiento incliye segun la gravedad del cuadroclinico; trasnplante de medula osea (BMT), terapia genica y terapia de reduccion de sustrato. AMC ACIDEMIA METILMALONICA AR Deficiencia de metilmalonil – CoA epimerasa Solamente se han descrito 6 casos de personas afectadas. Los síntomas incluyen dificultad para coordinar los movimientos y para hablar, hipotonía, parálisis parcial de las piernas, rigidez leve y convulsiones. #251000 El MMA fue caracterizado por primera vez por Oberholzer VG junto a Levin B, y Burgess, en 1970 . Enfermedad cerebral que empeora (encefalopatía progresiva), deshidratación, retrasos en el crecimiento, desarrollo retardado , letargo , infecciones recurrentes por levaduras, convulsiones y vómitos principalmente. Aproximadamente 1 de cada 25.000 a 48.000 bebés nacen con esta afección Afecta al cromosoma 6p12.3 en el GEN MMUT La enfermedad generalmente se diagnostica en el primer año de vida y un gran porcentaje de los portadores no sobrepasan los 2 años, casos extraordinarios se reportan de adultos bajo estricto control alimentario. El diagnostico requiere correlacion clínica, destacan las pruebas de amoníaco, gasometría arterial, conteo sanguíneo completo, tc o irm del cerebro, niveles de electrolitos y pruebas genéticas. El tratamiento corresponde a carnitina a dosis de 300 mg/día y vitamina b12 (1mg/día) en los casos que responden a ella. AMP SÍNDROME DE SMITH- LEMLI-OPITZ AR Se reportan 150 mutaciones, cinco de las cuales (IVS8-1G>C, T93M, W151X, V326L y R404C) representan alrededor del 60 % de los alelos mutados. #270400 Esta enfermedad hereditaria y congénita, fue descrita por primera vez en 1964 por David Smith, Luc Lemli y John Opitz Los pacientes presentan retraso en el crecimiento y discapacidad intelectual. Los problemas del comportamiento incluyen: rasgos autistas, hiperactividad, conductas de autolesión y alteraciones del sueño. Las anomalías estructurales del cerebro pueden incluir hipoplasia o ausencia del cuerpo calloso y holoprosencefalia. Las manifestaciones craneofaciales típicas son: microcefalia (80% de los casos), estrechamiento bitemporal, ptosis, puente nasal ancho, raíz nasal corta, anteversión de las fosas nasales (90% de los casos), barbilla pequeña y micrognatia. El pronóstico depende de la gravedad de la enfermedad y de las malformaciones asociadas. La enfermedad cardíaca y las malformaciones en el cerebro pueden ser letales. Algunos individuos viven hasta la edad adulta. Las mutaciones ocurren en el gen DHCR7 (11q13.4). Pueden llegar a tener una vida adulta. Diagnóstico bioquímico detección de 7DHC en plasma y tejidos con cromatografía de gases o espectrometría de masas. El tratamiento incluye una suplementación de colesterol y simvastatina. Otros posibles métodos: Administración directa de colesterol al cerebro.Antioxidantes. Esteroles sintéticos que atraviesen la barrera hematoencefálica. Suplementación prenatal de colesterol. Transplante al cerebro de células madres neurales.Terapia génica. TMP
