Tema 9a alcoholes
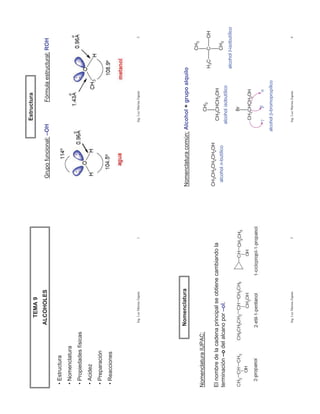
- 1. Estructura TEMA 9 ALCOHOLES Grupo funcional: –OH Fórmula estructural: ROH • Estructura • Nomenclatura • Propiedades físicas • Acidez • Preparación • Reacciones Ing. Luz Marina Zapata 1 Ing. Luz Marina Zapata 2 Nomenclatura Nomenclatura común: Alcohol + grupo alquilo CH3 Nomenclatura IUPAC: CH3 H3C C OH CH3CH2CH2CH2OH El nombre de la cadena principal se obtiene cambiando la CH3CHCH2OH terminación –o del alcano por –ol. alcohol n-butílico CH3 alcohol isobutílico alcohol t-isobutílico Br CH3CHCH2OH alcohol -bromopropílico Ing. Luz Marina Zapata 3 Ing. Luz Marina Zapata 4
- 2. Clasificación de los alcoholes Propiedades físicas • Alcoholes de PM más bajo líquidos y con olor característicos • p.e. alto (alcano PM similar) enlaces polares enlace hidrógeno ramificaciones • Alcoholes pequeños elevadas constantes dieléctricas • Metanol y etanol buenos stes. comp. iónicos • Alcoholes inferiores completamente solubles en agua • Alcoholes polihidroxilados > nº OH-, > p.e. Ing. Luz Marina Zapata 5 Ing. Luz Marina Zapata 6 Acidez • Grado de sustitución Los alcoholes son ácidos Mayor acidez Ing. Luz Marina Zapata 7 Ing. Luz Marina Zapata 8
- 3. • Sustitución de átomos de H por átomos de X Fuente industrial Hidratación craking RHC CH2 de alquenos RCHCH3 Petróleo OH Proceso Ej. Propeno + H+ + H2O oxo • Formación de alcóxidos metálicos RCH2CH2OH Ej. Etileno + CO + H2 + (CO)8Co2 CH3 Fermentación Na OCH3 Na OCH2CH3 K O C CH3 con levaduras CH3 Caña de Melasas Los alcoholes son bases azúcar CH3CH2OH Granos Almidón Ing. Luz Marina Zapata 9 Ing. Luz Marina Zapata 10 Preparación 2) Hidroboración - Oxidación 1) Oximercuración - Desmercuración 1) (BH3)2 R C C + B(OH)3 C C 2) H2O2 - OH 1) Hg(OAc)2 - H2O R H OH C C R C C 2) NaBH4 Ej. propeno R OH H - Alcoholes primarios Ej. 2-metilpropeno - Orientación: Anti - Markovnikov - Orientación: Markovnikov - Sin reordenamiento - Sin reordenamiento Ing. Luz Marina Zapata 11 Ing. Luz Marina Zapata 12
- 4. 5) Reducción de compuestos carbonílicos 3) Hidrólisis de halogenuros de alquilo O OH R X + OH R OH + X 1) NaBH4, etanol C C Ej. Tolueno + Cl2 + NaOH H 2) H3O Ej. Butanal Ácido 9-octadecenoico (ácido oleico) 4) Condensación aldólica Diciclohexilcetona 2-pentenoato de metilo Condensación de aldehídos y cetonas: reacción aldólica 6) Síntesis de Grignard O OH O O OH NaOH 2 C C C Estas reacciones H3C H CH3CH2OH H3C C H 1) MgX :R, etanol H las desarrollaremos C C + OHMgX H H R en el Tema 12 2) H2O Acetaldehído Aldol (aldehído + alcohol) (un -hidroxialdehído) Ej Formaldehído Óxido de etileno Ing. Luz Marina Zapata 13 Acetaldehído Propanoato de metilo 14 Acetona 7) Hidroxilación de alquenos Reacciones • Ruptura del enlace C–OH Ej. 1) Etileno + Ej. Ciclohexeno + C C Ácido peroxibenzoico KMnO4 + NaOH + H2O n HX RX + H2O 2) H3O+ - H2O c. co Rea HX Ej. 1- propanol + BrH 1) RCOOOH ol-t-butílico + HCl KMnO4 2) H2O - H Reac. con PX3 PX3 3 RX + H3PO3 OH ROH Ej. Etanol + P + I2 Desh C C C C idrat H:B ación OH OH OH C C + H2O Ing. Luz Marina Zapata 15 16 Ej. 3,3-dimetil-2-butanol + H:B
- 5. • Ruptura del enlace RO–H Reac. como ácido: con metales activos M ROM + 1/2 H2 Ej. Etanol + Na Formación de ésteres R´COOH H RCOOR´ + H2O Ej. Etanol + AcH Oxidación O K2Cr2O3 ROH R C H Ej. Alcohol 1º + Cr (VI) KMn + KMnO4 O4 O Alcohol 2º + Cr (VI) R C OH Ing. Luz Marina Zapata 17
