Sandrogreco Gases
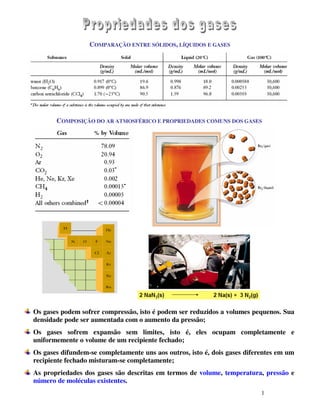
- 1. COMPARAÇÃO ENTRE SÓLIDOS, LÍQUIDOS E GASES COMPOSIÇÃO DO AR ATMOSFÉRICO E PROPRIEDADES COMUNS DOS GASES Os gases podem sofrer compressão, isto é podem ser reduzidos a volumes pequenos. Sua densidade pode ser aumentada com o aumento da pressão; Os gases sofrem expansão sem limites, isto é, eles ocupam completamente e uniformemente o volume de um recipiente fechado; Os gases difundem-se completamente uns aos outros, isto é, dois gases diferentes em um recipiente fechado misturam-se completamente; As propriedades dos gases são descritas em termos de volume, temperatura, pressão e número de moléculas existentes. 1
- 2. PRESSÃO (FORÇA POR UNIDADE DE ÁREA) F P= A EFEITO GREENHOUSE 2
- 3. LEI DE BOYLE – RELAÇÃO VOLUME-PRESSÃO 3
- 4. LEI DE CHARLES – RELAÇÃO VOLUME-TEMPERATURA 4
- 5. PRINCÍPIO DE AVOGRADO – VOLUME MOLAR PADRÃO – GAY LUSSAC Para amostra de dois gases GAY-LUSSAC Os volumes dos gases que reagementre siestão na proporção dos menores números inteiros possíveis Volume molar padrão Desvios no valor do volume molar padrão indicam que o gás não se comporta como um gás ideal O volume molar padrão de um gás ideal é de 22,4 L / mol no sistema padrão de temperatura e pressão 5
- 6. LEI DOS GASES IDEAIS P V1 P2V2 1 = n1T1 n2T2 Lei dos gases combinados APLICAÇÕES ADICIONAIS DA LEI DOS GASES 6
- 7. A LEI DAS PRESSÕES PARCIAIS DE DALTON EQUAÇÃO DOS GASES E A FRAÇÃO MOLAR 7
- 8. COLETANDO OS GASES SOBRE A ÁGUA TEORIA CINÉTICA MOLECULAR DOS GASES Teoria de moléculas em movimento RELAÇÃO TEMPERATURA - ENERGIA CINÉTICA Os gases consistem de um grande número de moléculas em movimento contínuo e aleatório; O volume de todas as moléculas do gás é desprezível, se comparado ao volume total no qual o gás está contido; As forças atrativas e repulsivas entre as moléculas de gás são desprezíveis; A energia pode ser transferida entre as moléculas durante as colisões. A energia cinética média não varia a temperatura constante; A energia cinética média é proporcional à temperatura aboluta. 8
- 9. TEORIA CINÉTICA MOLECULAR, A EQUAÇÃO DOS GASES E A VELOCIDADE MOLECULAR P ∝ impulso da colisão x velocidade da colisão impulso da colisão ∝ m u m = massa e u = velocidade velocidade da colisão ∝ velocidade molecular x moléculas por unidade de volume velocidade molecular ∝ u x N/V P ∝ (m.u) x u x N/V ou P ∝ Nmu2/V ou PV ∝ Nmu2 velocidade quadrática média correção da trajetória de colisão N ou NAv = n. NAv Lei dos gases ideais Substituindo PV, temos ou EC ∝ temperatura logo Velocidade quadrática molecular média M= massa molecular 9
- 10. DISTRIBUIÇÃO DE VELOCIDADES DE MAXWELL Quanto maior for a massa molar, menor a velocidade média e mais estreito o intervalo de velocidade. TEORIA CINÉTICA MOLECULAR E A LEI DOS GASES LEI DE BOYLE 10
- 11. LEI DE CHARLES LEI DE DALTON MOVIMENTO DAS MOLÉCULAS DOS GASES – EFUSÃO E DIFUSÃO DIFUSÃO – dispersão gradual de uma substância em outra Expansão dos odores e feromônios 11
- 12. EFUSÃO Fuga de um gás para o vácuo através de um orifício pequeno O gás escapa porque existem mais colisões no lado de alta pressão LEI DA EFUSÃO DE GRAHAM Velocidade de efusão ∝ 1/√M √ Velocidade de efusão ∝ √3RT/M 3RT r1 u1 M1 M2 r = taxa de efusão; = = = u = vel. média quadrática r2 u2 3RT M1 M 2 Velocidade de efusão A / velocidade de efusão B = √MB/MA Velocidade de efusão ∝ velocidade média das moléculas no gás Velocidade média das moléculas A / velocidade média das moléculas B = √MB/MA Velocidade de efusão aumenta com a raiz quadrada da temperatura Velocidade de efusão em T2 / velocidade de efusão em T1 = √ T2/ T1 Velocidade média das moléculas T2 / velocidade média das moléculas T1 = √ T2/ T1 VELOCIDADE MÉDIA DAS MOLÉCULAS EM UM GÁS ∝ √ T/M 12
- 13. GASES REAIS: DESVIO DA IDEALIDADE O volume de todas as moléculas do gás é desprezível, se comparado ao volume total no qual o gás está contido; As forças atrativas e repulsivas entre as moléculas de gás são desprezíveis. JOHANNES VAN VER WAALS Desvio da idealidade deve-se a existência das forças intermoleculares (atrações e repulsões intermoleculares) O comportamento não-ideal dos gases ocorrem normalmente a altas pressões e/ou a baixas temperaturas FATORES DE CORREÇÃO FATOR DE COMPRESSÃO (Z) Z = VOLUME MOLAR DO GAS REAL (VM) / VOLUME MOLAR DO GAS IDEAL (VMIDEAL) 13
- 14. EQUAÇÃO DE VAN DER WAALS nRT n2a P= − V − nb V 2 CORREÇÃO PARA O VOLUME DAS MOLÉCULAS CORREÇÃO PARA A ATRAÇÃO MOLECULAR 14
