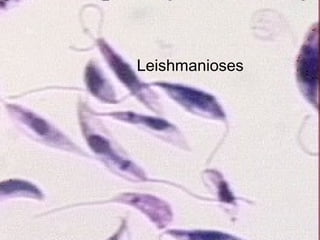
Leishmanioses: Doenças causadas por protozoários do gênero Leishmania
- 2. Leishmania sp. Classificação : Filo Sarcomastigophora Sub-filo Mastigophora Ordem Kinetoplastida Família Trypanosomatidae Gênero Leishmania Características gerais Protozoário flagelado Dois hospedeiros obrigatórios (igual ao T. cruzi /brucei ), heteroxénico Habitat: - Vetor: lúmen do trato digestivo (Subgenus Leishmania: intestino anterior/médio) (Subgenus Viannia: intestino anterior/médio/posterior) - Hospedeiro vertebrado : células do sistema mononuclear fagocitário (SMF), principalmente macrófagos
- 3. Leishmaniose: Aspectos históricos e sociais • Doença benigna ou mortal, na forma cutânea deixa cicatrizes grandes (“botão do oriente”), doença conhecida na America do Sul antes da chegada dos espanhóis • Agente etiológico descrito primeiramente por Borovsky em 1898 em um paciente no Usbequistão • Leishman e Donovan (1903) descreveram o parasita independentemente em um caso de calazar da Índia • Ross (quem descreveu o cíclo de vida do plasmódio) batizou o parasita em 1903 Leishmania donovani, e Wright denominou um parasita vindo de uma criança da Armênia (forma cutânea) Leishmania tropica
- 4. • Em 1909, Lindenberg, Paranhos & Carini demonstraram a presença dos parasitos em lesões de pacientes brasileiros, Gaspar Vianna denominouos Leishmania braziliensis e detectou em 1912 a ação curativa do tártaro emético • Em 1987, Lainson e Shaw sugerem um novo subgênero de Leishmania: o subgênero Viannia, que inclui espécies das Americas
- 5. •Polimórfico: Promastigota Paramastigota Inseto Promastigota metacíclico Amastigota • Reprodução por divisão binária Macrófago com amastigotas Hospedeiro mamífero
- 6. • Organização celular - Genoma com 36 chromossomos (L. major, Projeto genoma completo), 8305 genes identificados (4/2005) - K(C)inetoplasto, trans-splicing
- 8. Formas promastigotas metacíclicas regurgitadas por mosquitos são depositadas na dermis, onde são fagocitados por macrófagos • Vetores (Diptera, Phlebotomidae: Lutzomiya, Phlebotomus), no território brasileiro: Lutzomiya longipalpis, L. wellcomei e outros
- 9. Promastigotas dentro do fagolisossomo se transformam em amastigotas, que se multiplicam no macrófago. A célula hospedeira é rompida liberando amastigotas que são fagocitados por outros macrófagos MΦ
- 10. Macrófagos infectados com Leishmanias do subgênero Viannia (espécies das Américas) contém menos parasitas em vários vacúolos parasitóforos (ajuda no diagnóstico por microscopia) MΦ Subgênero Leishmania MΦ Subgênero Viannia
- 11. Macrófagos infectados são ingeridos por Lutzomiya MΦ
- 12. Após ingestão, amastigotas se transformam em promastigotas e se multiplicam dentro de uma membrana formada pelo vetor Trato digestivo Membrana peritrófica
- 13. Promastigotas se desenvolvem para paramastigotas que aderem em pontos diferentes no trato digestivo (critério da localização: subgenênero de Leishmania), a proliferação é estimulada se a fêmea ingere sucos vegetais
- 14. Após 3-5 dias, promastigotas metacíclicos migram ativamente para partes anteriores do tubo digestivo Assim, o parasita parece interferir ativamente com a capacidade de ingestão do hospedeiro mosquito! A saliva do flebotomíneo é muito importante para a infecciosidade da Leishmania Somente promastigotas metacíclicos são infecciosos para os hospedeiro vertebrado!
- 15. Patogenia e interação parasita-hospedeiro Após deposição de promastigotas na pele complemento liga à superfície do parasita mas a clivagem de C3b em iC3b não permite ligação do complexo lítico C3b iC3b
- 16. Proteína gp63 cliva o fator do complemento C3b para iC3b. Complemento ajuda na aderência das promastigotas nos macrófagos (receptor principal CR3). Interação de LPGs e gp63 com fibronectina também ocorre. Esta via de internalização não leva a produção radicais de oxigênio ou NO (“silent entry”) Receptor de complemento R3 c1) C a (M iC3b CR1 MΦ
- 17. Porque uma célula profissional do sistema fagocitário não consegue eliminar um parasita dentro do fagossomo? 1. A sinalização para ativação do macrófago está impedido por ação de LPG: Tradução de sinais, mobilização de cálcio, ativação de Proteina kinase C. MΦ
- 18. 2. Indução de resposta disfuncional: inibição da produção de radicais de OH e NO Falha na apresentação em MHC2 após estimulação com IFN γ Fosfoglicanos bloqueiam produção de IL-12 IFN γ ? MΦ
- 19. 3. Proteina tirosina quinases também são bloqueados Secreção de EF1α da Leishmania para o citossol Ativação de SHP-1 (uma Phosphotirosina fosfatase) Inativação da Fosfotirosinaquinase: reação atenuada a IFN γ MΦ
- 20. A espécie infectante é importante para o fenótipo da patologia desenvolvida em indivíduos imunocompetentes (Leishmanias que ocorrem no Brasil) A expressão diferencial ou presença/ausência de genes provavelmente causa as diferenças nas patologias observadas
- 21. Os diferentes tipos de Leishmaniose na clínica • Visceral ou Calazar ( L. donovani, L. infantum , no Brasil causada por L. chagasi ): - Enfermidade crônica - Caracterizada por: • febre irregular e de longa duração • hepatoesplenomegalia • linfoadenopatia • Anemia com leucopenia • Hipergamaglobulinemia • Emagrecimento • Edema • Caquexia e morte se não for tratado, dentro de 2 anos
- 22. - Formas clínicas calazar: assintomática, oligossintomática, aguda e crônica
- 23. •Tegumentaria: a) Cutânea: - Infecção confinada na derme, com epidermis ulcerada - Velho mundo, L. tropica, L. major e L. aethiopica - Novo mundo, leishmanias do complexo mexicana e braziliensis - no Brasil: L. braziliensis, L. guyanensis L. chagasi, L. lainsoni
- 24. Leishmaniose cutânea (“oriental sore” “botão do oriente”, “Úlcera de Bauru”
- 25. b) Muco-cutânea: - Infecção na derme (ulceras), invasão de mucosa e destruição da cartilagem - No novo mundo: L. braziliensis, L. guyanensis, L. mexicana (“espundia”), no Sudão/Etiópia L. major, L. tropica
- 28. c) Cutânea difusa: - Infecção confinada na derme, formando nódulos não ulcerados. Disseminação por todo o corpo - Associado a deficiência imunológica do paciente - Novo mundo, L. pifanoi, L. amazonensis - Velho mundo, L. aethiopica
- 29. Responsável pela patologia é o estado imunológico do hospedeiro predominância de resposta celular (Th1) leva a imunidade e cura, resposta humoral (Th2) leva às formas crônicas IFNγ, TNFα, IL-2 Th1 I MHC MΦ II Células T helper Th2 IL 4-6, IL-10, TGFβ indução da atividade policlonal de células B
- 30. No modelo L. major e camundongo Br Med Bull. 2006 Jul 17;75-76:115-30
- 31. Quais são os motivos patologia da infecção? para tanta diversidade da - Na forma cutânea, há uma inflamação ativa. Células dentríticas apresentam antígenos em MHC2 e expressam ICAM-1. Ativação de Th1 por IFNγ e TNFβ resulta no recrutamento de células T CD8+ para a região infectada. Cura. - Na forma mucocutânea, pouco envolvimento ou destruição de células Langerhans, mas há apresentação em MHC2 e células com ICAM1, mas TH1 e Th2 estão ativados. IL10 promove o decréscimo da apresentação de antígenos e de produção de IFNγ. Pode ter hiperprodução de IL1, TNFα e ICAM1, resultado é um estado pró-inflamatório e destruição sucessiva de tecido.
- 32. - Na forma visceral , não há resposta Th1 e nem aumento de atividade Th2. Fatores parecem ser do próprio macrófago infectado. Possivelmente, lipofosfoglicanos da Leishmania estão envolvidos.
- 33. Diagnóstico: As Leishmanias são vistas nas formas amastigotas
- 34. Diagnóstico Leishmaniose Tegumentaria • Clínico Caraterísticas da lesão e dados epidemiológicos • Laboratorial - Exame direto de esfregaços corados (Romanowsky, Giemsa ou Leishman) - Exame histológico - Cultura - Inóculo em animais - PCR (reação em cadeia da polimerase, permite a identificação da espécie infectante) • Importante para exclusão de tuberculose cutânea, hanseníase, infecções por fungos, úlcera tropical, neoplasmas
- 35. Diagnóstico Leishmaniose Tegumentaria • Imunológicos - Teste de Montenegro (teste da resposta contra formas promastigostas mortas do parasita, resposta celular) - Reação de imunofluorescência indireta (RIFI) (resposta humoral) - Hemaglutinação indireta
- 36. Diagnóstico Leishmaniose visceral ( Calazar) • Clínico: sintomas baixa recorrente, envolvimento linfohepático, - Febre esplenomegalia, caquexia e dados epidemiológicos • Laboratorial: 1. Exames Parasitológicos a) Demonstração direta do parasita Esfregaços corados com Giemsa ou Leishman de: - Material obtido por punção de medula óssea, fígado ou baço - Biopsia (menos eficiente ~ 50%)
- 37. - Fase aguda 80-90% de positividade - Fase sub-clínica 10% - Co-infectados com HIV recomendado exame de medula óssea - Aspirado esplênico 100 %, sangue periférica 30% b) Isolamento em cultivo in vitro Aspirado ou biopsia LIT, MEM, Schneider’s e Evans (Meio monofásico) a 26ºC Exame microscópico ( 2x semana/4 semanas)
- 38. c ) Isolamento em cultivo in vivo • Inoculação em animais - Hamsters ou camundongos isogênicos (BALB/c) - Cepas dermatotrópicas: pata ou tocinho dos animais (positivo após 2 a 4 semanas) - Cepas vicerotrópicas via intraperitoneal (positivo após 6 meses) - Recomendado para o isolamento do parasita nas formas subclínicas • Xenodiagnóstico - Flebótomos - Usado em pacientes com AIDS portadores de Leishmaniose visceral
- 39. 2. Testes Imunológicos a) Teste de Montenegro b) Testes serológicos •Antígenos (parasitas inteiros, inativados) - Reação de aglutinação direta Cave: Reatividade cruzada com Chagas e tuberculose Visualiza títulos até de 1:51.200 Leishmaniose visceral título > 1:1.600 (sensibilidade 100%) no Brasil o título > 1:6.400 c) Detecção do antigeno rK39 na urina
- 40. 3. Análise do DNA de material recolhido a) Por reação em cadeia da polimerase (PCR) Usa oligonucleotídeos espécie-específicos do DNA dos minicírculos do DNA do cinetoplasto 100% sensível e mais específico que sorologia b) Possibilita discriminação de espécies
- 41. Tratamento Leishmaniose Tegumentaria 1. Quimioterapia • Antimoniais Tártaro emético antimonial trivalente Glucantime (antimoniato de N-metil-glucamina) antimonial pentavalente Pentostan (estibogluconato de sodio) - antimonial pentavalente - inibe glicolise e síntese - administração intramuscular ou intravenosa absorção rápida
- 42. - Excreção rápida e pela urina, vida media 24 horas - Droga recomendada para os três tipos de leishmaniose Glucose Glucose 6-phosphate Fructose 6-phosphate Pentose Phosphate Pathway Fructose 1,6-bisphosphate Dihydroxyacetone Glyceraldehyde 3-phosphate Phosphate 1,3-Diphosphoglycerate 3-Phosphoglycerate 2- Phosphoglycerate Phophoenolpyruvate * PK Pyruvate Acetyl- CoA Krebs Cycle Antimoniais
- 43. • Pentamidina - liga ao DNA, inibindo a replicação - Inibe a dihidrofolate reductase, interfere com o metabolismo de poliaminas - Administração intramuscular - Excretado lentamente, é seqüestrado nos tecidos (tem uso profilático contra tripanossomiase) - Produz hipo- ou hiperglicemia
- 44. •Anfotericina B - lipofílico - Liga a esterois (ergosterol) da membrana formando poros. Funciona como um ionóforo - 2-5% excretado na urina - 90% ligado a proteínas do plasma - Meia vida 18 horas
- 45. Continuação tratamento Leishmaniose Tegumentaria 2. Imunoterapia Leishvacin® seriado Leishvacin® associado ao BCG Leishvacin® seriado associado ao BCG Leishvacin® associado ao BCG com Glucantime ® Interferon gamma humano recombinante (Rhifn-γ) anti-IL10-receptor
- 46. Tratamento Leishmaniose visceral 1. Quimioterapia • Antimoniais Tártaro emético Glucantime • Pentamidina • Anfotericina B • Miltefosin 2. Imunoterapia Interferon gamma recombinante (Rhifn-γ)
- 47. Br Med Bull. 2006 Jul 17;75-76:115-30
- 48. Medidas de prevenção • Identificação de focos de Leishmania (animais infectados em proximidade a domicílios: silvestres e domésticos: erradicação • Imunização em massa de cachorros (Leishvaccin) • Vacinas para seres humanos? • Componentes da saliva de Phlebotomíneos como vacina?
- 49. Ecologia dos Phlebotomíneos: Desenvolvimento e comportamento • 40-70 ovos por desova, agrupados em lugares humidos, eclodem depois 6-17 dias • Larvas se nutrem de matéria orgânica por mais 15-70 dias, depois pupa (7-14 dias) • Adultos são ativos no crepúsculo ou a noite, durante o dia permanecem em lugares tranquilos: tocas, arvores ocas, currais, moradias • Não sobrevivem bem em ambientes que não tenham pelo menos um mes T acima de 20°C
- 52. Medidas de prevenção • Uso de repelentes, telas de proteção • Borrifação frequente de ambientes • Tratamento de sintomáticos e assintomáticos em regiões com alta incidência de flebotomíneos • Tratamento/exterminação de animais domesticos infectados
- 53. Dentistas: Atenção na hora do tratamento de pacientes em área endêmica: eventuais lesões na boca
- 54. Med. oral patol. oral cir.bucal (Internet) v.12 n.4 Madrid ago. 2007
- 55. Literatura: L. Rey: Parasitologia Markell´s & Voge´s Medical Parasitology Links interessantes: http://www.hhmi.ucla.edu/parasite_course/Default.htm http://www.genedb.org/genedb/leish/index.jsp http://www.leishmaniasis.info/ Uma revisão muito interessante: Br Med Bull. 2006 Jul 17;75-76:115-30
- 56. 1. Cita uma espécie de cada Leishmania causadora para leishmaniose cutânea, mucocutânea e visceral, que ocorre no Brasil. 2. Associe as formas amastigota, paramastigota e promastigota metacíclico de Leishmania aos seus habitats (célula/tecido) de ocorrência. 3. No humano, em qual tipo de célula ocorre a proliferação de Leishmania? 4. Explique as diferenças morfológicas entre o processos da infecção do humano por Anopheles/Plasmodium e Flebotomíneo/Leishmania 5. O que é necessário para se infectar acidentalmente no tratamento odontológico de um portador de Leishmania braziliensis com lesão nos lábios?
