Datos jane mono
- 1. AGUA COMO PASAJE DIRECTO AL BAÑO Se sabe comunmente que al comer algún alimentos y te produzca diarrea es, probablemente, que estaba malogrado. No obstante, muchas personas ignoran que el tomar agua inadecuadamente procesada también puede desencadenar las mismas consecuencias, ya que alberga a parasitos como la Giardia Lamblia
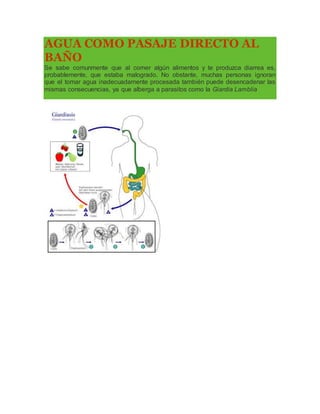
- 2. Giardiasis. Luis Felipe Higuita Gutiérrez Docente Escuela de Microbiología Universidad de Antioquia La giardiasis es la infección producida por Giardia intestinalis, protozoo flagelado que parasita el intestino delgado humano. Se encuentra ampliamente diseminada en el mundo, es una de las causas más frecuentes de diarrea no viral y entre los
- 3. parásitos intestinales es el que más frecuentemente se encuentra como agente causal de enfermedad diarreica aguda (EDA) en niños. Ciclo de vida Giardia intestinalis presenta un ciclo de vida con dos formas parasitarias, trofozoítos y quistes. Los trofozoítos se localizan en el intestino delgado, fijados a la mucosa. Allí se multiplican por división binaria y los que caen a la luz intestinal dan origen a quistes. Estos son eliminados con las materias fecales y pueden permanecer viables en el medio ambiente por varios meses contaminando agua o alimentos. La infección se da por el consumo de agua o alimentos contaminados con quistes del protozoo, que una vez ingeridos se rompen en el intestino delgado para dar origen a 4 trofozoítos por cada quiste, allí se localizan en duodeno y yeyuno lesionando la mucosa. La infección es principalmente persona a persona, pero algunos animales como perros, gatos y castores pueden ser reservorios. Período de incubación De 3 a 25 días o más, con una mediana de 7 a 10 días Período de transmisibilidad
- 4. Todo el período que dura la infección, que suele ser de meses Susceptibilidad Los niños son altamente susceptibles a la infección. En los adultos, la infección suele seguir un curso limitado, autorremitente. En individuos inmunocomprometidos suele ser más grave y duradera. Manifestacions clínicas Las infecciones por Giardia intestinalis pueden ser asintomáticas, causar cuadros clínicos agudos o crónicos Las infecciones asintomáticas son más frecuentes en adultos que en niños. En zonas endémicas la presencia de sintomatología y la intensidad de los síntomas son menores que en visitantes de zonas no endémicas que padecen de giardiasis La infección aguda se presenta principalmente en niños y hasta los 15 años, así como en adultos que residen en zonas no endémicas en los cuales es considerado un agente causal de la diarrea del viajero. El síndrome diarreico se caracteriza por deposiciones acuosas, abundantes, espumosas, fétidas con esteatorrea, heces lientéricas; se acompaña de náuseas, distención abdominal y flatulencias. En los casos crónicos, la diarrea persiste por mayor tiempo y presenta dolor abdominal, náuseas, vómito, flatulencia, pérdida de peso y deficiencias nutricionales en niños. Puede generar malabsorción de grasas, pérdida de proteínas, desnutrición y anemia. Diagnóstico de laboratorio El diagnóstico se establece mediante la observación de los trofozoítos o quistes a través del coprológico directo o por concentración. El examen macroscópico se caracteriza por heces acuosas, espumosas, fétidas, con esteatorrea y lientéricas. Sin moco ni pintas de sangre Examen microscópico Trofozoítos
- 5. El trofozoíto mide de 14 a 16 μm de longitud por 6 a 8 μm de ancho, tiene forma de pera, presenta 2 núcleos con nucléolos centrales, 4 pares de flagelos, uno anterior, dos laterales y uno posterior. Posee en la parte central una barra doble denominada axostilo que es atravesado por dos estructuras en forma de coma denominadas cuerpos parabasales. El trofozoíto tiene capacidad de traslación con movimiento lento, vibratorio y rotatorio Trofozoíto de Giardia intestinalis Coloración tricrómica 40X Informe: Se observan trofozoítos de Giardia intestinalis Quistes El quiste mide de 10 a 12 μm, tiene forma ovalada con doble membrana, de 2 a 4 núcleos ubicados en un extremo y el axostilo característico.0 Quiste de Giardia intestinalis Muestra con lugol 100X Informe: Se observan quistes de Giardia intestinalis Ir a galería de imágenes Diagnóstico diferencial El diagnóstico diferencial debe hacerse con otros protozoos ciliados de localización intestinal (Ver) Métodos de control. 1. Eliminar las heces por medio de técnicas sanitarias
- 6. 2. Proteger las fuentes de agua contra la contaminación por heces del hombre o de los animales. En caso en que se sospeche de la potabilidad del agua, se prefiere hervir el agua al tratamiento con hipoclorito 3. La educación sobre higiene personal a las familias y particularmente a quienes trabajan en guarderías o jardines infantiles, en cuanto a la necesidad de lavarse las manos antes de comer, de manipular alimentos y después de defecar. Casos clínicos Factores asociados a la infección por Giardia en escolares Artículos recomendados Giardiasis: la parasitosis más frecuente a nivel mundial. Mecanismo de disfunción epitelial en la giardiasis Diagnóstico Giardia CDC Adaptado de: [Botero D, Restrepo M. 2003]; [Francisco JC, et al. 2008];[Chin J. 2001] Fotografías tomadas por: Verónica Tangarife C (Docente SSO 2011) Gráfico realizado por: Felipe Higuita Gutiérrez En este momento está usando el acceso para invitados (Entrar)
- 7. DEFINICIONES En relación con los vocablos ameba y amebiasis, y otros términos con ellos vinculados, existen algunas confusiones. Como consecuencia, en no pocas ocasiones escuchamos expresiones, e incluso leemos textos en que se hace un uso incorrecto de los mismos. Por este motivo, nos ha parecido útil iniciar esta incursión por los viejos y nuevos saberes relativos a las amebas y la amebiasis, y precisaremos a continuación los términos que abordamos. AMEBAS El vocablo ameba designa un grupo de protozoos de la superclase Rhizopoda, pertenecientes a los géneros Naegleria, Acanthamoeba, Balamuthia, Entamoeba, Endolimax y Iodoameba. A las especies incluidas en este grupo, coinciden los textos clásicos, les son comunes dos elementos morfológicos de su fase trófica: la presencia de un protoplasma desnudo y la formación de seudópodos lobulados como estructuras de locomoción. La cantidad de especies de amebas presentes en la naturaleza es numerosa y la relación que estas establecen con otros seres vivos es variada. Las hay de vida completamente libre y existen las que parasitan, de manera facultativa u obligada, órganos y tejidos de una amplia gama de especies de animales. Sin embargo, solo un número reducido de especies pertenecientes a los géneros Naegleria, Acanthamoeba, Balamuthia y Entamoeba son patógenas al hombre (cuadro 84.1).
- 8. Cuadro 84.1. Clasificación, según patogenicidad y parasitismo que realizan, de las amebas que infectan al hombre Las especies de los géneros Naegleria, Acanthamoeba y Balamuthia son denominadas de conjunto amebas de vida libre. Las amebas de los géneros Naegleria y Acanthamoeba, y muy posiblemente las del género Balamuthia, habitan libremente en aguas estancadas en el suelo y en materia orgánica en descomposición, donde tienen lugar las dos fases de sus respectivos ciclos evolutivos de vida (quiste y trofozoito). Las amebas patógenas de estos géneros solo parasitan excepcionalmente al hombre, lo cual puede ocurrir por el contacto de este con aguas contaminadas con sus trofozoitos. AMEBAS PARÁSITAS OBLIGADAS Además de las especies de amebas de vida libre, el hombre puede ser infectado por especies amebianas de los géneros Entamoeba (E. histolytica, E. dispar, E. coli, E. hartmanni, E. gingivalis, E. polecki), Endolimax (E. nana) y Iodoameba (I. butschlii). Estas, a diferencia de las primeras, son parásitos obligados del hombre y de otros animales, pues deben realizar en uno de ellos, casi siempre en el aparato digestivo, parte de su ciclo evolutivo de vida. De las amebas parásitas del aparato digestivo del hombre, E. histolytica es la única especie patógena. Cuando invade los tejidos del humano, el espectro de las manifestaciones clínicas a que da lugar es tan amplio como variadas son las localizaciones que alcanza. E. histolytica, según se detallará en los siguientes acápites de este capítulo, puede habitar en el lumen intestinal, invadir la pared de esta víscera e, incluso, realizar migraciones a tejidos y órganos lejanos. AMEBIASIS La infección del hombre por especies de los géneros Naegleria, Acanthamoeba y Balamuthia da lugar con relativa frecuencia a manifestaciones clínicas, generalmente cuadros de muy mal pronóstico. La infección del humano por E. histolytica, por el contrario, es asintomática en la mayoría de las ocasiones. Es decir, los datos hoy disponibles parecen indicar que la proporción de personas que enferman y la gravedad de sus lesiones son mayores entre los individuos que se infectan con amebas de vida libre.
- 9. Sin embargo, las cifras de prevalencia de infección por especies de los géneros Naegleria, Acanthamoeba y Balamuthia, sobre todo si se les compara con las estimadas para la infección por E. histolytica, son extremadamente bajas. En este argumento radica que se haya reservado el término amebiasis exclusivamente para la infección. Agente etiológico Se considera la amebiasis como la infección del hombre por E. histolytica (cuadro 84.2), con independencia de que esta dé lugar o no a manifestaciones clínicas. Como en el caso de otras infecciones, el desarrollo de signos y síntomas atribuibles a la invasión amebiana está supeditado a la interacción de factores relacionados con el parásito, el hospedero y el medio ambiente, a los cuales se hace referencia en otros acápites de este capítulo. Cuadro 84.2. Clasificación taxonómica de E. histolytica Ciclo de vida La carencia de etapas sexuales y de hospederos intermediarios, que sí están presentes en el desarrollo ontogénico de otros parásitos, evidencia la sencillez del ciclo evolutivo de E. histolytica (Fig. 84.1). Básicamente, el ciclo de vida de este protozoo pasa por solo dos fases: la de quiste, forma infectante, y la de trofozoito, forma vegetativa. Las condiciones que desencadenan el exquistamiento y el enquistamiento son desconocidas. Fig. 84.1. Ciclo de vida de E. histolytica. En la parte superior están representadas las principales vías por las cuales los quistes pueden llegar al sistema digestivo del hombre. En ambos laterales se aprecian las diferentes etapas del ciclo biológico de esta especie amebiana: 1 y 8, quistes; 2, trofozoito metaquístico; 3 y 4, trofozoitos de menor tamaño; 5, trofozoito maduro; 6, prequiste y 7, quiste maduro. Al centro están esquematizadas las consecuencias de la invasión por E. histolytica: eventualmente, los trofozoitos amebianos penetran en la mucosa y forman úlceras en
- 10. ella. Desde esta localización pueden hacer migraciones al hígado, y desde este a otros tejidos aún más distantes. La infección es adquirida, casi exclusivamente, por la ingestión de quistes tetranucleados. Estos son resistentes a los efectos del pH ácido del estómago del hospedero y la exquistación debe ocurrir, en el intestino delgado. Allí, la alcalinidad del medio o la acción de determinadas enzimas digestivas, o ambas circunstancias, debilitan la pared del quiste, y emerge del mismo una ameba multinucleada, denominada metaquiste. Por división citoplasmática, esta estructura da lugar a cuatro pequeñas amebas, llamadas trofozoitos metaquísticos. Una nueva división, esta vez nuclear y citoplasmática, da origen a ocho trofozoitos similares a los precedentes. Los trofozoitos metaquísticos, incapaces de colonizar el intestino delgado, son arrastrados por las heces y llegan al intestino grueso. En esta región, utilizando el amplio arsenal de moléculas con actividad lítica presentes en su membrana celular y en su citoplasma, estos pequeños metaquísticos trofozoitos se alimentan de bacterias y otras células en contacto con su superficie. Aumentan de tamaño y alcanzan las dimensiones definitivas de los trofozoitos maduros. En la luz y en las criptas de la mucosa del intestino grueso, los trofozoitos amebianos continúan multiplicándose por simple división binaria y, eventualmente, pueden invadir la pared de esta víscera e, incluso, hacer migraciones a órganos y tejidos distantes. Paradójicamente, la invasión de los tejidos del hospedero por trofozoitos de E. histolytica, que no es necesaria para su ciclo de vida, no da lugar a quistes y, por tanto, no contribuye a la diseminación y perpetuación de la especie. La evolución de los trofozoitos amebianos en la luz intestinal sigue con más frecuencia un curso diferente al descrito en el párrafo anterior. Como consecuencia de condiciones en el colon aún no bien precisadas, pero aparentemente adversas para los trofozoitos, estos comienzan a eliminar sus vacuolas alimenticias, entre otras inclusiones citoplasmáticas, y a condensarse en una masa esférica, el prequiste. Posteriormente, esta célula se cubre de una pared protectora y se convierte en un quiste inmaduro. Este, como los trofozoitos que lo preceden, solo posee un núcleo. Dos divisiones nucleares sucesivas, que dan origen a un quiste tetranucleado, caracterizan su proceso de maduración. Se pueden encontrar trofozoitos, prequistes y quistes en diferentes fases de maduración en las heces humanas. De estos, la única forma infectante por vía oral es el quiste maduro (quiste tetranucleado), que, en dependencia de las condiciones ambientales, puede permanecer viable semanas y meses. Aspectos estructurales de E. histolytica Se han publicado recientemente revisiones bibliográficas exhaustivas sobre aspectos estructurales de E. histolytica, uno de los organismos eucarióticos más primitivos. Trofozoito
- 11. Los trofozoitos de E. histolytica presentan formas muy disímiles y miden entre 10 y 60 μm de diámetro. Estas amplias variaciones en forma y tamaño dependen, entre otros factores, del grado de actividad del parásito, siendo mayor el pleomorfismo y la talla de los trofozoitos hallados en heces disentéricas recién evacuadas que los encontrados ocasionalmente en heces de portadores asintomáticos. El citoplasma de los trofozoitos amebianos presenta dos áreas relativamente bien definidas: una porción externa hialina, transparente, sin gránulos, que recibe el nombre de ectoplasma, y una porción interna granular que contiene diversas inclusiones, algunas de ellas vacuolas fagocíticas, denominada endoplasma. La presencia de eritrocitos entre los elementos fagocitados es característica de E. histolytica (Fig. 84.2). Fig. 84.2. Trofozoito de E. histolytica en fresco. Se puede observar el aspecto transparente del ectoplasma dentro del seudópodo y el carácter granuloso del endoplasma, en el que se ven varios hematíes ingeridos. En frotis directo, sobre todo de heces disentéricas, es posible observar el movimiento progresivo, en ocasiones explosivo, de los trofozoitos de E. histolytica. Este es el resultado de la aparición de prolongaciones digitiformes del ectoplasma, denominadas seudópodos, hacia cuyo interior fluye posteriormente el endoplasma. Con el microscopio electrónico de barrido es posible observar otras especializaciones de la superficie amebiana (Fig. 84. 3). Fig. 84.3. Trofozoito de E. histolytica en el microscopio electrónico de barrido. Se aprecia fagocitosis de células epiteliales. Mediante el empleo de métodos de coloración, ya no es posible observar la movilidad del trofozoito, pero se hacen evidentes características de su núcleo que permiten identificar a E. histolytica de manera más precisa. Convenientemente fijado y teñido (Fig. 84.4), el núcleo es esférico y representa aproximadamente un cuarto de la talla del trofozoito; tiene un cariosoma compacto y pequeño localizado más o menos en su centro; y su cromatina se halla dispuesta en la periferia, junto a la superficie interna de la membrana nuclear, de manera finamente granular.
- 12. Fig. 84.4. Trofozoito de E. histolytica teñido con hematoxilina férrica. Se puede observar el aspecto finamente granuloso del endoplasma, donde se aprecian algunos hematíes y los característicos núcleos de la especie. Prequiste El prequiste es una célula inmóvil, de forma ovalada o redonda, de 10 a 20 μm de diámetro, aún sin cubierta quística y con algunas inclusiones citoplasmáticas. En relación con la fase de trofozoito, aparecen dos nuevas estructuras en el citoplasma del prequiste (Fig. 84.5): una vacuola de glucógeno más o menos grande y de bordes difusos, que aporta los requerimientos energéticos para la maduración del quiste, y unos cuerpos refringentes, de forma cilíndrica y de tipo cristalino que reciben el nombre de cuerpos cromatoidales. El núcleo muestra un tamaño superior y su cariosoma ya no es tan compacto. Fig. 84.5. Prequiste de E. histolytica/ E. dispar teñido con tricrómica. Se distingue una vacuola de glucógeno grande y algo coloreada, dos cuerpos cromatoidales y un núcleo relativamente grande, en el que el cariosoma se encuentra difuso. Quiste Hasta el presente, la obtención de quistes de E. histolytica no ha sido posible mediante cultivo in vitro. Por este motivo, la información de que se dispone acerca de la estructura de estos es mucho menor que la existente con respecto a los trofozoitos. En general, como los prequistes que los preceden, los quistes son células inmóviles, de formas ovaladas o redondas y miden entre 10 y 16 μm de diámetro (Fig. 84.6). Los quistes de E. histolytica, a diferencia de los trofozoitos de la misma especie, tienen tamaño y formas relativamente uniformes. Fig. 84.6. Quiste de E. histolytica/E. dispar teñido con tricrómica. Se muestran los cuatro núcleos característicos de los quistes maduros de estas especies y un cuerpo cromatoidal grande. Apenas se observan inclusiones citoplasmáticas en los quistes. La vacuola de glucógeno, remanente de la etapa anterior, se observa en los quistes inmaduros y prácticamente no existe en los quistes maduros (el glucógeno ha sido consumido durante el proceso de maduración). Se conservan los cuerpos cromatoidales surgidos en la fase anterior y, en dependencia del grado de maduración del quiste, este contiene de uno a cuatro núcleos con las características de especie ya descritas para el trofozoito. Marcadores de patogenicidad
- 13. Durante más de seis décadas, a varias generaciones de amebólogos llamó la atención la marcada diferencia siempre encontrada entre la prevalencia de infección por E. histolytica y la incidencia de enfermedad en los individuos supuestamente infectados por este protozoo. Sobre la base de estudios realizados en diferentes áreas geográficas, se estimó que alrededor de 10 % de la población mundial estaba infectada y, sin embargo, poco menos de 1 % desarrollaba manifestaciones clínicas. Para dar explicación a este hecho, se formularon varias hipótesis. Obviando algunos detalles, estas pueden ser resumidas en tres: 1. E. histolytica es una especie que siempre produce lesiones intestinales en el humano, y aquellas pueden dar lugar o no a manifestaciones clínicas. 2. E. histolytica es normalmente un comensal que habita en el colon humano y, en ocasiones, por razones no conocidas, se convierte en un patógeno invasor. 3. E. histolytica es un complejo de dos especies morfológicamente idénticas: una especie patógena que, en dependencia del contexto en que reside, exhibe diferentes grados de virulencia, y otra que no invade los tejidos. Existen elementos probatorios sobre la tercera de estas hipótesis y hoy está demostrada la existencia de marcadores de patogenicidad amebianos (cuadro 84.3). Cuadro 84.3. Marcadores de patogenicidad de E. histolytica Marcadores funcionales Trabajos de los 80 del siglo XX probaron que las cepas aisladas de individuos sintomáticos, en relación con las obtenidas de personas asintomáticas, tenían propiedades funcionales diferenciantes. Ellas son: mayor capacidad de aglutinación en presencia de la lectina concanavalina A (característica asociada a la presencia de receptores de superficie con un alto contenido de glucosa y manosa); carencia de carga negativa de superficie a pH neutro (lo cual favorece la adherencia a células de mamíferos cargadas negativamente); mayor habilidad para realizar eritrofagocitosis, poseer mayor efecto citopático in vitro; y, para solo hacer referencia a las mejor
- 14. caracterizadas, capacidad de producir lesiones (en colon e hígado) en animales de experimentación. Marcadores bioquímicos En 1978 Peter Sargeaunt y colaboradores reportaron un estudio de tipificación de isoenzimas, basándose en sus respectivas movilidades electroforéticas, que les permitió la clasificación de las amebas procedentes de más de 6 000 aislamientos, en las que entonces se denominaron cepas de E. histolytica patógenas y no patógenas. A partir de ese momento, los intentos por diferenciar las amebas de aislamientos obtenidos de pacientes con diferentes formas clínicas de la infección, y de individuos asintomáticos, se extendieron ampliamente, y se emplearon para ello variados y novedosos procedimientos bioquímicos, inmunológicos y genéticos. Marcadores inmunológicos La utilización de anticuerpos monoclonales a partir de 1988 permitió distinguir entre aislamientos con patrones isoenzimáticos patógenos y no patógenos (posteriormente E. histolytica y E. dispar). Marcadores genéticos Son las evidencias de tipo genético las más convincentes respecto a la aceptación de la hipótesis de las dos especies. Las primeras datan de finales de la década de 1980, cuando se clonaron y caracterizaron dos sondas de ADN, denominadas P145 y B133, procedentes de moléculas circulares de ADN extracromosomal de cepas patógenas y no patógenas, respectivamente, que hibridaban de manera selectiva con los correspondientes aislamientos. El conjunto de evidencias (funcionales, bioquímicas, inmunológicas y genéticas), contribuyó a favor de la existencia de las dos especies de amebas y condujo a Louis Diamond y Graham Clark, en 1993, a la redescripción formal de E. histolytica (Fig. 84.7), separándola de E. dispar (Fig. 84.8). Fig. 84.7. E. histolytica. Trofozoito observado con el microscopio electrónico de barrido. Fig. 84.8. E. dispar. Trofozoito observado con el microscopio electrónico de barrido. En enero de 1997, un grupo de expertos en amebiasis de la OMS, reunido en Ciudad de México, evaluó las implicaciones que para la práctica médica y para las investigaciones sobre amebiasis tiene la confirmación de la existencia de las dos especies, implicaciones que revolucionan ya, entre
- 15. otros aspectos, la interpretación de los datos epidemiológicos, y los criterios diagnósticos y terapéuticos en relación con esta parasitosis. Factores de virulencia Las fases que caracterizan la infección invasiva por E. histolytica han sido mejor estudiadas en modelos animales. De manera general, estas se suceden así: adherencia al epitelio intestinal, degradación de la matriz extracelular, lisis extracelular (por contacto) e intracelular (por fagocitosis) de células del hospedero y evasión de los mecanismos defensivos de este. Veamos con más detalles cada uno de estos eventos y los factores de virulencia de E. histolytica relacionados con los mismos (cuadro 84.4). Cuadro 84.4. Fases de la invasión amebiana y factores de virulencia de E. histolytica vinculadas a esta Adherencia al epitelio intestinal Como en el caso de otros microorganismos que parasitan el tubo digestivo, E. histolytica requiere adherirse a la pared de esa víscera. Varias moléculas han sido implicadas en la adhesión amebiana al epitelio intestinal, paso necesario para fases posteriores del proceso invasivo. Dos de ellas han recibido la mayor atención: la lectina Gal/GalNAc, a la cual ya hicimos referencia en el acápite anterior, y una adhesina de 112 kDa (Fig.84.9).
- 16. Fig. 84.9. Trofozoitos de E. histolytica incubados con un anticuerpo monoclonal que reconoce a la adhesina de 112 kDa en la membrana plasmática y un anticuerpo secundario acoplado al fluoróforo FITC. Los trofozoitos fueron contrateñidos con yoduro de propidio para la tinción de núcleos. Analizados con un microscopio invertido acoplado a un microscopio confocal. Degradación de la matriz extracelular En modelos murinos de amebiasis, la superficie luminal del epitelio intestinal experimenta marcados cambios estructurales (acortamiento de las microvellosidades y aumento del espacio intercelular en la porción apical) antes de la interacción directa con trofozoitos de E. histolytica. Después del contacto, estos trofozoitos penetran en el epitelio por puntos situados entre las glándulas de Liëberkuhn, donde la capa de mucus que lo recubre es más delgada. Esta cronología de hallazgos patológicos sugiere que la disolución de la matriz extracelular precede la invasión directa y la lisis dependiente de contacto de células del hospedero. Después del contacto, moléculas de E. histolytica con actividad proteolítica dependiente de cisteína parecen ser las principales responsables de la degradación de la matriz extracelular. El papel de estas moléculas como factor de virulencia está sustentado por su habilidad para degradar componentes de la matriz extracelular como colágeno, elastina y fibronectina, y en el hecho de que E. histolytica, en relación con E. dispar, libera mayor cantidad de este tipo de proteinasas. Lisis extracelular de células del hospedero La lisis extracelular de células del hospedero, en particular células epiteliales e inflamatorias, por trofozoitos de E. histolytica durante la invasión hística, es un evento sobre el que no existen dudas. Sin embargo, los mecanismos por los cuales dichas células son lisadas no son bien conocidos. Moléculas de varios tipos participan en el proceso por el cual los trofozoitos de E. histolytica lisan por contacto sus dianas celulares. Dicho proceso requiere de la lectina Gal/ GalNAc, de proteinasas cisteíno-dependientes y de la presencia extracelular de iones Ca2+. Mediadores adicionales son necesarios. A continuación, nos referiremos a varios de ellos. Amebaporos E. histolytica posee una familia de pequeños péptidos, denominados proteínas formadoras de poros o simplemente amebaporos, que tienen la capacidad de insertarse en la bicapa lipídica de la membrana de la célula blanco y formar canales por los que difunden agua y otras moléculas, lo que produce la inmediata lisis de la célula. Fosfolipasa A Una fosfolipasa A de E. histolytica parece participar en la lisis de leucocitos polimorfonucleares en las áreas donde está teniendo lugar la invasión amebiana. Otras moléculas con actividad citolítica
- 17. Otras moléculas de E. histolytica han sido implicadas en el proceso lítico y, por tanto, también han sido consideradas factores de virulencia de esta especie. Entre las más recientemente reportadas, se encuentra un grupo de hemolisinas que in vitro son citotóxicas a una línea de células epiteliales de intestino (Caco-2). Sin embargo, las evidencias experimentales en favor de la actividad citolítica de estas moléculas son aún escasas y no permiten, por el momento, precisar su real significación biológica. Lisis intracelular de células del hospedero Aparentemente, tanto E. histolytica como E. dispar fagocitan y lisan intracelularmente células del hospedero. Sin embargo, E. histolytica, en particular las cepas más virulentas, realiza estas actividades con mucha mayor intensidad. Evasión de los mecanismos defensivos del hospedero Desde el momento mismo de la llegada de E. histolytica al lumen intestinal, el hospedero opone barreras defensivas de muy diversos tipos a la multiplicación e invasión amebianas. Para vencer estos obstáculos, y poder alcanzar localizaciones tan distantes como los tejidos hepático y cerebral del individuo que parasita, E. histolytica despliega una amplia gama de mecanismos evasivos. A estos mecanismos nos referiremos más adelante. Patología de la invasión amebiana La invasión amebiana de la mucosa intestinal se puede iniciar por uno o más puntos de cualesquiera de las partes del intestino grueso; a partir de aquellos, o desde el lumen de este órgano, la infección se puede diseminar a otras áreas del colon. En orden decreciente de frecuencia, los segmentos anatómicos por donde suele comenzar la invasión, con la formación de úlceras, son el ciego, colon sigmoide y recto, regiones donde se produce un estasis más prolongado del contenido intestinal. Después de formada la úlcera intestinal (Figs. 84.10 y 84.11), la invasión amebiana puede evolucionar de las siguientes maneras (cuadro 84.5): Fig. 84.10. Típica úlcera amebiana. Se observa la invasión de la mucosa y submucosa del colon Fig. 84.11. Fondo de úlcera amebiana. Se aprecian trofozoitos con numerosos eritrocitos fagocitados. Cuadro 84. 5. Posibilidades evolutivas una vez formada la úlcera amebiana
- 18. 1. Cura espontánea o por tratamiento:con el tratamiento amebicida adecuado, y en ocasiones sin él, las lesiones iniciales pueden curar sin dejar huellas. 2. Megacolon tóxico: esta forma evolutiva, de muy mal pronóstico, es el resultado de la confluencia de numerosas úlceras y de la necrosis de grandes áreas del intestino grueso (Fig. 84.12). En estos casos la mortalidad es muy alta. 3. Perforación intestinal: generalmente, los trofozoitos de E. histolytica llegan a la capa submucosa y no atraviesan la muscular, pero, en ocasiones, pueden penetrar esta última capa, extenderse a la serosa y aún perforarla (Fig. 84.13). Esta complicación, que es más frecuente en las úlceras situadas en el ciego, es casi siempre de evolución fatal. 4. Ameboma: este vocablo designa una forma evolutiva poco frecuente de la amebiasis invasiva, macroscópicamente caracterizada por el desarrollo de una masa tumoral que tiende a obstruir la luz intestinal y a simular un adenocarcinoma (Fig. 84.14). Esta tumoración, que puede llegar a medir hasta 30 cm en su eje mayor, suele ser única y de forma irregular. También puede presentarse como una masa constrictiva anular de varios centímetros de grosor. En la mucosa sobre el ameboma, generalmente edematosa y muchas veces sangrante, se pueden observar zonas de necrosis. Como en el caso de las úlceras amebianas iniciales (a partir de las cuales se origina) el ameboma se ubica, en orden decreciente de frecuencia, en ciego, colon sigmoide y recto. En términos microscópicos, la principal característica de esta lesión es la presencia de un tejido de granulación, con linfocitos y células gigantes, y la ausencia de trofozoitos en el interior de la misma. El ameboma del colon puede coexistir con úlceras del órgano en las que, desde luego, sí es posible encontrar los trofozoitos de E. histolytica. 5. Diseminación hematógena al hígado y de este a otras localizaciones: a pesar de que con cierta frecuencia se han observado trofozoitos de E. histolytica en vasos linfáticos de la pared intestinal, estos rara veces son encontrados en los ganglios linfáticos mesentéricos. De aquí que esté universalmente aceptado que la principal vía de diseminación extraintestinal de la infección amebiana sea la hematógena. Desde la submucosa intestinal, y después de digerir la pared de pequeñas vénulas mesentéricas, los trofozoitos llegan al hígado en la circulación portal. En este órgano forman uno o más abscesos, la mayoría de las veces en su lóbulo derecho (Fig. 84.15). El absceso hepático es la más frecuente de las lesiones extraintestinales de la amebiasis invasiva. Desde él puede haber diseminación a sitios extrahepáticos por ruptura (a peritoneo, estómago, duodeno, vías biliares, colon, pleura, pulmón, pericardio y mediastino); por continuidad (a pared abdominal y piel); y por vía hematógena (a cerebro). La migración sanguínea de
- 19. trofozoitos de E. histolytica desde la submucosa intestinal a localizaciones extrahepáticas, sin producir afectación del hígado, es muy rara. 6. Extensión directa a la piel: esta es una evolución poco frecuente y de la cual es escasa la información existente. Fig. 84.12. Megacolon tóxico. Se observan perforaciones intestinales múltiples. Fig. 84.13. Amebiasis intestinal. Aspecto macroscópico de perforación intestinal. Fig. 84.14. Vista endoscópica de un ameboma. Fig. 84.15. Aspecto macroscópico de abscesos hepáticos amebianos múltiples. Alteraciones morfológicas de la colitis ulcerativa amebiana Alteraciones histopatológicas observadas en modelos animales han sugerido que la degradación de la matriz extracelular, posiblemente por proteinasas cisteíno-dependientes secretadas por E. histolytica, precede el contacto directo de este protozoo con la superficie epite-lial. E. histolytica invade los diferentes planos de la mucosa del colon merced a la actividad lítica a la que debe su nombre. Después de multiplicarse activamente en la mucosa, en la que finalmente provocan una microulceración superficial, los trofozoitos de E. histolytica se extienden hacia planos más profundos de la pared intestinal, pasan la lámina propia, la muscularis mucosae, y llegan hasta la submucosa, donde las condiciones para su reproducción son aún más favorables. A partir de este momento, la progresión de la destrucción de los tejidos se produce en dirección horizontal. En consecuencia, se desarrolla una lesión de amplio fondo y pequeño orificio de entrada, la clásica úlcera en “botón de camisa” presente en la colitis ulcerativa amebiana. El contenido necrótico de la submucosa está formado por trofozoitos, presentes en mayor cuantía en los bordes y fondo de la lesión, células inflamatorias muertas y detritos celulares.
- 20. Alteraciones morfológicas del absceso hepático amebiano Los abscesos amebianos del hígado se localizan preferentemente en el lóbulo derecho de esta víscera, suelen ser únicos con mayor frecuencia que múltiples y sus tamaños, muy variables, fluctúan entre pocos milímetros y 20 cm o más (Fig. 84.16). Fig. 84.16. Aspecto macroscópico de absceso amebiano hepático del lóbulo derecho. El examen microscópico de un absceso hepático amebiano completamente desarrollado revela el reemplazo de una extensa zona de parénquima por un material necrótico, característicamente eosinofílico, granular y con restos de estructuras nucleares; la escasa presencia de células inflamatorias, casi exclusivamente en los bordes de la lesión; y la activa multiplicación de los trofozoitos, también limitada a las áreas en que avanza la invasión (Fig. 84.17). Por lo general, el absceso es bacteriológicamente estéril. Fig. 84.17. Aspecto microscópico de absceso hepático amebiano. Se distinguen trofozoitos en el borde de la lesión. Aunque la frontera entre la zona de absceso y el tejido hepático no afectado está bien definida macroscópicamente (en los abscesos crónicos, incluso, puede formarse una cápsula fibrosa limitante), a escala microscópica no existe una separación neta y lo regular es encontrar una franja limítrofe de parénquima desorganizado, cuya arquitectura muestra signos de atrofia, fibrosis y compresión. Inmunobiología de la infección amebiana Mecanismos defensivos inespecíficos a E. histolytica Muchos aspectos de la inmunobiología de la infección del humano por E. histolytica no son bien conocidos. Ello obedece, fundamentalmente, a que en el caso de la amebiasis, a diferencia de otras interacciones hospedero-parásito, no existe un modelo animal que remede adecuadamente la cronología de eventos que ocurre en esta parasitosis. En relación con los mecanismos defensivos inespecíficos, la información acumulada nos permite referirnos a los siguientes aspectos. Funciones defensivas del mucus intestinal En el caso de la infección por E. histolytica, el mucus intestinal realiza funciones defensivas por, al menos, dos mecanismos: atenuación, como consecuencia de su viscosidad, de las funciones
- 21. motrices de E. histolytica y unión de parte de las glicoproteínas que lo componen, por intermedio de sus residuos oligosacarídicos, a la lectina Gal/GalNAc de los trofozoitos de E. histolytica. Esta última acción tiene dos consecuencias: el impedimento a la adherencia de los trofozoitos al epitelio subyacente y el atrapamiento de los mismos en el interior del mucus, con su posterior eliminación peristáltica. Reclutamiento de neutrófilos La caraterización cronológica de los cambios patológicos producidos en intestino e hígado por la invasión amebiana ha permitido concluir que los neutrófilos, aunque escasamente presentes en las lesiones bien establecidas, incluido el absceso hepático, son las primeras células en responder al contacto de este protozoo con los tejidos del hospedero. Estudios in vitro han demostrado que la incubación de monocapas de células de diferentes líneas de cultivo (células epiteliales de colon T84, LS174T y Caco-2) con proteínas amebianas, con productos secretados por E. histolytica, o con los propios trofozoitos de esta especie, resulta en un aumento en la secreción de IL-8 por las primeras. El incremento en la secreción de IL-8 se produce, incluso, en ausencia de contacto directo entre los trofozoitos amebianos y las células epiteliales. Con base en estos hallazgos, se ha sugerido que IL-8 es secretada por las células epiteliales del colon ante la presencia de trofozoitos de E. histolytica, y que esta citoquina actúa como agente quimiotáctico para la infiltración por neutrófilos que caracteriza las primeras etapas de la invasión amebiana. Activación de la vía alternativa del complemento Como barrera defensiva contra E. dispar, la activación de la vía alternativa del sistema del complemento es altamente eficiente. De hecho, este es uno de los mecanismos por los cuales no se produce la invasión hística por esta especie. Sin embargo, E. histolytica, particularmente las cepas más virulentas, ha desarrollado la capacidad de evadir los efectos biológicos que se derivan de la activación de este sistema. Fagocitosis y eliminación de trofozoitos amebianos por células mononucleares Células mononucleares de humanos y de animales de experimentación son capaces de fagocitar trofozoitos de E. histolytica. En la lisis intracelular de los trofozoitos fagocitados participan mecanismos microbicidas dependientes e independientes de oxígeno. Evidencias recientes demuestran que el óxido nítrico (NO, del inglés: nitric oxide), derivado de L-arginina, es el principal mediador de la muerte amebiana intramacrofágica. La información respecto a la adquisición de inmunidad después de la infección por E. histolytica es limitada. No obstante, se conoce que la curación de un episodio de colitis amebiana o de un absceso hepático amebiano resulta en el desarrollo de cierto grado de inmunidad.
- 22. INTRODUCCIÓN GIARDIA DUODENALIS Giardia lamblia es un protozoo flagelado que fue primeramente observado por Van Leewenhoek en 1681, y más detalladamente descrito por Vilein Lamb en 1859. Aunque durante mucho tiempo se pensó que era un comensal humano, no es hasta los años 60 que se comienza a conocer claramente que puede producir diarreas y malabsorción en el hombre. Este parásito constituye una de las principales infecciones intestinales del hombre, y está presente en forma endémica aun en países desarrollados. Puede llegar a producir brotes de infección a través de la ingestión de aguas o alimentos contaminados, y por transmisión de persona a persona como en las guarderías infantiles. Clasificación taxonómica G. lamblia es un protozoo flagelado que ha sido clasificado taxonómicamente como se refiere a continuación: 1. Reino: Protista. 2. Subreino: Protozoa. 3. Phyllum: Sarcomastigophora. 4. Subphyllum: Mastigophora. 5. Clase: Zoomastigophorea. 6. Orden: Diplomonadida. 7. Familia: Hexamitidae. 8. Género: Giardia. 9. Especie: lamblia. Los quistes son entre redondos u ovales y miden de 8 a 14 por 7 a 10 μm. Cada uno de ellos tiene cuatro núcleos y contiene estructuras como axonemas y cuerpos medianos. Los flagelos, al igual que los axonemas, están enrollados. Los trofozoitos tienen simetría bilateral, miden de 10 a 20 μm de largo por 5 a 15 μm de ancho, y tienen la forma de “una gota lagrimal” cuando son vistos en sentido dorsal o ventral. Son convexos en sentido dorsal y presentan un disco suctorial cóncavo en su porción ventral. Poseen cuatro pares de flagelos dispuestos simétricamente. De ellos, dos son anterolaterales, y dos posterolaterales, dos ventrales y un par caudal, los que tienen su origen en ocho cuerpos parabasales colocados simétricamente en la línea media, a la altura del borde superior de los núcleos. Además presentan dos axonemas y dos cuerpos medianos. Los trofozoitos tienen dos núcleos que son idénticos, ambos ovoides y con el endosoma central bien diferenciado.
- 23. Estos protozoos contienen cinco cromosomas y son poliploides. Algunas estructuras, tales como las mitocondrias, el retículo endoplásmico rugoso y los nucléolos no han sido identificadas, lo que conforma la hipótesis de que este organismo es un eucariote primitivo. En realidad tres especies de Giardia han sido descritas basado en las diferencias identificables de los cuerpos medianos, las que pueden ser apreciadas por el microscopio óptico. Estas especies, según Filice, son Giardia agilis procedente de anfibios; Giardia muris, de roedores, aves y reptiles; y Giardia lamblia (también llamada G. intestinalis o G. duodenalis) procedente de mamíferos. Existen dos especies adicionales que son indistinguibles de G. lamblia por el microscopio de luz: G. ardeae (de garzas) y G. psittaci (de cierto grupo de aves), las que han sido identificadas a partir de las diferencias morfológicas en el examen, por el microscopio electrónico. G. lamblia, se encuentra en animales domésticos como gatos y perros, así como en una variedad de animales silvestres como los castores, que han sido implicados en brotes de transmisión hídrica. Ciclo de vida El ciclo de vida está compuesto de dos estados fundamentales: el trofozoito y el quiste. El quiste es la forma infecciosa de este protozoo y es relativamente inerte y resistente a los cambios ambientales, aunque puede ser destruido por la desecación y el calor. Sin embargo, es viable en agua fría hasta por 16 días, y es resistente a las concentraciones de cloro utilizadas habitualmente en los sistemas de acueductos. Después de la ingestión, ocurre la exquistación que comienza en el estómago y se completa en el duodeno, como resultado de la exposición al pH ácido del estómago y a las enzimas pancreáticas quimiotripsina y tripsina, y producen dos trofozoitos (estado vegetativo) de cada quiste. Los trofozoitos se replican en las criptas del duodeno y en la porción superior del yeyuno, y se reproducen asexualmente por fisión binaria o bipartición. Algunos de los trofozoitos pueden enquistarse en el íleon, posiblemente como resultado de la exposición a sales biliares o a la ausencia de elementos nutritivos como el colesterol (Fig. 78.1).
- 24. Fig. 78.1. Ciclo de vida de Giardia lamblia. 1. Trofozoito oforma vegetativa de frente. 2. Trofozoito o forma vegetativa de perfil. 3. Forma quística con dos núcleos. 4. Quiste maduro (cuatro núcleos). Tomado de Kourí P et al. Lecciones de Parasitología, Tomo II. Protozoología Médica. 1963. Las infecciones experimentales han demostrado que la infección puede establecerse con inóculos tan pequeños como un trofozoito o 10 quistes. Los quistes han aparecido en las heces entre 5 y 41 días posteriores a la infección experimental, y entre 2 y 3 semanas en viajeros que retornan de áreas endémicas. Patogenia y fisiopatología En los casos sintomáticos, se ha observado aplanamiento de las microvellosidades, infiltración linfocítica y malabsorción. En ocasiones, este acortamiento de las micro-vellosidades recuerda al de la enfermedad celíaca, sobre todo en individuos con hipo-gammaglobulinemia; sin embargo, no se ha observado invasión hística y a veces se ve un gran número de trofozoitos en las criptas duodenales sin evidencias de trastornos patológicos. La presencia de una toxina no ha sido bien demostrada hasta la fecha, y no existen otros mecanismos potenciales identificados a través de los cuales el protozoo pueda causar diarrea. Otros mecanismos propuestos incluyen disrupción del borde en cepillo y procesos inmunopatológicos, además de que se plantea la interferencia mecánica por efecto de tapizado, que pueden producir los trofozoitos adheridos al duodeno, acompañados de la inflamación catarral consecuente. La respuesta inmunitaria desempeña un importante papel en la patogenia a nivel de la mucosa intestinal. Al menos, 20 polipéptidos con un rango de peso molecular que va de 14 a 125 kDa han sido identificados a partir de extractos crudos de trofozoitos. Varios estudios han reportado que el polipéptido de 82 kDa es el antígeno mayor de superficie en los trofozoitos. Los aislamientos de diferentes áreas geográficas tienen semejanzas antigénicas. Los antígenos de quistes detectados en heces humanas tienen pesos moleculares que varían entre 21 y 49 kDa. Otras moléculas producidas por el protozoo son las proteínas de choque térmico (heat shock proteins), las lectinas, las giardinas, las tubulinas y las quitinas. La variación antigénica ocurre en la giardiosis y ha sido reportada tanto in vivo como in vitro. Los antígenos variables de superficie han sido localizados en la membrana superficial de los trofozoitos; la mayoría de ellos tienen una estructura con abundantes residuos de cisteína. La inmunidad innata desempeña un papel para el control de la infección. En la inmunidad adquirida, ambas vertientes del sistema inmunológico, la humoral y la celular, tienen una importante función para el control de la infección. Los anticuerpos IgM, IgA e IgG específicos cumplen un papel mayor, tanto como las células T, los macrófagos y los neutrófilos. Los componentes accesorios del sistema inmunológico, tales como el complemento, son importantes. Pocos estudios se han desarrollado para averiguar el papel de las citoquinas. La resistencia adquirida frente a la giardiosis ha sido bien documentada solo en modelos animales.
- 25. Se ha reportado que Giardia puede deprimir el sistema inmunológico de los hospederos infectados. La infección es más severa en las personas afectadas por hipogammaglobulinemia. Sin embargo, la infección no es más severa en los pacientes afectados por otros agentes infecciosos que pueden deprimir el sistema inmunológico, como los afectados por el SIDA. Por diversas razones, la sensibilidad de los ensayos serológicos para detectar anticuerpos contra Giardia es baja, aun cuando se utiliza el suero de pacientes con casos clínicos probados. Manifestaciones clínicas La infección en el hombre tiene una evolución clínica variable, que va desde la infección asintomática, la mayoría de las veces, hasta la diarrea severa. Esto parece estar relacionado tanto con factores del hospedero como del agente biológico. El período de incubación después de la ingestión de quistes es variable y puede ser tan corto como 1 ó 2 semanas. Los signos y síntomas de la enfermedad son difíciles de distinguir de los de otras enfermedades gastrointestinales. La infección no siempre produce diarrea. De hecho, otros síntomas digestivos como los dolores abdominales y los cólicos pueden ocurrir más frecuentemente que la diarrea. Giardia es reconocida como una causa de rápida pérdida de peso y malabsorción de grasas, y puede presentarse lo mismo en forma crónica, que en forma aguda. Entre los síntomas digestivos más comunes están la diarrea, los cólicos o dolores abdominales, náuseas, meteorismo y disminución del apetito. En los pacientes con hipogammaglobulinemia, la enfermedad puede ser más grave, con tendencia marcada a la cronicidad y a la malabsorción. Esto es más evidente en las personas con deficiencias de la IgA secretora. También se ha señalado la deficiencia subclínica de lactasa que puede llevar a una intolerancia de la lactosa, que pudiera persistir aún un tiempo después de la erradicación del parásito. Algunas manifestaciones extraintestinales inusuales han sido descritas y se han involucrado mecanismos inmunoalérgicos para explicar su patogénesis, dentro de las cuales se señalan la urticaria, la artritis reactiva, y hasta raros casos de bronquitis y retinitis alérgica. También se ha señalado, pero con baja frecuencia, la enfermedad biliar. Este parasitismo se ha visto muy relacionado con trastornos del crecimiento y desarrollo en los niños. De todas formas, numerosas investigaciones se acometen para elucidar este último aspecto, debido a que en ocasiones se hace muy difícil evaluar los efectos de la infección por este flagelado sobre el crecimiento y el estado nutricional en niños, a causa de la presencia de varios factores, como múltiples patógenos que pudieran explicar estas diferencias en el crecimiento. Diagnóstico Aunque el examen microscópico de las heces es el método más práctico y efectivo para establecer la presencia de la infección en el hombre, la excreción de quistes puede ser errática, lo que
- 26. pudiera llevar a falsos negativos. Por esta razón, es importante la realización de exámenes seriados con el fin de aumentar la sensibilidad. El examen microscópico de las heces consume tiempo y requiere muchas veces de buena calificación y experiencia del personal que realiza el diagnóstico; los quistes y trofozoitos de Giardia se pueden observar en frotis húmedos directos o con coloraciones permanentes. En ocasiones se ha descrito la presencia de quistes retraídos que pierden su estructura normal y toman una coloración anormalmente azulosa o grisácea hialina con la coloración de Lugol (Fig. 78.2). Fig. 78.2. Quiste de G. lamblia teñido con coloración de Lugol en un frotis. El empleo de métodos parasitológicos de concentración como el método de Ritchie (formol - éter//acetato de etilo) o el de Faust (sulfato de zinc) aumenta considerablemente la sensibilidad del examen parasitológico. Algunas sustancias tales como bario, antiácidos, laxantes oleosos y enemas, pueden dificultar los exámenes de heces. En casos de alta sospecha clínica, en los que los exámenes seriados sean negativos, se puede examinar el contenido duodenal por sondaje o intubación directa, por visualización endoscópica, por biopsias o por el empleo menos invasivo de la cápsula del Entero-Test® (cuerda de Beal). Algunos ensayos inmunoenzimáticos sobre fase sólida (ELISA) han sido desarrollados para la detección de antígenos de Giardia en heces, como el que emplea anticuerpos contra el antígeno GSA-65 de G. lamblia. Estos han demostrado una sensibilidad y especificidad comparables a los exámenes microscópicos de alta calidad, pero son más sencillos y consumen menos tiempo cuando un gran número de muestras tienen que ser analizadas. Es bueno aclarar que hasta el momento, estos ensayos comerciales son caros y los reactivos son difíciles de conseguir, sobre todo en países subdesarrollados. Una gran variedad de nuevas tecnologías ha mostrado ser prometedora en evaluaciones recientes. Por ejemplo, se han desarrollado métodos para extracción de los ácidos nucleicos de los quistes, y una prueba de reacción en cadena de la pol imerasa con el uso de adecuados primers, lo que permite detectar la infección y determinar el biotipo de Giardia. Epidemiología Este es uno de los protozoos más comunes del hombre a nivel mundial. Estudios realizados en algunos países subdesarrollados han verificado que a la edad de 3 años todos los niños han sido infectados en esas poblaciones. En países desarrollados, aunque la infección ocurre menos frecuentemente, constituye un importante problema para la salud pública. En los Estados Unidos, por ejemplo, donde la prevalencia de infección parece estar incrementándose, esta es la principal
- 27. causa de brotes de enfermedad diarreica asociados con agua potable y es responsable de un estimado mínimo de 4 000 admisiones hospitalarias al año. En Cuba, la prevalencia de la infección por G. lamblia es de 7,2 % según la encuesta nacional aplicada en 1984, con una muestra representativa de la población cubana; otro estudio posterior desarrollado en los Estados Unidos, demostró en ese país una idéntica tasa de prevalencia. En el estudio cubano nacional de 1984, se encontró una prevalencia superior en las edades de 1 a 5 años con 22,6 %. Otros estudios realizados en Cuba han señalado que casi 20 % de los niños cubanos que asisten a guarderías infantiles están infectados por G. lamblia. Otras investigaciones probaron que esta tasa era similar a la de los niños de las mismas edades (1 a 5 años), que no asistían a guarderías, por lo que se plantea que estas tasas están más relacionadas con el fenómeno de la edad que con l a asistencia a este tipo de institución educacional; y estos resultados son reproducibles en muchas áreas geográficas y en una gran cantidad de estudios epidemiológicos. Por otra parte, se ha evidenciado que existe una pequeña cantidad de niños que asisten a guarderías infantiles con una tendencia o “predisposición” a la infección por G. lamblia, y en ellos se encontró una mayor asociación con síntomas clínicos tales como diarrea; sin embargo, no se conocen bien aún, los factores del parásito, del hospedero o del medio, que están involucrados en la génesis de este fenómeno. En países subdesarrollados, los factores de riesgo para adquirir la infección no están bien definidos. Las infecciones ocurren más frecuentemente en niños que en adultos, con especial énfasis en los preescolares, aunque no está claro aún si esto es debido a una mayor exposición a la parasitosis en la niñez temprana o al desarrollo de inmunidad en la niñez más tardía, después de repetidas exposiciones. Los lactantes parecen estar más protegidos, y esto pudiera deberse al efecto de la leche durante la lactancia materna o por una menor probabilidad de ingerir quistes. La infección por Giardia puede ser transmitida por el agua o los alimentos, y la vía fecal -oral se puede complementar de persona a persona. Sin embargo, poco se conoce acerca de la importancia relativa de las diferentes rutas de la infección. En los países desarrollados los factores de riesgo para la infección incluyen el pertenecer al grupo de 1 a 4 años de edad, asistir a guarderías infantiles, ingerir agua no filtrada, viajar a países donde la infección es altamente endémica, las prácticas de sexo oral -anal, y la presencia de ciertas condiciones médicas tales como la hipogammaglobulinemia. Organismos similares a Giardia se encuentran en una gran variedad de animales. En estudios experimentales, varias especies de animales han sido infectadas con aislamientos de este protozoo obtenidos de humanos y otras especies de animales. Aunque los castores han sido implicados en brotes de transmisión hídrica, no está claro si los humanos pueden ser infectados con aislamientos de Giardia procedentes de animales. La identificación de animales reservorios puede tener importantes implicaciones para el control de la transmisión de Giardia.
- 28. Control y prevención Los esfuerzos de la salud pública para controlar la infección por Giardia se han visto obstaculizados por la falta de conocimientos acerca de la biología, la historia natural, la ecología y la transmisión del microorganismo, los factores de riesgo en diferentes condiciones, y de las respuestas clínicas e inmunitarias de la infección en el hospedero humano. Es probable que el empleo de una sola medida de control no sea completamente efectivo en la prevención y el control de la infección. La estrategia básica para el control de la transmisión de Giardia se basa en prevenir o reducir la exposición a las heces infectivas. Los métodos para llevar esto a cabo pueden ser sofisticados o simples, y deben ser adaptados a las situaciones locales. En algunos países desarrollados, la infección y la enfermedad han sido asociados a brotes de transmisión hídrica, en grupos de riesgo relativamente bien descritos. Sin embargo, aun en estos países, la mayoría de las infecciones más bien son esporádicas que asociadas a brotes, y casi siempre el origen de la infección es desconocida. Las infecciones por Giardia asociadas con el acueducto pueden ser prevenidas por el empleo de sistemas apropiados de filtración y tratamiento, y con una buena protección de los sitios de colección y depósito. Medidas tales como el lavado de las manos, la buena higiene personal, el uso de letrinas y de sistemas adecuados para el depósito de las excretas son recomendadas. Hay que tener en cuenta que en zonas endémicas, el papel de la transmisión persona a persona puede ser muy importante y las medidas de control deben ir dirigidas a interrumpir este ciclo de transmisión. Son muy importantes la educación sanitaria para promover la higiene personal, el suministro de agua potable segura y la efectiva deposición de excretas. La importancia de los animales reservorios no está clara aún y se necesitan todavía más investigaciones al respecto. Existen algunas evidencias clínicas y epidemiológicas que muestran la existencia de inmunidad adquirida, y se han encontrado algunas fracciones antigénicas en las proteínas superficiales de Giardia, asociadas con el desarrollo de inmunidad. Sin embargo, no parece ser factible aún una vacuna en el futuro cercano. Por lo tanto, será necesario un mejor conocimiento de la inmunidad intestinal en general, y de la inmunidad específica contra Giardia. Tratamiento Un buen número de tratamientos ha sido empleado para los pacientes sintomáticos. Los 5- nitroimidazoles son las drogas de elección. Algunos productos de este grupo tales como el tinidazol y el secnidazol se han utilizado en dosis única, pero en ciertos países como en los EE.UU. estos fármacos no se consiguen. Algunos compuestos antihelmínticos del grupo de los benzoimidazoles, como el mebendazol, fueron ensayados con resultados prometedores al principio, pero los estudios posteriores demostraron una baja eficacia. Otros estudios preliminares señalaron una buena eficacia in vitro del antihelmíntico albendazol, pero en ensayos clínicos posteriores y en nuestra propia
- 29. experiencia se llegó a la conclusión de que su eficacia es inferior a la de las drogas antigiardiásicas clásicas. Otra droga de este grupo, el fenbendazol, ha tenido buenos resultados en ensayos preliminares con modelos animales como el perro; sin embargo, su eficacia en humanos debe ser mejor evaluada aún. La quinacrina, que fue uno de los primeros fármacos efectivos para el tratamiento, se ha dejado de usar en algunos países por las reacciones secundarias que puede producir en determinados pacientes. El tratamiento de los niños asintomáticos es controversial. Aunque generalmente se recomienda no tratar estos casos, en ciertas ocasiones se recomienda basado en consideraciones de salud pública, como controlar brotes de giardiosis en guarderías infantiles, cuando otras medidas preventivas no son efectivas, o para prevenir la infección en los convivientes con un alto riesgo de enfermedad severa. En la tabla 78.1 se reflejan los principales fármacos utilizados en el tratamiento de la giardiosis, así como sus dosis más recomendadas tanto en pacientes adultos como en niños. Tabla 78.1. Principales fármacos utilizados en el tratamiento de giardiosis Leyenda: * Fármaco de elección; v: veces. Otros productos como la cloroquina, pirimetamina, mefloquina, rifampicina, azitromicina, y algunas tetraciclinas como la doxiciclina, han sido ensayados in vitro y han demostrado algún grado de actividad. Según nuestra experiencia en un ensayo clínico reciente, la cloroquina mostró una actividad similar al tinidazol y superior al albendazol. Además se han empleado otros nuevos productos, que necesitan ser mejor evaluados, como la nitazoxanida, un derivado nitroti azol, que se han utilizado con éxito en las primeras evaluaciones en humanos. Otros productos naturales, como los propóleos, también se han empleado con resultados muy variables. En la actualidad se continúan los estudios, tanto con productos de origen vegetal como sintéticos con el fin de buscar medicamentos cada vez más eficaces, con pocas reacciones colaterales y que puedan, si es posible, ser eficaces en dosis únicas.
- 30. bvscuba Ecimed Calle 23 No.654 e/ D y E. Plaza de la Revolución. Ciudad de La Habana. CP Sobre los mecanismos protectores que median el desarrollo de inmunidad tras un episodio de amebiasis invasiva existe menor claridad aún. Respuestas inmunitarias mediadas por anticuerpos Varios estudios realizados ilustran la evolución regular de la respuesta inmunitaria humoral a la invasión intestinal por E. histolytica. Esta, aparentemente, consiste en una respuesta de anticuerpos secretorios de corta duración, seguida de una respuesta de anticuerpos séricos más prolongada. Los individuos con absceso hepático amebiano desarrollan una vigorosa respuesta de anticuerpos séricos a E. histolytica, que es detectada 1 semana después de comenzados los síntomas. Durante la amebiasis invasiva, se produce una respuesta de anticuerpos IgA e IgG secretorios a E. histolytica. Estos anticuerpos antiamebianos han sido evidenciados en calostro y en saliva. Sin embargo, existe escasa información acerca de si son también producidos en la evolución de una infección no invasiva. Estudios in vitro han demostrado que anticuerpos IgA secretorios antiamebianos pueden bloquear la adherencia de trofozoitos de E. histolytica a células de líneas de cultivo. En relación con la definitiva función protectora de los anticuerpos IgA secretorios anti -E. histolytica, se deben tener en cuenta dos aspectos adicionales: la ausencia de evidencias en favor de que la amebiasis intestinal es más frecuente o más severa en individuos con déficit de IgA; y la demostración, in vitro, de que los trofozoitos de E. histolytica degradan, por intermedio de sus proteasas, la IgA secretoria humana. Respuestas inmunitarias mediadas por células Desde una perspectiva epidemiológica, los argumentos sobre el papel de las respuestas inmunitarias celulares en la protección contra la invasión amebiana son contradictorios. En ese sentido, las evidencias más fuertes en favor de una participación significativa de este tipo de respuestas provienen de reportes sobre complicaciones severas en pacientes de amebiasis que han recibido tratamiento con drogas corticoesteroides. La inexistencia de informes sobre un incremento significativo de la incidencia de amebiasis en pacientes de SIDA en áreas donde ambas entidades son endémicas es el principal argumento en contra. Sin embargo, estudios in vitro parecen demostrar la existencia de mecanismos protectores mediados por células. Linfocitos T de individuos con absceso hepático amebiano que han rebasado la fase aguda de la enfermedad, desarrollan respuestas proliferativas cuando son estimulados con
- 31. antígenos de E. histolytica. La capacidad de las células mononucleares de fagocitar y eliminar trofozoitos de E. histolytica se incrementa cuando las mismas son puestas en contacto con sobrenadantes de cultivos linfocitarios estimulados con antígenos amebianos. En línea con lo anterior, las linfoquinas detectadas en dichos sobrenadantes fueron el interferón gamma (INF-g), la interleuquina 2 (IL-2) y el factor de necrosis tumoral beta (TNF-a, del inglés: tumour necrosis factor beta), que corresponden a un patrón de respuestas Th1. Finalmente, células T CD8+ de personas que fueron tratadas por un absceso hepático tienen actividad citotóxica sobre los trofozoitos amebianos. Desde luego, en este último caso queda por explicar el mecanismo por el que se produciría la lisis en ausencia de expresión de antígenos clase I del complejo mayor de histocompatibilidad (MHC, del inglés: major histocompatibility complex) en la superficie de los trofozoitos de E. histolytica. Mecanismos de evasión de E. histolytica La relativa ineficiencia de los mecanismos defensivos del hospedero contra la infección por E. histolytica, que es más manifiesta en las primeras fases de esta, ha conducido a la consideración de que este protozoo desarrolla mecanismos evasivos de las respuestas inmunitarias que son los siguientes: 1. Hipersecreción de glicoproteínas alteradas por las células de Goblet. 2. Degradación de la IgA secretoria. 3. Recambio antigénico de E. histolytica. 4. Lisis de células inflamatorias. 5. Inmunodepresión del hospedero. 6. Evasión de los efectos derivados de la activación del sistema del complemento. Formas clínicas de la amebiasis El espectro clínico de la amebiasis es amplio, como consecuencia de las muy diferentes formas de interacción hospedero-parásito que pueden establecerse cuando el humano es infectado por E. histolytica (cuadro 84.6). Cuadro 84.6. Formas clínicas de la amebiasis intestinal sintomática
- 32. Amebiasis intestinal asintomática En casi la totalidad de los estudios reportados, 90 % o más de los individuos infectados por E. histolytica son asintomáticos. Los portadores sanos representan la principal fuente de diseminación de la infección y, en dependencia de la relación hospedero-parásito que se establezca, pueden evolucionar hacia el cese espontáneo de la eliminación de quistes en las heces o al desarrollo de una de las formas de amebiasis sintomática. Amebiasis intestinal sintomática La amebiasis intestinal sintomática es consecuencia de la invasión de la pared del colon, en uno o más de sus segmentos, por trofozoitos de E. histolytica. Su período de incubación es en extremo variable, y su duración depende, entre otros factores, del inóculo infectante, de las oportunidades de reinfección y de las características particulares de la relación hospedero-parásito que se desarrolle. De manera general, puede ser tan breve como de 2 a 5 días, o tan prolongado como de 1año. La mayoría de los autores coincide en que las formas de presentación de la amebiasis intestinal sintomática son dos: colitis amebiana disentérica y colitis amebiana no disentérica. Estas formas clínicas pueden dar lugar a complicaciones de mayor gravedad. Colitis amebiana disentérica Esta forma de presentación de la amebiasis intestinal sintomática se puede observar en todos los grupos de edades, pero su incidencia es más alta en niños menores de 5 años. Tres son las manifestaciones clínicas que la caracterizan: diarreas mucosanguinolentas, cólicos intestinales y tenesmo rectal. Al comienzo de los síntomas, las deposiciones pueden ser poco numerosas, abundantes y de consistencia blanda o francamente diarreicas. A medida que la enfermedad progresa, lo cual suele ocurrir con rapidez, las evacuaciones se tornan muy frecuentes (10 o más en el día), de poco volumen y están constituidas principalmente por moco y sangre. El examen endoscópico de la mucosa del colon realizado en este momento suele revelar la presencia de las típicas úlceras amebianas, muchas veces sangrantes y en ocasiones recubiertas por una secreción amarillenta. Los cólicos intestinales preceden, y en ocasiones acompañan, al acto de la defecación. Estos dolores espasmódicos suelen ser de intensidad leve a moderada, de aparición y desaparición rápidas, y se pueden localizar en cualquier punto del marco cólico. A veces, el dolor también puede ser continuo. Ocurre con relativa frecuencia que, después de una defecación, la musculatura del recto permanece contraída y le crea al paciente la necesidad de una nueva evacuación, sin que la misma
- 33. se produzca. Este síntoma, el llamado tenesmo rectal, tiene una importante significación semiológica. En los niños, cuando la disentería se prolonga, se puede producir atonía de los músculos perineales y relajación del esfínter anal, acompañado de rectitis, lo que muchas veces da lugar a un prolapso rectal. Al realizar el examen físico el paciente puede sentir durante la palpación del abdomen dolor, que es difuso o localizado en uno de sus cuadrantes, más frecuentemente el inferior derecho, y se puede auscultar un aumento de los ruidos hidroaéreos. Sin tratamiento, la evolución de la colitis amebiana disentérica es variable. Depende, entre otros factores, de la edad y condiciones del hospedero, y de la virulencia de la cepa de E. histolytica presente. Algunos casos curan espontáneamente, otros pasan a una forma de colitis amebiana no disentérica y los de peor evolución sufren de alguna de las complicaciones de la amebiasis intestinal, a las que nos referiremos más adelante. Con el tratamiento adecuado, los síntomas desaparecen rápidamente. Colitis amebiana no disentérica La colitis amebiana no disentérica, también llamada por algunos colitis amebiana crónica, es la forma más comúnmente observada de amebiasis intestinal sintomática. Al examen endoscópico, la mucosa del colon se observa edematosa y, en ocasiones, también se pueden observar las úlceras amebianas. Está caracterizada por la presencia de síntomas de colitis, sin que se desarrolle el cuadro disentérico clásico. La colitis no disentérica puede ser la forma de presentación inicial de la infección amebiana o, menos frecuentemente, una fase evolutiva de la colitis disentérica. Las manifestaciones clínicas que de manera protagónica caracterizan la colitis amebiana no disentérica son dos: cambios en el ritmo de defecación y dolor abdominal. Al examen físico, y sobre todo en los períodos en los que el paciente presenta diarreas y dolor abdominal, con mucha frecuencia aparece dolor a la palpación del abdomen y aumento de los ruidos hidroaéreos. Como en el caso de la colitis disentérica y por los mismos factores, la evolución de la forma no disentérica es variable. Sin tratamiento, algunos individuos curan espontáneamente, otros evolucionan tórpidamente, con períodos de crisis y etapas de aparente bienestar, y los menos sufren de alguna de las complicaciones de la amebiasis intestinal sintomática. También en los pacientes de colitis amebiana no disentérica se logra la rápida desaparición de los síntomas con el tratamiento adecuado. Complicaciones de la amebiasis intestinal sintomática La amebiasis intestinal sintomática, en cualesquiera de sus dos presentaciones habituales, puede evolucionar hacia formas clínicas más complejas que, en general, comprometen en mayor grado la
- 34. vida del paciente. Estas complicaciones son, entre otras menos frecuentes, la colitis fulminante, las perforaciones intestinales, el ameboma y la apendicitis amebiana. 1. Colitis fulminante: también llamada colitis necrosante, aunque relativamente rara, es la complicación más grave de la amebiasis intestinal sintomática. Ocurre entre 6 y 10 % de los pacientes con infección invasiva y es más frecuente en niños. El examen endoscópico de la mucosa del intestino grueso de estos pacientes permite observar extensas zonas de lesiones ulceronecróticas. La confluencia de estas lesiones puede llevar a la necrosis total de esta víscera. En este último caso nos estamos refiriendo al megacolon tóxico, la forma de colitis necrosante de peor pronóstico. Desde el punto de vista clínico, cinco manifestaciones caracterizan esta complicación de la amebiasis intestinal sintomática: diarrea sanguinolenta, dolor abdominal, tenesmo rectal, fiebre y marcada toma del estado general. El examen físico permite encontrar distensión e hiperestesia notables en la región abdominal y, en la mayoría de las ocasiones, la auscultación revela ausencia de ruidos hidroaéreos. Con y sin tratamiento, la mortalidad por colitis fulminante es de casi 100 %. 2. Peritonitis por perforación intestinal: uno de los primeros síntomas de esta complicación, y para muchos autores el más constante, es la distensión abdominal, la cual se manifiesta por abombamiento, timpanismo y, en muchas ocasiones, borramiento de la matidez hepática. Un segundo elemento característico de las perforaciones es la atonía del esfínter rectal, lo que se expresa en salida espontánea del contenido intestinal, generalmente moco y sangre en volúmenes variables. En estos pacientes la temperatura llega a elevarse hasta los 40 °C, o más. No obstante, la ausencia de fiebre, e incluso la hipotermia, no debe descartar el diagnóstico, pues en los casos más graves el individuo puede presentarse en estado de choque. El paciente se queja de dolor abdominal intenso, sin localización preferente, y, al examen físico, se evidencia una fuerte resistencia muscular a la palpación profunda. Vómitos, deshidratación y un notable estado de toxemia completan el cuadro de abdomen agudo por peritonitis. Como en el caso de la colitis fulminante, las perforaciones intestinales son de muy mal pronóstico y casi la totalidad de los pacientes, con tratamiento médico y sin este, evolucionan rápidamente hacia la muerte. 3. Ameboma: el ameboma, una complicación que se presenta en 1 % de los pacientes de amebiasis intestinal, es el resultado de la producción excesiva de tejido de granulación en respuesta a la invasión de la pared del colon por E. histolytica. Al examen endoscópico, esta lesión, también llamada granuloma amebiano, suele ser observada como una masa tumoral de color rojo intenso, que sangra con facilidad y que tiende a obstruir la luz intestinal. Radiológicamente, el ameboma simula un adenocarcinoma. Desde el punto de vista clínico, los amebomas pueden presentarse de una manera aguda, que es lo regular, o crónica. Con mucha menor frecuencia, también pueden ser asintomáticos. En este último caso, son detectados mediante palpación abdominal o por exámenes radiológicos realizados con otros fines.
- 35. Las manifestaciones clínicas, cuando las hay, corresponden a un cuadro de colitis, que puede ser disentérica o no. Al examen físico, se detecta la presencia de una masa palpable en la región abdominal correspondiente. Cuando la lesión se localiza en el segmento más distal del intestino grueso, esta puede ser detectada mediante tacto rectal. Aunque el ameboma tiende a estrechar la luz intestinal, síntomas y signos por obstrucción de este órgano son excepcionales. Sin tratamiento, la evolución de los pacientes de amebomas es incierta. Unos pasan a formas crónicas en las que se alternan períodos de diarreas, no siempre disentéricas, con fases de contispación; otros evolucionan a otras complicaciones más graves. Con el tratamiento adecuado, la masa tumoral se reduce y los pacientes suelen curar sin secuelas. Apendicitis amebiana: es una complicación infrecuente de la amebiasis intestinal, resultado de la invasión del apéndice ileocecal por trofozoitos de E. histolytica. Histológicamente, está caracterizado por inflamación, necrosis y, en los casos más graves, perforación de este órgano. Las manifestaciones clínicas de la apendicitis amebiana son similares a las de causa bacteriana. No obstante, dado que en la mayor parte de los casos coexisten úlceras amebianas, generalmente en el ciego, las diarreas mucosanguinolentas también pueden estar presentes. De hecho, la denominación más correcta en estos casos es la de tifloapendicitis amebiana. Sin tratamiento, la evolución de la complicación apendicular es generalmente fatal. El éxito del tratamiento depende, como en el caso de apendicitis de otras causas, de cuán temprano este se instaure, de la coexistencia y gravedad de úlceras amebianas en otras regiones del intestino grueso, y del estado general del paciente. Amebiasis extraintestinal El absceso hepático es la más frecuente de las lesiones extraintestinales de la amebiasis invasiva. La diseminación a sitios extrahepáticos, a cuyos aspectos fundamentales también nos referiremos posteriormente, puede ocurrir por ruptura (a peritoneo, estómago, duodeno, vías biliares, colon, pleura, pulmón, pericardio y mediastino), por continuidad (a pared abdominal y piel) y por vía hematógena (a cerebro). Absceso hepático amebiano Aunque el absceso hepático amebiano puede presentarse a cualquier edad y en ambos sexos, es más frecuente en adultos masculinos. Cuando se presenta en niños, ocurre sobre todo en la edad preescolar y con frecuencias parecidas en hembras y varones. Por otro lado, el absceso hepático amebiano puede aparecer sin historia reciente de infección intestinal y en ausencia del parásito en las heces del paciente. En general, se considera que tiene dos formas de presentación. Presentación aguda. El dolor, de aparición brusca e intensidad variable, es un síntoma siempre presente en esta forma de comienzo del absceso amebiano del hígado. Otras características semiológicas de este dependerán del número (regularmente uno), tamaño y ubicación de los abscesos.
- 36. Los abscesos que se ubican en el lóbulo hepático derecho producen dolor en el hipocondrio derecho, que puede irradiarse a hombro y regiones escapular y subescapular del mismo lado. Este dolor suele intensificarse con la respiración profunda, la tos, la posición de decúbito lateral derecho y al apoyar la pierna derecha durante la marcha. Los abscesos de esta localización también pueden dar lugar a dolor de tipo pleural. En ocasión de abscesos del lóbulo izquierdo del hígado, los pacientes aquejan dolor en el epigastrio, que puede irradiarse a las regiones retroesternal y precordial y, más raramente, al hombro izquierdo. También en los abscesos de este lóbulo hepático, el dolor se puede incrementar con la tos y, menos frecuentemente, con la respiración profunda. La fiebre es otro síntoma siempre presente en la forma aguda del absceso hepático amebiano. Esta, que suele acompañarse de escalofríos, alcanza cifras entre 38 y 40 °C, sobre todo durante la tarde y la noche. Los pacientes de absceso hepático amebiano sufren tos seca e irritante, en particular cuando este se ubica en el lóbulo derecho. Otros síntomas, no siempre presentes, contribuyen a completar el cuadro: anorexia, náuseas, vómitos y diarreas. Al examen físico, todos los pasos de la exploración del abdomen del paciente conducen a demostrar el signo más importante del absceso hepático amebiano: una hepatomegalia dolorosa. La inspección puede hacer evidente una zona de edema o una elevación localizada de la caja torácica, sugestiva de un absceso hepático subyacente. A la palpación, la sensibilidad hepática está aumentada y puede ser demostrada la expansión del hígado, como una masa suave, por debajo del reborde costal derecho. La percusión suele ser dolorosa y a la auscultación, en el caso de los abscesos en la parte superior del lóbulo derecho, se puede encontrar indicios de compresión de la base pulmonar derecha, que es confirmada por las radiografías de tórax que muestran al diafragma desplazado hacia arriba, consecuencia de la presión ejercida sobre él por el hígado aumentado de tamaño. La presencia de ictericia, que aparece en menos de 10 % de los pacientes, es más frecuente en los casos de mayor gravedad y debe conducir a la sospecha de abscesos hepáticos múltiples. Presentación subaguda. La forma de presentación subaguda del absceso hepático amebiano, considerada menos común por los autores que la describen, se caracteriza por una incorporación gradual, en semanas o meses, de los síntomas y signos que conformarán el cuadro florido de la enfermedad. Sin el tratamiento adecuado y oportuno, la evolución de los pacientes de absceso hepático amebiano es generalmente desfavorable, pues suelen progresar hacia complicaciones graves, tales como diseminación extrahepática de la infección amebiana, sobreinfección bacteriana del absceso e insuficiencia hepática grave. La evolución es más desfavorable en los niños, de manera particular en los menores de 2 años y en los desnutridos. Otras localizaciones extraintestinales de la infección por E. histolytica
- 37. 1. Amebiasis pleuropulmonar: cuando el absceso amebiano se localiza próximo a la cara diafragmática del hígado, pueden afectarse estructuras en el interior de la caja torácica. Los mecanismos por los que dicha afectación se podría producir son dos: una respuesta inflamatoria por contigüidad, en ausencia de amebas, en dichas estructuras, y una apertura del absceso hacia las mismas. La respuesta inflamatoria pleuropulmonar, en ausencia de amebas, puede dar lugar a pleuresías serosas y a zonas de atelectasia. Clínicamente, estas lesiones se traducen en dolor pleurítico, con irradiación a hombro y, en ocasiones, a toda la región dorsal, tos irritante y disnea. Por lo general, el cuadro desaparece con relativa rapidez con el tratamiento adecuado del absceso hepático amebiano. La apertura más frecuente de un absceso hepático amebiano es hacia un bronquio, sin afectación protagónica del tejido circundante. Los síntomas iniciales de la apertura hacia bronquios son: dolor pleurítico, tos irritante, disnea y esputos hemoptoicos. Posteriormente, con la ruptura y canalización del contenido del absceso, la expectoración se hace rápidamente profusa y, por su volumen, puede llegar a constituir una vómica. En el material expectorado se suelen encontrar trofozoitos de E. histolytica. La salida del material de un absceso a través de un bronquio proporciona al paciente un medio natural de drenaje que, en muchos casos, facilita o acelera su curación, pero, en otros, puede causar la muerte por asfixia debido a la invasión masiva de las vías respiratorias. Esta última eventualidad, como veremos más adelante, es relativamente frecuente en niños. Si la apertura se produce hacia el parénquima pulmonar, lo cual casi nunca sucede, se suele formar un absceso en este órgano, cuyas manifestaciones clínicas dependerán de la existencia o no de comunicación bronquial. El empiema amebiano, la forma pleuropulmonar de menor frecuencia y de mayor gravedad, se caracteriza por la instalación súbita de un cuadro de distress respiratorio y dolor torácico. Su evolución depende del volumen del derrame y de la existencia de comunicación bronquial. Si se logra realizar drenaje oportuno, los pacientes pueden resolver con el correspondiente tratamiento antiamebiano. 2. Amebiasis pericárdica: la afectación del pericardio, aunque rara, es la más grave complicación de un absceso hepático amebiano. Por lo general, la apertura hacia la cavidad pericárdica es precedida de una fase en que se produce una efusión serosa y libre de amebas, que es consecuencia de una respuesta inflamatoria de los tejidos circundantes al absceso amebiano cercano. Este período se caracteriza por fiebre y dolor abdominal, que progresivamente se hace torácico. Cuando ocurre la apertura hacia la cavidad pericárdica, las manifestaciones se hacen más floridas, y a la fiebre y el dolor torácico se pueden agregar una disminución de la intensidad de los ruidos cardíacos, ingurgitación yugular, frote pericárdico y edema de miembros inferiores. En los casos más graves puede ocurrir taponamiento cardíaco y choque. 3. Amebiasis peritoneal por ruptura de absceso hepático: como forma evolutiva de un absceso hepático, la amebiasis peritoneal ocupa el segundo lugar en orden de frecuencia (ocurre en 2 a 7 % de los casos). De manera general, se produce ruptura hacia la cavidad
- 38. peritoneal de uno o más abscesos situados en la cara inferior de uno o ambos lóbulos hepáticos, lo que da lugar al desarrollo de un cuadro de peritonitis. Con los tratamientos actuales, la mortalidad por esta complicación ha quedado reducida a menos de 20 % de los casos. 4. Amebiasis cerebral: la localización cerebral de la amebiasis invasiva es muy rara. La lesión característica suele ser un absceso en la corteza cerebral de tamaño variable, que pocas veces rebasa los 5 cm de diámetro. Las manifestaciones clínicas de la amebiasis cerebral dependen del sitio y tamaño de la lesión y, en general, se corresponden con las de una masa que ocupa espacio y comprime las estructuras vecinas. La evolución de estos pacientes muchas veces es desfavorable debido a que con poca frecuencia se piensa oportunamente en la amebiasis cerebral como posibilidad diagnóstica, de modo que cuando se instaura el tratamiento específico ya se han producido daños irreversibles. 5. Amebiasis cutánea: la invasión de la piel por E. histolytica es también un evento poco frecuente. La amebiasis cutánea puede ser primaria, cuando se produce en ausencia del parásito en otra localización, o secundaria, cuando ocurre por extensión de la infección desde otros tejidos. En general, la amebiasis cutánea primaria, observada casi siempre en la región genital, puede asumir dos formas clínicas: úlceras cutáneas y lesiones vegetantes. Las úlceras cutáneas son lesiones agudas, muy dolorosas, de forma serpiginosa y de bordes elevados y enrojecidos. El fondo de las mismas siempre es húmedo, con material necrótico y pus. Su evolución suele ser tan rápida y destructiva, que se han reportado casos de destrucción completa del pene y de invasión vaginal y del cuello uterino. Por sus características, estas úlceras remedan lesiones carcinomatosas. Las lesiones vegetantes son proliferaciones hísticas, por lo general precedidas por zonas de ulceración, que evolucionan crónicamente. Estas lesiones suelen sangrar con facilidad y se localizan con regularidad en un borde o pliegue mucocutáneo, que en ocasiones se encuentra indemne en apariencia. La amebiasis cutánea secundaria se puede producir de dos maneras: la diseminación de la infección intestinal al ano y a la piel que lo rodea, lo que da lugar al desarrollo de úlceras perianales y perineales, de bordes irregulares y tamaño variable, de las cuales el elemento clínico protagónico es el intenso dolor; y la fistulización de un absceso amebiano, en cuyo caso la piel puede infectarse en el lugar de salida. El pronóstico de los casos de amebiasis cutánea depende de la edad y estado general del paciente, de la forma clínica de la lesión y, sobre todo, de cuán temprano se haya realizado el diagnóstico de la misma y, en consecuencia, administrado el tratamiento adecuado. Cuando esto último ocurre oportunamente, suele haber recuperación completa de las lesiones. Diagnóstico de la amebiasis Diagnóstico de la amebiasis intestinal asintomática
- 39. La amebiasis intestinal asintomática, en sentido estricto, es la forma de esta parasitosis presente en individuos que, sin tener manifestaciones clínicas atribuibles a enfermedad amebiana, eliminan en sus heces quistes o trofozoitos de E. histolytica. A la luz de los conocimientos actuales, que demuestran que los quistes de E. histolytica y E. dispar son microscópicamente indistinguibles, el diagnóstico de esta forma de amebiasis solo se puede hacer si se dispone de uno o más procedimientos complementarios. Si esto no fuera posible, el hallazgo microscópico de los quistes solo permite suponer la presencia de una o ambas especies del complejo E. histolytica/E. dispar, y de ninguna manera permite establecer el diagnóstico de amebiasis intestinal asintomática. El hallazgo de trofozoitos amebianos en las heces de un individuo asintomático es un evento muy poco frecuente. Cuando en las heces de una persona asintomática se han encontrado amebas con las características morfológicas del complejo E. histolytica/E. dispar y no se dispone de uno de los procedimientos que permiten precisar la especie presente, la búsqueda de anticuerpos antiamebianos en suero, en saliva o en heces y la detección de hemoglobina humana en heces son exámenes complementarios de utilidad. La presencia de anticuerpos antiamebianos en los fluidos mencionados es indicativo de infección presente o pasada por E. histolytica (un resultado negativo no niega la infección por esta especie, pues en la mayoría de los casos de amebiasis intestinal asintomática no se producen estos anticuerpos). La ausencia de sangre oculta en heces microscópicamente positivas sugiere fuertemente que no es E. histolytica la especie presente (un resultado positivo no confirma la infección por E. histolytica, pues puede estar presente otro tipo de lesión intestinal sangrante). Diagnóstico de la amebiasis intestinal sintomática La amebiasis intestinal sintomática se sospecha por la presencia de los síntomas y signos relacionados con alguna de sus formas de presentación (ver acápite “Amebiasis intestinal sintomática”); y el diagnóstico se confirma mediante la realización de los exámenes complementariosque directa o indirectamente demuestran la presencia del parásito. La observación microscópica de muestras seriadas de heces, que puede incluir la realización de procedimientos suplementarios, como técnicas de concentración y de coloración especiales, es el examen complementario más utilizado para el diagnóstico de la amebiasis intestinal. La presencia de trofozoitos móviles con las características morfológicas de E. histolytica y con eritrocitos fagocitados permite establecer el diagnóstico de amebiasis. Por otro lado, el hallazgo de trofozoitos no hematófagos y de quistes con las características microscópicas de E. histolytica no confirma dicho diagnóstico. La observación de estas estructuras solo permite suponer la presencia de una o ambas especies del complejo E. histolytica/E. dispar. En estos casos, se debe emplear alguno de los procedimientos que permiten la identificación precisa de la especie presente. Si no se dispone de una de estas pruebas, se deben tener en cuenta otros exámenes complementarios y elementos epidemiológicos.
- 40. Cuando las características del paciente hacen pensar en una de las formas de amebiasis intestinal y el estudio de muestras fecales no ha permitido arribar a un diagnóstico definitivo, la realización de estudios endoscópicos de colon y recto puede aportar nuevos elementos. Estos exámenes permiten la obtención de muestras de heces en la luz intestinal, la observación de la mucosa de ese órgano en busca de posibles lesiones y la toma de tejidos de las mismas para posterior análisis anatomopatológico. El cultivo in vitro de E. histolytica a partir de muestras fecales puede ser empleado en el estudio de un paciente. Sin embargo, los inconvenientes de esta prueba, le restan utilidad diagnóstica. La presencia de anticuerpos antiamebianos en suero, en saliva o en heces solo es indicio de infección actual o pasada por E. histolytica. La detección de hemoglobina humana en las heces de los pacientes en los que se trata de establecer el diagnóstico de amebiasis intestinal sintomática, es un procedimiento complementario de utilidad cuando no se ha podido precisar la especie amebiana presente en las heces. Como en los casos asintomáticos, la ausencia de sangre oculta en las muestras fecales microscópicamente positivas a E. histolytica/E. dispar sugiere que la primera no es la especie presente (un resultado positivo no confirma la infección E. histolytica, pues otro tipo de lesión intestinal sangrante puede estar presente). Excepto la radiografía de colon contrastada con bario, de utilidad en los casos de amebomas (Fig. 84.18), los estudios imagenológicos son poco empleados. Fig. 84.18. Ameboma. Se observa la estrechez de la luz intestinal. Cuando se sospecha un cuadro de amebiasis intestinal sintomática, y la realización de uno o más procedimientos complementarios no ha permitido demostrar la infección por E. histolytica, o cuando dichos exámenes no están disponibles, algunos elementos epidemiológicos pueden ser de utilidad diagnóstica. En ese sentido, una historia de contacto estrecho del paciente-problema con un caso de amebiasis invasiva o la estadía de este en un área geográfica endémica o en una institución cerrada, donde existan evidencias del desarrollo de una epidemia de amebiasis, son datos de mucho interés. Lesiones de colon y recto de muy variada naturaleza pueden manifestarse por un síndrome disentérico y, en consecuencia, deben ser tenidas en cuenta cuando se estudia un posible caso de colitis disentérica de causa amebiana. La colitis amebiana debe ser diferenciada de las colitis bacterianas causadas por Shigella, Salmonella, Campilobacter, Vibrio, Escherichia coli enteroinvasiva y Yersinia enterocolitica. En general, la diferenciación se debe realizar mediante la indicación de coprocultivos bacterianos y de los exámenes complementarios que permiten el diagnóstico positivo de amebiasis intestinal.
- 41. Otro grupo de enfermedades infecciosas que se deben diferenciar de la disentería amebiana son las parasitarias. Al menos tres de estas pueden causar síndrome disentérico: tricocefalosis, balantidiosis y esquistosomosis. En estos casos, los exámenes coproparasitológicos resuelven regularmente el problema diagnóstico. Entre las enfermedades no infecciosas que evolucionan con colitis y diarreas se debe hacer diferenciación con la colitis ulcerativa idiopática, los adenocarcinomas de colon sigmoides y recto, y la polipolisis colorrectal, entre otras. En estos casos, los exámenes endoscópicos, con toma de muestras para estudios histopatológicos de las lesiones, permiten llegar al diagnóstico sin muchas dificultades. De las formas clínicas de amebiasis intestinal, son los amebomas los que con más frecuencia deben ser diferenciados de otras enfermedades de colon y recto, como adenocarcinomas de esos segmentos intestinales, granulomas tuberculosos y linfogranulomas venéreos. Diagnóstico de la amebiasis extraintestinal Diagnóstico del absceso hepático amebiano El absceso hepático amebiano se sospecha por la presencia de los síntomas y signos que caracterizan a una de sus formas de presentación (ver acápite “Absceso hepático amebiano”), y el diagnóstico se confirma mediante la realización de los exámenes complementarios que directa o indirectamente demuestran la presencia del absceso y la causa amebiana de este. De estos estudios, los más eficaces son los estudios imagenológicos y la detección sérica de anticuerpos antiamebianos. Entre los primeros, los más empleados en el diagnóstico de esta forma de amebiasis extraintestinal son las radiografías de tórax y abdomen (Fig. 84.19), la ultrasonografía (Fig. 84.20) y la tomografía axial computarizada (Fig. 84.21). Fig. 84.19. Absceso hepático. Véase la elevación del hemidiafragma derecho. Fig. 84.20. Absceso hepático. Se aprecia la zona de baja ecogenicidad.
- 42. Fig. 84.21. Absceso hepático. Se observa el área hipodensa del lóbulo derecho. La detección de anticuerpos séricos antiamebianos, sobre todo en individuos que no viven en áreas endémicas de amebiasis, es una herramienta de mucha utilidad para el diagnósti co de las formas invasivas de esta parasitosis. Esta consideración tiene mayor alcance en los pacientes de alguna forma de amebiasis extraintestinal, en los que los anticuerpos anti -E. histolytica séricos están presentes en más de 95 % de los casos. Las pruebas ELISA, por su eficacia y por ser las primeras que ofrecen resultados positivos (antes de haber transcurrido 10 días de comenzados los síntomas), son los procedimientos más eficientes para el diagnóstico. La aspiración percutánea del contenido de un absceso hepático con fines diagnósticos es cada vez más rara. La observación microscópica de muestras seriadas de heces no tiene utilidad para el diagnóstico de un absceso hepático amebiano. En casi la totalidad de las series reportadas, E. histolytica solo está presente en las heces de menos de 15 % de los casos de absceso hepático estudiados. Con más frecuencia, el absceso hepático amebiano se debe diferenciar de otras enfermedades que produzcan hepatomegalia dolorosa, como abscesos piógenos, quistes congénitos infectados, quistes hidatídicos, hepatitis virales y tumores, y de otras parasitosis que afectan el hígado y evolucionan con fiebre, como la malaria y la fasciolosis. De estas, los diagnósticos diferenciales más complejos son los abscesos piógenos y, en menor medida, la fasciolosis. Diagnóstico de la amebiasis en otras localizaciones extraintestinales Excepto en algunos casos de amebiasis cutánea, la diseminación de la infección por E. histolytica a localizaciones extraintestinales y extrahepáticas es casi siempre una complicación de un absceso hepático. Por este motivo, con la excepción mencionada, la conducta diagnóstica ante posibles casos de amebiasis en dichas localizaciones debe incluir la detección de un absceso hepático de base. Tratamiento de la amebiasis Drogas con actividad antiamebiana Las drogas antiamebianas, en mayor o menor grado, actúan contra los trofozoitos de E. histolytica y, en general, son incapaces de penetrar la pared de los quistes. En los casos de amebiasis intestinal, en los cuales se generan quistes que pueden ser observados al examen microscópico, la desaparición de estos de las heces después de un tratamiento se debe a la acción de la droga empleada sobre las formas trofozoíticas que los originan y no a un efecto directo sobre ellos. En dependencia de los sitios anatómicos donde ejercen su acción, los fármacos antiamebianos se clasifican en tres grupos: amebicidas de acción luminal, amebicidas de acción principalmente hística y parcialmente luminal, y amebicidas de acción exclusivamente hística (cuadro 84.7). Cuadro 84.7. Drogas con actividad antiamebiana
