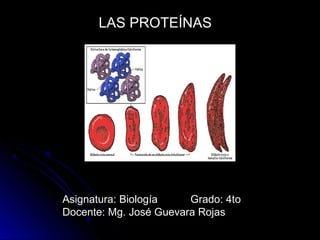
Las proteínas: componentes esenciales de los seres vivos
- 1. LAS PROTEÍNAS Asignatura: BiologíaAsignatura: Biología Grado: 4toGrado: 4to Docente: Mg. José Guevara RojasDocente: Mg. José Guevara Rojas
- 2. Proteínas: El término propuesto por J. Berzelius deriva del griego proteicos, que significa primero. Moléculas complejas, variadas y formadas básicamente por C, H, O, N, aunque algunas también contienen S y P y otras Fe, Zn o Cu. Componentes fundamentales de los seres vivos. Descubiertas en 1838, y suponen más del 50% del peso seco de los animales. Químicamente son polímeros de aminoácidos.
- 3. LOS AMINOÀCIDOS: La unión de aminoácidos, mediante enlaces peptídicos da origen a péptidos. Una cadena de aminoácidos forma un poli péptido. En la naturaleza existen unos 300 aminoácidos. De ellos, solo veinte forman parte de las proteínas. Solo diez se consideran aminoácidos esenciales para el ser humano, que los incorpora a través de su dieta. Los seres vivos construimos una variedad casi infinita de proteínas con un "alfabeto" de veinte aminoácidos. Serán diferentes tanto si varía el número de cada aminoácido como si cambia su ubicación.
- 4. Por su Función Estructurales El colágeno, que forma huesos, tendones, ligamentos y cartílagos. La queratina, componente de pelos, uñas, cuernos. La elastina de la piel. De reserva Almacenan materiales y energía. La ovoalbúmina de clara de huevo que proporciona fuente de aminoácido para embriones en desarrollo. Caseína de la leche De defensa Los anticuerpos que las infecciones. El veneno de la serpiente. De transporte La hemoglobina, que lleva oxigeno y trae el CO2 Contráctiles Actina y miocina, presentes en las células musculares. Reguladoras Hormonas, que regulan procesos metabólicos como insulina que regulan cantidad de azúcar en la sangre. Catalíticas Las enzimas, catalizadores bioquímicos
- 5. Por su composición Fosfoproteínas Glicoproteínas Cromoproteínas Lipoproteínas Nucleoproteínas Compuestas Simples Globulares Fibrosas Albúminas.- Globulinas Luteínas.- Histonas Prolaminas.- Protaminas Hormonas.- Enzimas Queratina.- Colágeno Elastina.- Fibroínas
- 6. PROTEÍNAS GLOBULARES Son esféricas y solubles. Desempeñan función dinámica en el metabolismo corporal. Ejemplos: albúmina, globulina, caseína, hemoglobina, todas las enzimas y las hormonas proteicas. Albúminas y globulinas son proteínas solubles abundantes en las células animales, el suero sanguíneo, la leche y los huevos. La hemoglobina es una proteína respiratoria que transporta oxígeno por el cuerpo; a ella se debe el color rojo intenso de los eritrocitos.
- 7. Enzimas Proteínas globulares que se combinan con otras sustancias, llamadas sustratos, para catalizar las numerosas reacciones químicas del organismo. Son responsables del metabolismo y de su regulación Hormonas proteicas Segregadas por glándulas endocrinas, estimulan a ciertos órganos fundamentales que inician y controlan actividades importantes, como el ritmo metabólico o la producción de enzimas digestivas y de leche. La insulina, segregada por los islotes de Langerhans en el páncreas, regula el metabolismo de carbohidratos. La tiroxina, segregada por la tiroides, regula el metabolismo global; y la calcitonina, también producida en el tiroides, reduce la concentración de calcio en la sangre y estimula la mineralización ósea. Los Anticuerpos Llamados inmunoglobulinas, agrupan los miles de proteínas distintas que se producen en el suero sanguíneo como respuesta a los antígenos (sustancias u organismos que invaden el cuerpo).
- 8. Proteínas Fibrosas Colágeno: Forma parte de huesos, piel, tendones y cartílagos, es la proteína más abundante en los vertebrados. Queratina: Constituye la capa externa de la piel, el pelo y las uñas en el ser humano y las escamas, pezuñas, cuernos y plumas en los animales, se retuerce o arrolla en una estructura helicoidal regular llamada hélice a. Fibrinógeno: Proteína plasmática de la sangre responsable de la coagulación. Bajo la acción de la trombina, el fibrinógeno se transforma en fibrina (proteína insoluble), el elemento estructural de los coágulos sanguíneos o trombos. Proteínas musculares: La miocina, la principal proteína responsable de la contracción muscular, se combina con la actina, y ambas actúan en la acción contráctil del músculo esquelético y en distintos tipos de movimiento celular.
- 9. 1. ESTRUCTURA PRIMARIA Es la secuencia específica de aminoácidos que forman las cadenas polipeptídicas de la proteína. Es decir, el número, tipo y orden de colocación de sus aminoácidos. Una simple alteración en la estructura causa daños en el organismo. ARQUITECTURA DE LAS PROTEÍNAS 2. ESTRUCTURA SECUNDARIA Es el enrollamiento o plegamiento de ciertas partes del polipéptido y da origen a estructuras: Alfa hélice (enrollamiento espiral), la más común. Hoja plegada (láminas plegadas).
- 10. 3. ESTRUCTURA TERCIARIA Es la forma tridimensional de un polipéptido. Se origina por la interacción de los grupos R y obliga que la molécula se enrolle sobre sí misma, con lo que origina dos tipos de estructuras apropiadas a su función: globular soluble (enzimas) y fibrosa insoluble (queratina). 4. ESTRUCTURA CUATERNARIA Si la proteína posee más de una cadena polipeptídica o subunidad, adquiere esta estructura. Resulta de las interacciones de enlace entre las subunidades, idénticas o no. Ejemplo: la hemoglobina tiene cuatro subunidades de dos tipos diferentes.
- 11. DESNATURALIZACIÒN DE LAS PROTEÌNAS Las proteínas pueden inactivarse al romperse las fuerzas que mantienen la forma tridimensional de la cadena por acción del calor, cambios en el pH o agitación. Ejemplo: Cuando freímos un huevo, el calor desnaturaliza las proteínas de la clara, que se vuelve sólida, blanca e insoluble en agua. La leche cortada debido a la acción de los ácidos sobre la caseína. El laceado o permanente que se ofrecen en las peluquerías y que actúan por efecto del calor sobre la queratina. Importancia: Se encargan de la construcción del cuerpo humano. Son la base sobre la que se forma huesos y músculos Reponen los tejidos dañados durante la actividad diaria. Forman anticuerpos del sistema inmune. Mantenimiento de distintos tejidos corporales. Si dejamos de consumir proteínas podemos perder masa muscular. Energéticos: 1 g proteínas produce 4.1 cal
