KARBONIL
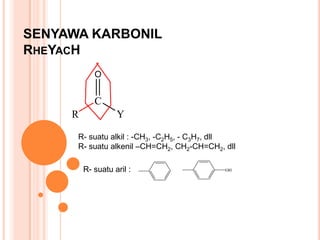
- 1. SENYAWA KARBONILRheYacH R- suatualkil : -CH3, -C2H5, - C3H7, dll R- suatualkenil –CH=CH2, CH2-CH=CH2, dll R- suatu aril :
- 2. Y bukan leaving group Y = H Gol. Aldehida Y = R’ Gol. Keton
- 3. Y leaving group -> Gol. AsamKarboksilatdanturunannya Y = OH Gol. As. Karboksilat Y = OR’ Gol. Ester Y = Gol. Anhidridaasam Y = halogen Gol. Asilhalida Y = NH2 NHR Gol. Amida NR2
- 4. KonfigurasiSenyawakarbonil Sudut-sudutikatan: R-C-O R-C-Y 120O O-C-Y Hibrida orbital = sp2 Konfigurasitrigonal planar e~ takterbagi Guguskarbonil (C=O) mengandung atom karbon sp2 yang dihubungkandengan atom oksigenolehikatanrangkapdua (1 ikatanσdan 1 ikatanπ Karenaoksigenmerupakan atom elektronegatifmakaterjadipolarisasi, dimana atom C bermuatanδ+ danoksigenδ- h Resonansi C=O akanmenghasilkan C+ dan O- Sisinukleofildari C=O Sisielektrofildari C=O
- 5. Elektrofilmasukpadasisinukleofildari C=O Nukleofilmasukpasasisielektrofildari C=O Pengaruhgugus C=O pada proton α (Hα) yaitu proton yang diikatoleh Cα Proton αolehpengaruhguguskarbonil (C=O) mudahdilepaskan, sehingga Cαdapatmembentuk ion karbonion Bentukkarbonion C(-) bertindaksebagainekleofilsehinggadapatmenyerangelektrofil
- 6. Senyawakarbonil Gol. Aldehidaddanketon Gol. As. Karboksilatdanturunannya Reaksi-reaksi yang daptberlangsungpadasenyawakarbonil: Oksidasidanreduksi (1,2) Reaksiadisinukleofilik (1) Reaksisubstitusinukleofilik (2) Reaksisubstitusiα (1,2) Reaksikondensasikarbonil (1,2)
- 7. I. Gol. Aldehiddanketon Tata namaaldehid NamaUmumNamaSistematik FolmaldehidMetanal AsetaldehidEtanal PropionaldehidPropanal 2-etil-4-metil pentanal BenzaldehidBenzenakarbaldehid Sikloheksana-karbaldehid GugusKarbaldehid Naftalena-karbaldehid
- 8. Tata namaketon NamaUmumNamaSistematik AsetonPropanon Meil, etilketonButanon Dietilketon Pentanon-3 Parakinon Sikloheksanon
- 9. Pembuatanaldehida Oksidasialkohol primer AlkoholAldehida primer Oksidator: a. KMnO4dalam H2SO4 P b. K2Cr2O7dalam H2SO4 P c. PereaksiJone’s (CrO3 + H2SO4 P) d. PCC (PiridiumChloroChromat) Keuntungan PCC” - Reaksiberjalanpadakondisilunak (yaitusuhukamar) - Rendemencukuptinggi (≥ 90%) PCC, Suatu pasta berwarnacoklat
- 10. Mekanismereaksi
- 11. Reduktif-ozonolisissuatualkena Syarat: alkenatersebutsekurang-kurangnyaharusmempunyai proton vinilik (proton yang diikatolehkarbonikatanrangkat). Contoh:
- 12. Mekanismereaksi: 3 O2elektrik charge 2 O3 OksigenOzon
- 13. 3. Reduksiturunanasamkarboksilat Reaksiumum 3.1. ReduksiRosenmund ReaksiUmum Mekanismereaksi:
- 14. 3.2. Reduksi ester olehsuatureduktorhidrida Reduktorhidrida: - LiAlH4 = Lithium AluminiumHidrida - DIBAH = DiisobutilAlumuniumHidrida Contoh :
- 15. Mekanismereaksi
- 16. Pembuatanketon Oksidasialkoholsekunder Oksidator: a. KMnO4 / H+ b. K2Cr2O7 / H+ c. CrO3 / H+ d. PCC (PiridiumChloroChromat) Contoh: PR: Tuliskanmekanismereaksinya!
- 17. Reduktif-ozonolisissuatualkena Contoh: PR: Tuliskanmekanismereaksinya!
- 18. AsilasiFriedel & Craft terhadapsenyawaaromatis AsilasiFriedel & Craft : reaksiantarasenyawaaromatisdenganasilhalida yang dikatalisisolehasamlewis AlX3menghasilkansuatuketon, yaitualkilfenilketon. Lihat Kimia Organik I, asilasi (reaksisubstitusiaromatikelektrofilik)
- 19. Mekanismereaksi Ion asiliumdanresonannyasangatreaktifterhadapnukleofil : benzen / turunanaromatik lain. Contoh: PR: Tuliskanmekanismereaksinya!
- 20. Pembuatanketonmetil Hidrasikatalitikoleh ion mercuri (Hg2+) terhadapsenyawaalkuna terminal Contoh:
- 21. Mekanismereaksi
- 22. Reaksi – ReaksiPadaAldehidadanKeton ReaksiOksidasi Aldehida Oksidator: - KMnO4 / H2SO4 - K2Cr2O7 / H2SO4 - CrO3 / H+ (jone’soksidator) - PCC Mekanismereaksimelaluistrukturhidrat!
- 24. Keton Hanyadapatdioksidasidalamkondisikerasdanmenghasilkancampuranasamkarboksilat. Untukketonsimetris: Padaoksidasiketon yang asimetris, akanterbentukcampuranproduk yang lebihbanyak. Oksidasialdehidmudahdikontrol, sedangkanoksidasiketonsukardikontrol. Aldehidalebihmudahdioksidasidibandingketonkarenagugusaldehidamengandung proton aldehida yang ternyatamudahuntukdipindahkan.
- 26. Nukleofil: - suatuspesies / rekatan yang sukaakannukleus (inti) - reaktan yang sukmuatan (+) Ada 2 jenisnukleofil: Nukleofilnetral: spesies yang mempunyai “ione-pair” elektron mis: -OH, halogen (-Cl, -Br, -I), H2O, -NH2, -SH, Nukleofilbermuatan (-) mis: -OH, Cl-, Br-, I-, -OR, H-
- 27. ReaktivitasRelatifAldehiddanKeton Aldehidalebihrelatifdibandingketon, karena 2 alasan: Alasanelektronik Aldehidlebihreaktifdibandingketonkarenatingkatpolaritasguguskarbonilaldehidalebihbesardibandingpadaketon. Sepertitelahdiketahuibahwapolarisasiguguskarbonilakanmenghasilkan atom C yang bermuatanδ+. Padaaldehida, karbokationtersebuthanyadistabilkanolehsuatugugusalkilsecarainduktif; sedangkarbokationpadaketondistabilkanoleh 2 gugusalkil. Akibatnyaaldehidmenjadikurangstabildibandingketon. Karenakurangstabil, makaaldehidakanlebihreaktif
- 28. AlasanSterik Adanya 2 gugusalkil yang bersifat “bulky” (=meruah, gemuk) padaketonmenyebabkannukleofillebihsukarmenyerang sis elektrofilguguskarbonilketon (Cδ+) dibandingpadaaldehid, dimananukleofil yang akanmasukhanyadihalangiolehsuatugugusalkilsaja. Akibatnyaaldehidalebihreaktifdibandingketon.
- 29. Jenis-jenisadisinukleofilik Reaksiadisi HCN Produknyaberupasenyawanitril R-C≡N Reaksiadisiamina Denganamina primer R-NH2, produknyaberupasenyawaimina R-CH=NH Denganaminasekunder , produknyaberupasenyawaenamina Reaksiadisihidrazine (H2N-NH2) (Reduksiwolff-Kishner), produknya: senyawaalkana R-CN3 Reaksiadisialkohol (Reaksipembentukanasetal/ketal) 5. Reaksiadisiilidafosfat (Reaksi Wittig) 6. ReaksiCanizzaro
- 30. Reaksiadisi HCN Aldehidadanketonbereaksidengan HCN menghasilkansianohidrin Karena HCN merupakanasamlemah (pKa ~ 9,1) makapadareaksidigunakancampuran HCN/KCN untukmenguatkanreaksiionisasi HCN. Sianohidrin yang terbentukselanjutnyadapatdireduksimenggunakan LiAlH4menghasilkanamina primer dandapatdihidrolisismenghasilkanasamkarboksilat. Contoh:
- 33. Reaksiadisiamina Amina primer Amina primer, R-NH2, bereaksidenganaldehidadanketon menghasilkanimina. Reaksiiniumumnyadikatalisisolehasamdanmerupakanreaksi yang reversibel. Mekanismereaksi
- 34. Aminasekunder Aminasekunder, R2-NH bereaksidenganaldehida/ketonmembentukenaminasuatuaminatakjenuh. Reaksiiniumumnyajugadikatalisisolehasam. Mekanismereaksi
- 35. Contoh: PR!! 1. 2. 3. 4.
- 36. Reaksiadisihidrazina (Reaksi Wolff-Kisher) Aldehiddanketondaptdiubahmenjadialkana yang bersesuaianbiladireaksikandenganhidrazina H2N-NH2, diikutiperlakuandenganbasakuatapasuhutinggi Contoh: Tahap-tahapreaksinya: Pembentukanintermediethidrazona Migrasiikatanrangkap yang dikatalisbasa Keluarnya gas N2 danpembentukanprodukalkana.
- 38. Contoh lain: PR!! 1. 2.
