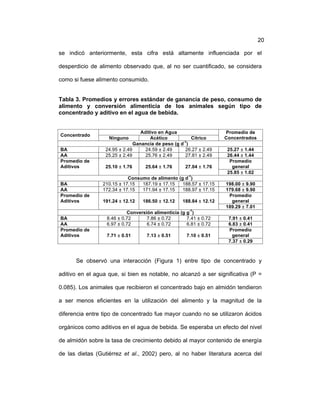
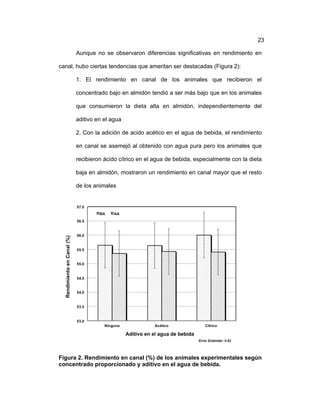
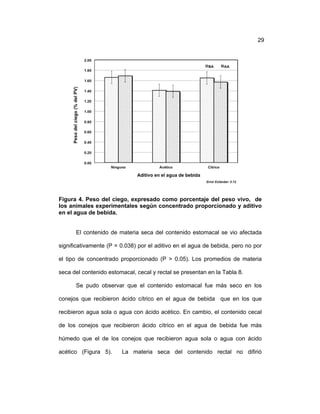
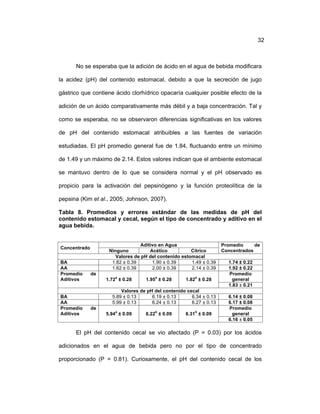
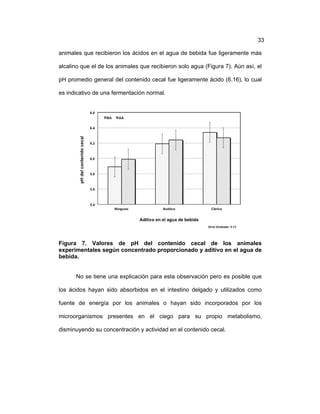
Este documento resume un estudio sobre el desempeño productivo de conejos alimentados con dietas que variaban en contenido de almidón y suplementados con ácidos orgánicos en el agua de bebida. Cuarenta y ocho conejos fueron asignados aleatoriamente a tratamientos que consistieron en dos dietas con alto o bajo contenido de almidón y la adición de ácido acético, ácido cítrico o ningún ácido al agua. Se midieron variables de desempeño, rendimiento en canal y pesos de órganos