Trabajo de quimica
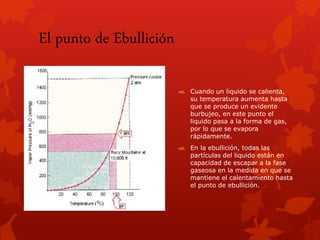
- 1. El punto de Ebullición Cuando un liquido se calienta, su temperatura aumenta hasta que se produce un evidente burbujeo, en este punto el liquido pasa a la forma de gas, por lo que se evapora rápidamente. En la ebullición, todas las partículas del liquido están en capacidad de escapar a la fase gaseosa en la medida en que se mantiene el calentamiento hasta el punto de ebullición.
- 2. Definimos el punto de ebullición como la temperatura a la cual se produce la transición de la fase líquida a la gaseosa. En el caso de sustancias puras a una presión fija, el proceso de ebullición o de vaporización ocurre a una sola temperatura; conforme se añade calor la temperatura permanece constante hasta que todo el líquido ha hervido.
- 3. El punto de fusión es la temperatura a la cual se encuentra el equilibrio de fases sólido-líquido, es decir la materia pasa de estado sólido a estado líquido, se funde. Cabe destacar que el cambio de fase ocurre a temperatura constante. El punto de fusión es una propiedad intensiva. En la mayoría de las sustancias, el punto de fusión y de congelación, son iguales. Pero esto no siempre es así: por ejemplo, el agar-agar se funde a 85 °C y se solidifica a partir de los 31 °C a 40 °C; este proceso se conoce como histéresis.
- 4. Cuando un solido se calienta su temperatura hasta que comienza a fundirse y pasa al estado liquido esto se debe a que el ordenamiento de su estructura solida comienza a ceder para pasar a un estado mas desordenado y menos rigido.