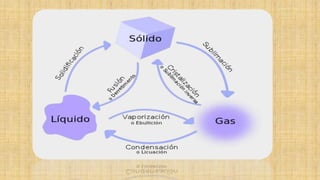
Este documento describe los diferentes tipos de cambios de estado de la materia, incluyendo la fusión, solidificación, vaporización, condensación, sublimación e ionización. Explica conceptos como el punto de ebullición y el punto de fusión, las diferencias entre ellos, y cómo se pueden representar los cambios de estado a través de curvas de calentamiento.