Tejidos
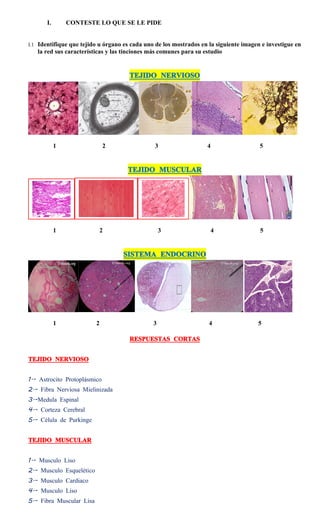
- 1. I. CONTESTE LO QUE SE LE PIDE I.1 Identifique que tejido u órgano es cada uno de los mostrados en la siguiente imagen e investigue en la red sus características y las tinciones más comunes para su estudio TEJIDO NERVIOSO 1 2 3 4 5 TEJIDO MUSCULAR 1 2 3 4 5 SISTEMA ENDOCRINO 1 2 3 4 5 RESPUESTAS CORTAS TEJIDO NERVIOSO 1.- Astrocito Protoplásmico 2.- Fibra Nerviosa Mielinizada 3.-Medula Espinal 4.- Corteza Cerebral 5.- Célula de Purkinge TEJIDO MUSCULAR 1.- Musculo Liso 2.- Musculo Esquelético 3.- Musculo Cardiaco 4.- Musculo Liso 5.- Fibra Muscular Lisa
- 2. SISTEMA ENDOCRINO 1.- Glándula Tiroides 2.- Glándula Tiroides 3.- Glándula Hipófisis 4.- Glándula Suprarrenal 5.- Páncreas
- 3. TEJIDO NERVIOSO El tejido nervioso tiene como una de sus principales funciones la coordinación de las actividades de otros tejidos del cuerpo. Está constituido por células nerviosas o neuronas altamente especializadas y por células de sostén, llamadas en conjunto células de la neuroglia. Anatómicamente el sistema nervioso se divide en sistema nervioso central (SNC) y sistema nervioso periférico (SNP). El primero está formado por el encéfalo y la médula espinal; el segundo, por los ganglios nerviosos y los nervios. Al encéfalo lo constituyen los hemisferios cerebrales, el diencéfalo, el tallo cerebral, el cerebelo y el bulbo raquídeo. 1.- Astrocito Protoplásmico Astrocitos Células en forma de estrella. Cierto número de sus prolongaciones se unen a "capilares" mientras que otras lo hacen a los cuerpos celulares de neuronas y fibras nerviosas. Las prolongaciones se caracterizan por tener puntas expandidas, los pies de astrocitos, que forman una vaina que recubre casi por completo a los capilares y que interrumpen solo las células gliales (o sus prolongaciones) de otros tipos en áreas pequeñas. Astrocito Protoplasmáticos: Se localizan en la SG poseen prolongaciones numerosas que se ramifican de manera considerable y son relativamente cortas. Las prolongaciones de los astrocitos poseen microtúbulos y también están reforzadas por haces de filamentos intermedios formados por un tipo especial de proteína, la proteína ácido fibrilar glial, estos elementos le confieren rigidez y resistencia a la tracción; suficientes para unir los cuerpos celulares y fibras nerviosas a la membrana basal que rodea a los vasos sanguíneos del SNC y les brinda sostén. El núcleo es grande ovoide y por lo general excéntrico. Su citoplasma contiene ribosomas libres y polisomas así como mitocondrias filiformes en cantidad moderada. Además de los microtubulos y filamentos intermedios mencionados posee unas cuantas cisternas de REL, Golgi y unos cuantos lisosomas.
- 4. Función de los astrocitos: 1. Regulación de la composición del medio intercelular del SNC . Captan iones K excesivos que salen de las neuronas durante la transmisión de impulsos. 2. La proximidad estrecha de sus prolongaciones con los capilares y los espacios del SNC y los alrededores de este que están llenos de líquido cefalorraquídeo sugieren la regulación de la entrada de sustancias en los espacios interneuronales. 3. Median el intercambio de nutrientes y metabolitos entre neuronas y sangre. 4. Aportan sustancias metabólicas intermedias para su uso por parte de las neuronas. 2.- Fibra Nerviosa Mielinizada Cada fibra nerviosa está cubierta por el neurilema, el cual es una vaina formada por el citoplasma de los neurilemocitos (células de Schwann). Las fibras mielínicas están recubiertas por varias vueltas de la membrana plasmática de las células, mientras que las fibras amielínicas están rodeadas una sola vez por dicha membrana. Esta envoltura está constituida por lipoproteínas que se disuelven con el uso de deshidratantes y aclaradores (solventes de las grasas), dejando alrededor de la fibra nerviosa una red de material proteínico denominado neuroqueratina. Los neurilemocitos (células de Schwann) presentan un núcleo aplanado y en posición central en la célula. La mielina puede teñirse y fijarse bien con tetraóxido de osmio. En un corte longitudinal se aprecia la fibra nerviosa como una línea continua y central, muy delgada, envuelta por los neurilemocitos que se interrumpen en ciertos sitios, y que constituyen los nodos intermielínicos. 3.-Medula Espinal Médula Espinal: Sustancia Gris (SG): En la médula espinal semeja la letra H, cuando se observa en cortes transversales. La SG tiene 2 cuernos grises posteriores y otros 2 anteriores. Los cuernos son columnas que se extienden a todo lo largo de la médula espinal. En algunas partes también hay una columna lateral a cada lado. La SG contiene muchos cuerpos celulares, y poca mielina. Sustancia Blanca (SB): Rodea a la H. Contiene un abundante número de fibras nerviosas que ascienden y descienden por la médula. La SB no contiene cuerpos de neuronas. Las fibras que la forman se originan en la SG del encéfalo o médula espinal o en los ganglios raquídeos. Las fibras están organizadas en haces o fascículos, c/u de los cuales incluye fibras de neuronas con funciones similares (sensitivos o motores). La SB contiene muchas células gliales (astrocitos, oligodendrocitos). La mielina (formada por los oligodendrocitos) es un complejo lipoproteico que los solventes disuelven con facilidad, por lo que la preparación de cortes en parafina elimina la mielina. Al colorear los cortes con H/E en c/sitio en los que había mielina aparece un espacio redondeado que parece vacío con un pequeño punto redondo (corte trasversal del axón) que en vida estaba rodeado por mielina
- 5. 4.- Corteza Cerebral Constituye el recubrimiento de los 2 hemisferios cerebrales. Aquí se realizan las siguientes funciones: - integración de la información sensorial. - inicio de las respuestas motoras voluntarias. - coordinación de las respuestas motoras voluntarias. - Se efectúan procesos intelectuales complejos (adquisición y uso del lenguaje, aprendizaje en general, memoria). Los hemisferios cerebrales presentan circunvoluciones profundas, entre las que se ubican surcos (depresiones más superficiales) y cisuras (depresiones más profundas). Las neuronas de la corteza cerebral se disponen en 6 capas: - Capa molecular (más superficial): presenta pocos cuerpos celulares y abundantes fibras de células subyacentes. - Granulosa externa: neuronas pequeñas. - Piramidal externa: cuerpos celulares en forma de pirámide. - Granulosa interna: neuronas pequeñas. - Piramidal interna: cuerpos celulares en forma de pirámide. - Polimorfas: cuerpos celulares de diversas formas. Corteza Cerebelosa: Se organiza en tres capas: - Molecular: la más superficial, neuronas pequeñas, escasa, junto con numerosas fibras mielínicas. - Células de Purkinje: en forma de pera. - Granular interna: con abundantes neuronas pequeñas. El cerebelo presenta las siguientes funciones: - regulación de los movimientos de grupos musculares. - Coordinación de los movimientos de grupos musculares. 5.- Célula de Purkinge Las células de Purkinje son neuronas muy grandes que representan las unidades funcionales del cerebelo. Forman la capa de Purkinje, una capa de la corteza cerebelos situada entre la capa molecular y la capa granulosa. Las células de Purkinje forman la capa de Purkinje, una capa de la corteza en el cerebelo situada entre la capa molecular y la capa granulosa. Las células de Purkinje se encuentran alineadas como piezas de dominó colocadas una frente a la otra. Su árbol dendrítico forma capas bidimensionales a través de las cuales pasan fibras paralelas provenientes de las células musgosas ubicadas en la capa granulosa. Estas fibras paralelas tienen sinapsis excitatorias más débiles (glutamatérgicas) hacia las espinas en la dendrita de la célula de Purkinje, mientras que las fibras trepadoras que se originan desde el núcleo olivario inferior en la médula oblongada y el tronco encefálico proveen un estímulo muy excitatorio a las dendritas cercanas y al soma celular. Las fibras paralelas pasan ortogonalmente a través del árbol dendrítico de la neurona de Purkinje; hasta 200.000 fibras paralelas formando una sinápsis con una única célula de Purkinje. Alternativamente, cada célula de Purkinje solo recibe una sinápsis de una única fibra trepadora. Tanto las células en cesta y las células estrelladas, que se
- 6. encuentran en la capa molecular cerebelosa, proveen un estímulo inhibidor (GABAérgico) a la célula de Purkinje, con las células de cesto en sinápsis hacia el segmento inicial del axón de la célula de Purkinje y las células estrelladas hacia las dendritas. Las células de Purkinje envían proyecciones inhibidoras hacia el núcleo cerebelar profundo, y constituyen la única salida de toda la coordinación motriz en la corteza cerebelar. Técnicas de estudio.
- 7. Los elementos celulares del tejido nervioso son de dos tipos básicos: neuronas y células de glía. A su vez estas últimas incluyen tres tipos: astroglía, oligodendroglía (células de Schwann en el sistema nervioso periférico) y microglía (macrofagos del sistema nervioso). La morfología ramificada tridimensional de todas las células del tejido nervioso central hace complicado su análisis, teniendose que recurrir a diferentes técnicas para poder obtener una información lo más completa posible. Algunas de las técnicas más empleadas son las siguientes: Los colorantes básicos como el Azul de tolouidina (AT), tiñen los cuerpos celulares (somas) de todas las células del tejido, pero no tiñen las ramificaciones, por lo que solo proporcionan información acerca de la distribución, tamaño y morfología de los cuerpos celulares (citoarquitectonia). Este tipo de tinciones son la base de la tinción de Nissl. Otras técnicas permiten detectar la mielina de los axones permitiendo detectar las principales rutas por las que las neuronas proyectan a otras áreas como en el método de Klüver-Barrera. La demostración de la morfología externa tridimensional (geometría) de las células nerviosas se puede poner de manifiesto mediante impregnaciones con metales. Una técnica clásica de este tipo es el método de Golgi, donde solo un pequeño porcentaje de células (1-5%) son impregnadas con cromato de plata que rellena la célula en su totalidad, demostrandose todas sus ramificaciones. La pieza de tejido se impregna en bloque y luego se obtienen cortes gruesos (100-150mm) que permitan el estudio de neuronas individuales en una sola sección. Las técnicas inmunocitoquímicas, en las que se emplean anticuerpos marcados, para detectar sustancias especificas contenidas en las células, han permitido identificar y distinguir tipos celulares concretos y, en muchas ocasiones, estudiar la morfología de las células dado que las sustancias detectas aparecen en la totalidad de la célula. EJEMPLOS: Corteza e hipocampo de gato, cortes de vibratomo de 20 mm. -Tinción de Nissl (somas neuronales) -Tinción de K- Barrera (axones mielínicos y somas) -Tinción inmunocitoquímica frente a GAFP (astroglía) Corteza cerebral de ratón, cortes de 150 mm tenidos con el método de Golgi. -observación de neuronas piramidales y multipolares. -observación de oligodendroglía. Corteza e hipocampo de rata (observación de hipocampo). -cortes teñidos con anticuerpos frente a calbindina. -cortes teñidos con anticuerpos frente a parvalbumina. -cortes teñidos con anticuerpos frente a calretinina. -cortes teñidos con anticuerpos frente a NPY. -Método del sublimado de oro de Cajal para astroglia:
- 8. 1º.- Piezas frescas de cerebro de mamífero se fijan de 2 a 15 días en Solución de formol-bromuro. 2º.- Corte por congelación . 30-40 micras. 3º.- Lavado breve en AD 4º.- Baño aureo: Colocar la Solución de cloruro de oro en una placa de Petri de 5 cm. de diámetro alcanzando una altura mínima de 0,5 cm. Sumergir en ella 4-6 cortes, procurando que todos asienten extendidos en el fondo y sin contactar unos con otros. La temperatura debe ser 24-26ºC, el tiempo 4-6 horas y en la oscuridad. 5º.- Lavado rápido en AD 6º.- Fijación en Solución Fijadora.-------5-10 min. 7º.- Lavado en alcohol de 70ºC. 8º.- Extensión sobre el porta y secado con papel de filtro. 9º.- Deshidratar, aclarar con esencia de orégano y xilol, y montar. Astrocitos de color rojo púrpura. Neuronas en rosa pálido o violeta -Método del carbonato de plata de Rio Hortega para microglia: 1º.- Fijación de fragmentos delgados de tejido nervioso en solución de formol-bromuro de Cajal, de 1 a 3 dias. Calentar 10 min. a 50ºC. 2º.- Corte por congelación 25-30 micras. 3º.- Lavar los cortes en agua amoniacal. 4º.- Lavar en AD, rápido. 5º.- Impregnar en carbonato de plata amoniacal , 5-l0 minutos a temperatura de 15-20ºC. 6º.- Reducción en formalina al 1%. Colocar la solución en una placa de Petri amplia, introducir el corte y agitarlo creando una turbulencia soplando sobre la solución. Cuando el corte se enturbia, sacarlo del formol y 7º.- Lavarlo en agua corriente. 8º.- Virado en cloruro de oro 10-15 mm. 9º.- Fijación en solución fijadora.. 10º.- Deshidratación prolongada, aclaramiento con carboxilol-creosota y montar con bálsarno. Microglía en color violeta casi negro sobre fondo palido. -Método de Golgi-Hortega para oligodentroglia: lº.- Fragmentos de tejido fresco de 2-3 mm. de espesor en Solución fijadora. Durante 2-3 días. 2º.- Lavado rápido en AD. 3º.- Impregnación en Solución de Nitrato de plata, en oscuridad y temperatura ambiente .3-4 días. 4º.- Cortes por congelación de 50-70 micras (seleccionar los que tengan áreas rojizas). 5º.- Deshidratación prolongada: 10 min en alcohol de 90%. y tres pases de 10 min c/u en alcohol absoluto. 10 min. 6º.- Aclarado en carhoxilol 2 veces de 15 min cda una. 7º.- Xilol 3 veces de 10 min c/u. 8º.- Montar con abundante bálsamo. La oligodendroglia aparece en color rojo oscuro, casi negro, sobre fondo rojizo Se pueden teñir por la técnica de Klüver-Barrera, ya que permite detectar la mielina de los axones permitiendo detectar las principales rutas por las que las neuronas proyectan a otras áreas. 1º.- Desparafinar e hidratar hasta alcohol de 96ºC.. 2º.- Solución de azul luxol en estufa (37ºC o 60ºC) de 12 a 20 horas. 3º.- Extraer el exceso de colorante con alcohol de 96ºC, 5-10 seg.
- 9. 4º.- Diferenciar con solución de carbonato de litio, 5-10 seg. 5º.- Pasar varias veces por alcohol de 70ºC bajo control microscópico hasta que se diferencien bien sustancia blanca y sustancia gris. 6º.- Lavar en AD 7º.- Teñir con solución de violeta de Cresilo 6 minutos como mínimo. (Nota: antes de usar esta solución se le añaden 15 gotas de acido acético, se filtra y se calienta a 60ºC. 8º.- Diferenciar en alcohol de 96ºC. 9º.- Deshidratar aclarar y montar. RESULTADOS: Núcleos y grumos de Nissl color rojo-violeta. Vainas de mielina azul oscuro TINCIÓN HEMATOXILINA-EOSINA (Corteza cerebral) La tinción hematoxilina-eosina corresponde a la mezcla de hematoxilina y eosina. La tinción hematoxilina y eosina es el método más popular de tinción utilizado en histología y medicina diagnostica. El método supone la aplicación de la tinción de hematoxilina, que tiñe estructuras acidas (basofilas) en tonos azul y púrpura, y el uso de eosina que tiñe componentes básicos (acidofilos) en tonos de color rosa. TÉCNICA • Sumergir los preparados histológicos en xilol para eliminar los excesos de parafina. • Luego pasan por una serie de alcoholes (100°. 95° y 70°). • Se lava en agua para eliminar exceso de alcohol • Se sumerge en hematoxilina por 10 minutos, luego se lava en agua para eliminar excesos y se pasa rápidamente por alcohol ácido. • Se lava nuevamente • Se sumerge 30 segundos en eosina. • Se pasa por otra serie de alcoholes, en orden creciente (70°, 95° y 100°). • Finalmente se deja remojar 10 minutos en xilol, antes de realizar el montaje final. TINCIÓN HISTOQUÍMICA (NADPH-DIAFORASA) (Célula de Purkinje) La diaforasa pertenece al grupo de las deshidrogenasas, enzimas capaces de eliminar hidrógeno de los sustratos y transferirlo a otra sustancia aceptora. La NADPH-diaforasa cataliza la deshidrogenación del NADPH. En la práctica, se utiliza la reacción de la diaforasa sobre el NADPH para reducir un compuesto dando un producto coloreado. El sustrato utilizado es el NADPH y la sustancia aceptora es una sal de tetrazolio (nitro blue tetrazolium, NBT). La técnica histoquímica empleada “tiñeÓ las neuronas que presentan actividad diaforasa. La actividad NADPH-diaforasa es una actividad enzimática alternativa de la sintasa del óxido nítrico, por lo que la detección histoquímica de la diaforasa nos marca de manera indirecta la sintasa del óxido nítrico, o lo que es lo mismo las neuronas productoras de óxido nítrico. La tinción se realiza sobre cortes “libresÓ, sin pegar a portaobjetos. El protocolo básico es el siguiente: 1. Lavado de los cortes en tampón fosfato (PB) 0.1M 2. Preincubación de los cortes en PB con un 0.25% de Triton X-100, (aprox. 10 minutos)
- 10. 3. Incubación en una solución que contiene: 0,5 mg/ml de NADPH y 0,2 mg/ml de Nitro Blue Tetrazolium en PB 0.1M, con 0,25% de Triton X-100 (aprox. 10 minutos a temperatura ambiente) 4. Colocar en estufa a 37ºC durante varias horas (controlar). 5. Parar la reacción con varios lavados en PB 0.1M 6. Lavado de los cortes en agua destilada y pegado sobre portaobjetos 7. Deshidratación (etanol 96%, etanol 100%), aclarado y montaje Microscopia Electrónica de Barrido El microscopio electrónico de barrido (SEM) es un instrumento que permite la observación y caracterización superficial de materiales inorgánicos y orgánicos, entregando información morfológica del material analizado. A partir de él se producen distintos tipos de señal que se generan desde la muestra y se utilizan para examinar muchas de sus características. Con él se pueden realizar estudios de los aspectos morfológicos de zonas microscópicas de los distintos materiales con los que trabajan los investigadores de la comunidad científica y las empresas privadas, además del procesamiento y análisis de las imágenes obtenidas. Las principales utilidades del SEM son la alta resolución (~100 Å), la gran profundidad de campo que le da apariencia tridimensional a las imágenes y la sencilla preparación de las muestras. Un microscopio electrónico de barrido crea una imagen ampliada de la superficie de un objeto. No es necesario cortar el objeto en capas para observarlo con un SEM, sino que puede colocarse en el microscopio con muy pocos preparativos. El SEM explora la superficie de la imagen punto por punto, al contrario que el TEM, que examina una gran parte de la muestra cada vez. Su funcionamiento se basa en recorrer la muestra con un haz muy concentrado de electrones, de forma parecida al barrido de un haz de electrones por la pantalla de una televisión. Los electrones del haz pueden dispersarse de la muestra o provocar la aparición de electrones secundarios. Los electrones perdidos y los secundarios son recogidos y contados por un dispositivo electrónico situado a los lados del espécimen. Cada punto leído de la muestra corresponde a un píxel en un monitor de televisión. Cuanto mayor sea el número de electrones contados por el dispositivo, mayor será el brillo del píxel en la pantalla. A medida que el haz de electrones barre la muestra, se presenta toda la imagen de la misma en el monitor TEJIDO MUSCULAR El tejido muscular es el responsable de los movimientos corporales. Está formado por células alargadas que contiene una elevada cantidad de filamentos citoplasmáticos responsables de la contracción. Las células musculares son de origen mesodérmico y su diferenciación se debe principalmente a un proceso de alargamiento gradual, con síntesis simultánea de proteínas filamentosas. La célula o fibra muscular es un tipo celular especializado en la síntesis de proteínas contráctiles (actina y miosina). Las fibras
- 11. están ordenadas regularmente en el músculo esquelético y cardíaco, pero irregularmente en el músculo liso. Cualquiera que sea el tipo de tejido muscular, con la técnica de H y E, se observa de color rosa intenso, y con la tinción tricrómica de Masson, de color rojo. De acuerdo con sus características morfológicas y funcionales, en los mamíferos se pueden distinguir tres tipos de tejido muscular. El Músculo Liso El Músculo Estriado Esquelético El Músculo Estriado Cardiaco MÚSCULO LISO El músculo liso está formado por agregados de células fusiformes que no poseen estrías transversales. El proceso de contracción es lento y no está sujeto al control voluntario. Por lo que también es llamado involuntario o visceral, forma parte del aparato digestivo, urogenital, respiratorio y vascular. Morfológicamente, sus células presentan un solo núcleo central y no se encuentran estriaciones en su citoplasma. En un corte transversal se observan estructuras circulares o poligonales con un núcleo central. En un corte longitudinal se aprecian los núcleos alargados e irregulares. Los límites celulares son muy poco detectables con la técnica de H y E. Las células musculares lisas participan en una gran variedad de sistemas alrededor del cuerpo incluyendo: 1) Sistema integumentario – forman los vasos sanguíneos los cuales regulan el flujo de sangre a las dermis. 2) Sistema Cardiovascular – forman los vasos sanguíneos los cuales regulan las distribución de sangre a todo el cuerpo y la presión sanguínea 3) Sistema Respiratorio – Las contracciones y relajaciones del musculo liso alteran el diámetro de los pasajes respiratorios. 4) Sistema Digestivo – El musculo liso en el tracto digestivo ayuda en el procesamiento mecánico del bolo alimenticio y de su movimiento a través del tracto. 5) Sistema Urinario – El musculo liso alrededor de los vasos sanguíneos alteran la razón con la que filtra la sangre los riñones. Contracciones del tejido muscular liso alrededor de la vejiga fuerzan la orina hacia el exterior. 6) Sistema reproductor – El movimiento de los espermatozoides y del huevo en hombre y mujeres, respectivamente, depende de las contracciones de los tractos reproductores por parte del musculo liso. MÚSCULO ESTRIADO ESQUELETICO El tejido muscular estriado esquelético presenta estrías transversales al eje longitudinal de las fibras musculares. En el microscopio óptico, dichas estrías aparecen como pequeñas líneas oscuras sobre el citoplasma de la célula muscular, que sólo pueden observarse con objetivo seco fuerte (40x) o con el de inmersión de aceite (100x). Las células tienen varios núcleos que se sitúan en la periferia; esto último puede apreciarse en los cortes longitudinales, pero aún más en los cortes transversales de las fibras celulares.
- 12. Las fibras musculares están organizadas en haces envueltos por una membrana externa de tejido conjuntivo, llamada empimisio. De éste parten septos muy finos de tejido conjuntivo, que se dirigen hacia el interior del músculo, dividiéndolo en fascículos, estos septos se llaman perimisio. Cada fibra muscular está rodeada por una capa muy fina de fibras reticulares, formando el endominsio. El tejido conjuntivo mantiene las fibras musculares unidas, permitiendo que la fuerza de contracción generada por cada fibra individualmente actúe sobre el músculo entero, contribuyendo así a su contracción. MÚSCULO ESTRIADO CARDIACO El tejido muscular estriado cardíaco está formado por tres tipos de células: células musculares estriadas cardíacas típicas, células nodales y miofibrillas cardíacas conductoras. Las fibras musculares estriadas cardíacas típicas presentan estriaciones transversales, al igual que el músculo estriado esquelético; sus células tienen uno o dos núcleos alargados y centrales Las miofibrillas cardíacas conductoras son células más grandes que las fibras musculares cardíacas típicas, son fusiformes, presentan un núcleo central; el citoplasma es poco acidófilo, porque contiene gran cantidad de glucógeno, y no se observan estriaciones en él. Los discos intercalares unen las células musculares cardíacas entre sí, lo que proporciona mayor adhesión al tejido e intervienen en la rápida comunicación entre células. Esto permite su contracción simultánea y la producción del latido. La célula muscular cardiaca es muy semejante a la fibra muscular esquelética, aunque posee más sarcoplasma, mitocondrias y glucógeno. También llama la atención el hecho de que en los músculos cardiacos, los filamentos ocupen casi la totalidad de la célula y no se agrupen en haces de miofibrillas. Una característica específica del músculo cardiaco es la presencia de líneas transversales intensamente coloreables que aparecen a intervalos regulares. Estos discos intercalares presentan complejos de unión que se encuentran entre células musculares adyacentes. Son uniones que aparecen como líneas rectas o muestran un aspecto en escalera. Las células musculares cardiacas son casi totalmente dependientes del metabolismo aeróbico (oxigeno) para obtener las energía necesaria para contraerse. Por esto el sarcoplasma (equivalente del citoplasma en células musculares) tiene un gran número de mitocondria y abundantes reservas de mioglobina (almacenaje de oxigeno). Cada célula muscular cardiaca se comunica con otras a través de los discos intercalados los cuales permiten una comunicación eléctrica entre las células permitiendo la transferencia de la señal que produce la contracción. TINCIÓN: HEMATOXILINA-EOSINA • Fijación de la muestra con Formalina (solución acuosa tamponada de formaldehído). Detiene el metabolismo y conserva la estructura del tejido (proteínas pero no lípidos ⇒ mal fijador de membranas). • Lavado y deshidratación (serie de soluciones alcohólicas de concentración creciente hasta el 100%). Extracción del alcohol con Xileno, luego inclusión de la muestra con parafina fundida (miscible en Xileno). Enfriamiento y endureci-miento de la parafina ⇒ Taco ⇒ cortes de 5-15 µ de espesor con micrótomo que se montan sobre portaobjetos.
- 13. • Coloración con Hematoxilina: extracción de la parafina con Xileno, re-hidratación del corte con soluciones alcohólicas de concentración decreciente, y tinción con solución acuosa de Hematoxilina. • Coloración con Eosina: deshidratación del corte con soluciones alcohólicas de concentración creciente, y tinción con solución alcohólica de Eosina. Lavado con Xileno, agregado de un líquido de montaje no acuoso, y cobertura con un cubre-objetos para lograr un preparado permanente. La Eosina es un colorante ácido (predomina densidad de carga negativa), por lo cual se asocia y colorea a estructuras catiónicas del citoplasma y matriz extracelular, tales como: filamentos citoplasmáticos (como los de células musculares); membranas intracelulares; y fibras extracelulares (por sus aminoácidos básicos ionizados). La Hematoxilina se asocia con mordientes para actuar como un colorante básico, por lo cual se asocia y colorea estructuras aniónicas (que posean fosfatos, sulfatos y/o carboxilos ionizados): • Heterocromatina y nucléolos • RNA ribosomal • Matriz extracelular (por los sulfato de los GAG) Ácido periódico-Schiff (PAS): Fundamento El ácido periódico rompe la unión entre carbonos con hidroxilos adyacentes, y forma grupos aldehído. El reactivo de Schiff reacciona con los aldehídos para dar un color rojo púrpura intenso. La reacción de PAS tiñe carbohidratos, y se usa para detectar: • Gránulos de glucógeno • Moco en diversas células • Membrana basal de los epitelios • Fibras reticulares del tejido conjuntivo TRICROMICO DE MASSON 1º-Desparafinado. Estufa durante 30 min. a 60º. Sumergimos en xilol durante 10 o 15 min. 2º- Hidratación. Alcohol absoluto-5min. Alcohol 96º-5min. Alcohol 70º-5min. 3º- Lavar en H2O destilada. 4º- Hematoxilina de Weigert – 5 min. 5º- Lavar con agua corriente – 10 min. 6º- Fucsina de Ponceau – 5 min.
- 14. 7º- Ácido fosfomolíbdico – 5 min. 8º- Ácido fosfomolíbdico – 5 min. 9º- Verde luz – 5-7 min. 10º-Deshidratar. Alcohol de 70º Alcohol de 96º. Xilol. 11º- Montaje. RESULTADOS: Tejido conjuntivo: verde Tejido muscular: pardo Tejido epitelial: rojizo. SISTEMA ENDOCRINO TIROIDES Es una glándula endocrina folicular. El estroma consiste en una cápsula de conjuntivo denso irregular que emite trabéculas al interior del órgano. El parénquima está formado de multitud de folículos tiroideos, cada uno puede presentar células aplanadas, cúbicas o cilíndricas, dependiendo de la actividad secretoria. La secreción se almacena en el interior de los folículos, en el corte histológico tiene una apariencia de sustancia homogénea a la que se denomina coloide tiroideo. En la tiroides existe un grupo de células débilmente teñidas (con citoplasma claro) llamadas células «C» o parafoliculares; estas células producen la hormona calcitonina y suelen localizarse entre los folículos
- 15. tiroideos (en el intersticio que los separa), pero pueden observarse también entre las células foliculares de cada folículo. Estas células se distinguen por ser más grandes, esféricas y con núcleo central igualmente esférico. HIPÓFISIS O PITUITARIA Es la glándula endocrina por excelencia, se sitúa en el piso del diencéfalo. En los cortes histológicos se distinguen dos porciones: la adenohipófisis y la neurohipófisis. La segunda libera hormonas producidas en el hipotálamo. Adenohipófisis La adenohipófisis es una glándula endocrina, cordonal en su mayor parte, aunque pueden observarse en ciertas áreas algunos folículos. Existen dos grandes grupos celulares: el de células con una gran afinidad tintorial denominadas cromófilas, y el de aquellas que no tienen esta afinidad, denominadas cromófobas; estas últimas son células grandes con poco citoplasma y muy débilmente teñidas. Las células cromófilas pueden ser: basófilas o acidófilas, dependiendo de si presentan granulaciones citoplasmáticas con afinidad a colorantes básicos o a ácidos, respectivamente; entre las células se observan abundantes capilares sanguíneos. La adenohipófisis suele dividirse en varias porciones: pars distalis (parte distal), pars tuberalis (parte tuberal o infundibular) y pars intermedia; la primera es la más grande e importante y su descripción histológica se ajusta a la que se ha mencionado anteriormente; en la pars intermedia y la pars tuberalis predominan células cromófilas basófilas; en la primera pueden existir, además, algunos folículos con secreción en el interior. Neurohipófisis La neurohipófisis está formada por una gran cantidad de fibras nerviosas (axones), de neuronas cuyos cuerpos se sitúan en el hipotálamo (por lo que no se aprecian al corte histológico), estas fibras están rodeadas de células de la neuroglia denominadas pituicitos, que son células pequeñas y de núcleo denso, también pueden observarse vasos sanguíneos y capilares. En las fibras existe un material oscuro que se tiñe intensamente, llamado corpúsculo de almacenamiento, o sustancia neurosecretora acumulada, según la Nómina Histológica, y corresponde a la congregación de hormonas y otras estructuras en este sitio, antes de su liberación. SUPRARRENALES Son glándulas pares. Su estroma está compuesto de una cápsula de conjuntivo denso irregular que emite pequeñas trabéculas apenas perceptibles. El parénquima se divide en una corteza y una médula. Cualquiera de estas dos porciones corresponde a una glándula endocrina cordonal. En la corteza se distinguen tres zonas, que de afuera hacia adentro son: glomerular, fascicular y reticular. La zona glomerular está formada por células cilíndricas o poliédricas con citoplasma tenuemente acidófilo; en ciertas especies (hombre y equinos) estas células presentan gránulos
- 16. basófilos, sus núcleos son pequeños y oscuros y se agrupan en cordones que adquieren la forma de pequeños arcos (glomérulos) adyacentes a la cápsula. La zona fascicular (o fasciculada) está compuesta de células cúbicas o poliédricas, cuyo citoplasma es débilmente acidófilo y contiene múltiples vesículas de lípidos que por los procedimientos rutinarios no se observan, los cuales le dan una apariencia espumosa; por esta razón se les denomina espongiocitos. Las células se agrupan en cordones paralelos entre sí, dispuestos radialmente en relación con la porción medular del órgano. La zona reticular está formada por cordones celulares que se unen (o anastomosan) formando pequeñas redes (de ahí el nombre de esta parte de la corteza), las células son poliédricas con núcleo esférico e hipercromático (en ocasiones se observan picnóticos), su citoplasma tiene un menor número de vesículas lipídicas. En la porción medular se observan células que forman cordones en diversas direcciones, se pueden distinguir porque son células más grandes que en la zona reticular, además de tener núcleos voluminosos y débilmente teñidos. Hay también células ganglionares (cuerpos de neuronas simpáticas). En ambos tipos celulares los nucléolos se advierten con facilidad. Las células de la médula adrenal producen dos tipos de catecolaminas: la adrenalina y la noradrenalina (o epinefrina y norepinefrina, respectivamente); las células se especializan en la producción únicamente de uno de estos dos compuestos (hormonas) y están distribuidas al azar en el parénquima medular, sin embargo, en los rumiantes las células que producen epinefrina se distribuyen especialmente en la periferia de la médula y las que producen noradrenalina, hacia el centro. PANCREAS El páncreas es una glándula anficrina pues se encarga de producir enzimas digestivas (secreción exocrina) y hormonas (secreción endocrina). Presenta agrupamientos especializados para cada una de estas funciones: la porción exocrina está formada por glándulas acinosas ramificadas, los acinos son serosos; una característica importante y específica de los acinos es la presencia de células aplanadas de citoplasma acidófilo tenue al centro, por lo que se conocen como células centroacinosas, éstas corresponden a la parte inicial de uno de los conductos conocido como conducto intercalado, que penetra a la luz de los acinos. La porción endocrina está formada por glándulas cordonales de células poliédricas acidófilas tenuemente teñidas, agrupadas y localizadas al azar entre los acinos serosos, dichos agrupamientos se conocen como islotes pancreáticos endocrinos. Con técnicas de tinción especiales se pueden distinguirse diversos tipos celulares, pero con técnicas de rutina esto no es factible. El páncreas presenta una cápsula y trabéculas de tejido conjuntivo ordinario laxo areolar que divide al parénquima en lóbulos y lobulillos. Tinción de Gomori: tinción utilizada para la demostración de enzimas, especialmente fosfatasas y lipasas. También evidencoa fibras de tejido conjuntivo y gránulos de secreción Tinción de van Gieson: un método de tinción del tejido conjuntivo. No se utiliza tan a menudo como la tinción de Mallory porque se difumina con el tiempo. El colágeno tiñe de rojo y el músculo y el citoplasma de amarillo. En combinación con la tinción de Verhoeff es una las tinciones más interesantes para el estudio de los vasos sanguíneos
