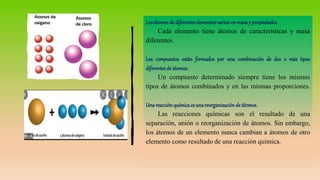
El documento presenta un resumen del modelo atómico propuesto por John Dalton en 1803. De acuerdo con Dalton, toda la materia está compuesta de átomos indivisibles e indestructibles. Cada elemento químico está formado por un tipo único de átomo, y los átomos de diferentes elementos varían en masa y propiedades. Los compuestos químicos se forman por la combinación de dos o más tipos de átomos.