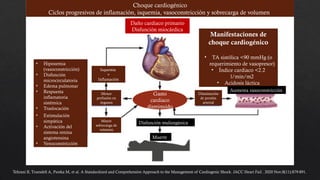
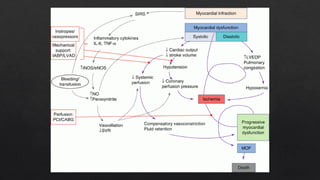
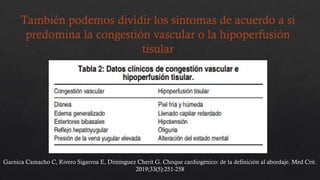
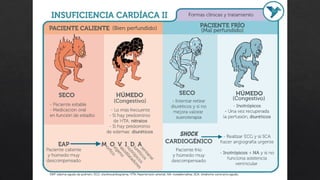
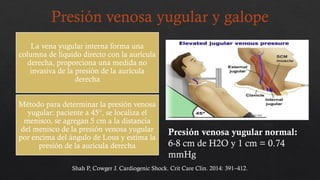
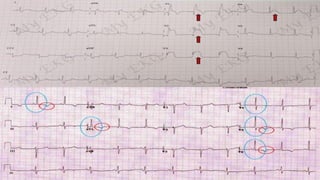
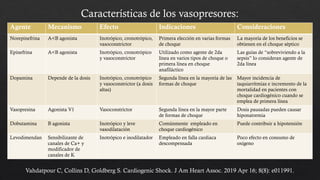
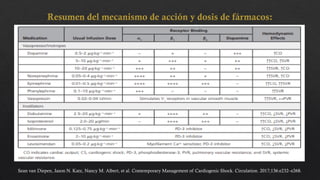
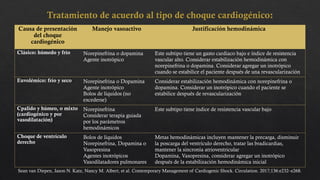
El choque cardiogénico es un síndrome caracterizado por hipotensión e hipoperfusión sistémicas debido a un gasto cardiaco insuficiente, con criterios diagnósticos que han evolucionado en el tiempo. Su manejo incluye identificación de la etiología, evaluación hemodinámica y tratamiento con líquidos y fármacos inotrópicos para estabilizar al paciente. Las manifestaciones clínicas varían entre congestión vascular y hipoperfusión tisular, y se requiere un enfoque diagnóstico integral que incluya historia clínica, electrocardiograma y ecocardiograma.