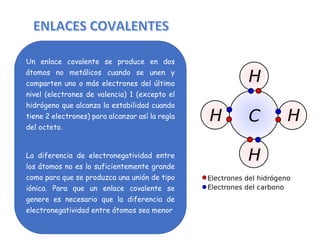
Enlace covalente entre átomos no metálicos
- 1. Un enlace covalente se produce en dos átomos no metálicos cuando se unen y comparten uno o más electrones del último nivel (electrones de valencia) 1 (excepto el hidrógeno que alcanza la estabilidad cuando tiene 2 electrones) para alcanzar así la regla del octeto. La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor
- 2. Enlace Covalente Polar Se produce entre átomos de distinta Electronegatividad. Como, por ejemplo: HCL, CO, Entre otros. Los electrones compartidos están más desplazados hacia el átomo más electronegativo Aparecen zonas de mayor densidad de carga positiva (∂+) y zonas de mayor densidad de carga negativa (∂-)
- 3. Enlace Covalente Apolar. Se da cuando los pares de electrones se comparten de manera equitativa o muy pareja. Se da en todas las moléculas Diatómicas. Para efectos prácticos no es polar si la diferencia de electronegatividad está en el rango de: (0.0 a 0.4) Ejemplo: CL2 , SiH4 , SbH3
- 4. Enlace Covalente Múltiple Enlace Covalente Doble Un doble enlace se forma cuando se comparten cuatro electrones entre dos átomos. Por ejemplo, en la molécula de oxígeno (O2). Cada O tiene la siguiente configuración electrónica: Que también se puede representar como: O 1s2 2s2 2p4 En el caso de las moléculas de Cl2 e H2, únicamente se comparte un par de electrones entre los dos núcleos; esto se conoce como un enlace covalente sencillo. En otras moléculas se comparte más de un par de electrones entre dos núcleos y estos enlaces se denominan enlaces covalentes múltiples. Podemos encontrar dos tipos de enlaces múltiples: enlaces covalente dobles y enlaces covalentes triples.
- 5. Enlace Iónico El enlace iónico es la atracción electrostática entre iones de carga opuesta. Los compuestos iónicos están formados por cationes metálicos y aniones no metálicos. El metal cede electrones al no metal, para que ambos alcancen una configuración de gas noble. El metal tiene electrones de más que cede al no metal. Entonces, el metal queda con un número de electrones menor, lo que se traduce en una carga más positiva que lo convierte en un catión. El no metal acepta los electrones del metal. De este modo, adquiere un número mayor; esto significa una carga más negativa, convirtiéndose en un anión. Ambos iones terminan con las capas externas llenas de electrones, así anulan mutuamente sus cargas para dar lugar a un compuesto neutro.
- 6. Enlace Metálico El enlace metálico se produce cuando se combinan metales entre sí. Los átomos de los metales necesitan ceder electrones para alcanzar la configuración de un gas noble. En este caso, los metales pierden los electrones de valencia y se forma una nube de electrones entre los núcleos positivos. A los enlaces metálicos se deben muchas de las propiedades típicas de los metales, como su solidez, su dureza, e incluso su maleabilidad y ductilidad. La buena conducción del calor y de la electricidad de los metales.
- 7. Regla del Octeto La regla del octeto establece que los iones de los distintos elementos químicos que se encuentran en la Tabla Periódica suelen completar sus últimos niveles de energía con 8 electrones. Debido a esto, las moléculas pueden adquirir una estabilidad semejante a la de los gases nobles (ubicados al extremo derecho de la tabla periódica), cuya estructura electrónica (con su último nivel de energía completo) los hace muy estables, o sea, poco reactivos.
- 8. Enlace Dativo Un enlace covalente dativo es un tipo de enlace covalente en el que ambos electrones del par compartido proceden del mismo átomo. También se conoce como enlace de coordinación. Formación de ion amonio NH4 + En el NH3 molécula, el átomo de nitrógeno tiene un par solitario de electrones después de completar su octeto. Este par solitario de electrones comparte con el ion H+ de HCl. El enlace covalente coordinado formado entre N y H, que conduce a la formación de iones de amonio NH4+.