atomo.docx
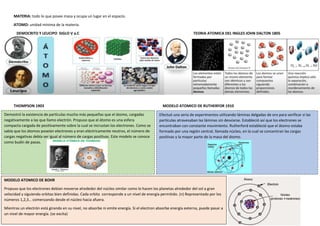
- 1. MODELO ATOMICO DE BOHR Propuso que los electrones debían moverse alrededor del núcleo similar como lo hacen los planetas alrededor del sol a gran velocidad y siguiendo orbitas bien definidas. Cada orbita corresponde a un nivel de energía permitido. (n) Representado por los números 1,2,3… comenzando desde el núcleo hacia afuera. Mientras un electrón está girando en su nivel, no absorbe ni emite energía. Si el electron absorbe energía externa, puede pasar a un nivel de mayor energía. (se excita) MATERIA: todo lo que posee masa y ocupa un lugar en el espacio. ATOMO: unidad mínima de la materia. DEMOCRITO Y LEUCIPO SIGLO V a.C TEORIA ATOMICA DEL INGLES JOHN DALTON 1805 THOMPSON 1903 MODELO ATOMICO DE RUTHERFOR 1910 Demostró la existencia de partículas mucho más pequeñas que el átomo, cargadas negativamente a las que llamo electrón. Propuso que el átomo es una esfera compacta cargada de positivamente sobre la cual se incrustan los electrones. Como se sabía que los átomos poseían electrones y eran eléctricamente neutros, el número de cargas negativas debía ser igual al número de cargas positivas. Este modelo se conoce como budín de pasas. Efectuó una seria de experimentos utilizando láminas delgadas de oro para verificar si las partículas atravesaban las láminas sin desviarse. Estableció así que los electrones se encontraban con constante movimiento. Rutherford estableció que el átomo estaba formado por una región central, llamada núcleo, en la cual se concentran las cargas positivas y la mayor parte de la masa del átomo.
- 2. MODELO ATOMICO DE SCHRODINGER: Describió el comportamiento del electrón en términos probabilísticos y considero que la trayectoria definida del electrón según Bohr, debía sustituirse por la probabilidad de hallarlo en una zona del espacio periférico al número atómico. MODELO NUBE DE ELECTRONES MODELO ATOMICO ACTUAL: este modelo se basa en el principio de dualidad onda-corpúsculo y en el principio de incertidumbre de Heidelbeng. En 1924 Louis de Broglie concluyo que las ondas se comportaran como partículas y estas muestran propiedades ondulatorias. Toda particula en movimiento lleva asociada una onda. En 1927 Warner Heidelberg planteo el principio de incertidumbre, el cual indicaba que era imposible conocer simultáneamente la posición y el movimiento de un electron. Si bien la mecánica cuántica no indica en que parte del átomo esta un electrón, si advierte la región de mayor probabilidad en un momento dado. (orbital atómico). Entonces podemos decir que los átomos componen la materia. TABLA PERIODICA: La tabla periódica de los elementos es una forma gráfica de ordenar y distribuir los distintos elementos químicos de acuerdo con ciertos criterios y características. La tabla periódica actual ha sido construida en orden creciente de números de protones (z) de tal manera que todos los elementos con propiedades análogas se ubican en la misma columna. Se dividen en grupos y periodos. Periodos: son cada una de las filas de la tabla y se corresponden al nivel mayor de energía correspondiente a cada atomo. Hay 7 periodos. Grupos: los elementos de un mismo grupo tienen características físicas y químicas similares. Esto no se debe a que se encuentran en un mismo grupo todos los elementos cuyos átomos tienen igual número de electrones en el último nivel de energía. La tabla está dividida en grupos a y b. en total hay 18 grupos. Numero atómico: al número de protones que tienen los átomos de un elemento se lo llama número atómico y se los simboliza con la letra Z Isotopos: a los átomos del mismo elemento (igual z) pero distintos número de neutrones ( distinta masa) se los llama isotopos. El número másico: es la suma de protones y neutrones y se simboliza con la letra A. LOS METALES: Pierden electrones (se oxidan) con facilidad formando iones positivos o cationrs Son buenos conductores del calor y la electricidad Son sólidos a temperatura ambiente Son dúctiles y maleables LOS NO METALES: Tienen tendencia a captar electrones (se reducen) Tienen muchos electrones en la última orbita
- 3. Son malos conductores del calor y la electricidad Son frágiles, no tienen brillo ni reflejan Se encuentran en estado líquido solido o gaseosos Se ubican por encima de la escalera LOS GASES NOBLES: No reaccionan con nada Son inertes Tienen 8 electrones en la ultima orbita Son inoloros, incoloros e insípidos Solubles en agua Se ubican en el grupo 18 METALES ALCALINOS: METALES ALCALINOSTERREOS: METALES DE TRANSICION: GRUPO DEL ALUMINIO: GRUPO DEL CARBONO: GRUPO DE NITROGENO