salmonellas
- 1. Apoptosis Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 2. Proliferación Diferenciación y Apoptosis
- 3. Necrosis Apoptosis Muerte celular fisiológica Muerte celular que se presenta en los mismos tejidos en un punto predecible del desarrollo APOPTOS: la caída de las hojas & marchitar de una flor Kerr JFR, Wyllie AH, Currie AR. (1972) Apoptosis: A basic biological phenomenon with wide-ranging implications in tissue kinetics. Br J Cancer ; 26: 239-257. Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 4. Durante la metamorfosis desaparecen algunos órganos y aparecen otros Metamorfósis Degeneración y Reabsorción Tisular
- 5. Erizos y estrellas de mar Crinoideos y anémonas La metamorfosis de larvas al estado adulto implica un proceso de muerte celular fisiológica de algunos de los tejidos de la larva Mulcrone, R. 2005. "Echinodermata" (On-line), Animal Diversity Web., 2008 http://animaldiversity.ummz.umich.edu/site/accounts/information/Echinodermata.html. . Metamorfósis en Equinodermos Degeneración y Reabsorción Tisular
- 6. Acherontia atropos La metamorfosis de oruga a mariposa implica un proceso de muerte celular fisiológica de la mayoría de los tejidos de la oruga Harris, M. 2002. "Lepidoptera" (On-line), Animal Diversity, 2008 at http://animaldiversity.ummz.umich.edu/site/accounts/information/Lepidoptera.html. Metamorfósis en Lepidópteros Degeneración y Reabsorción Tisular Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 7. Agalychnis callidryas La metamorfosis de renacuajo a rana o sapo implica un proceso de muerte celular fisiológica de algunos tejidos del renacuajo como la cola y las branquias Heying, H. 2003. "Anura" (On-line), Animal Diversity Web. 2008 at http://animaldiversity.ummz.umich.edu/site/accounts/information/Anura.html.. Metamorfósis en Anfibios Degeneración y Reabsorción Tisular
- 10. Apoptosis en humanos Mórura Blátura Células del epiblasto
- 11. Figure 23-47. Experimental demonstration that different classes of sensory neurons in the dorsal root ganglion require different trophic factors for survival. Degeneración Neuronal y Apoptósis Los factores tróficos ayudan a mantener la viabilidad meuronal Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 12. TP: Regeneración hepática SI: Selección de clonas auto-reactivas T/B M orfogénesis y Apoptósis
- 15. CASPASAS Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 16. CASPASAS Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 17. Natu r e 2000, 407:770-776 Activación de Caspasas
- 18. Clasificación de Caspasas Cistein Aspartic Acid Petidases
- 19. CASPASAS Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 20. CASPASAS Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 21. CASPASAS
- 22. Apoptosis D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B Departamento INCMN SZ de Bioquímica
- 23. ced-9 ced-4 ced-3 Bcl-2 Apaf1 Casp9 Casp3 Cit C Bax Regulador Adaptador Efector Regulador Adaptador Efector En C. elegans En humanos
- 25. Apoptosis Fosfatidilserina Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 26. R egeneración hepática y apoptósis Kren BT, Trembley JH, Krajewski S, Behrens TW, Reed JC, Steer CJ (1996). Modulation of apoptosis-associated genes bcl-2, bcl-x, and bax during rat liver regeneration. Cell Growth Differ. 7(12):1633-1642 Remoción del 70% del hígado promueve regeneración hepática in vivo. Bax Bcl-2 y Bcl X 0 5 10 15 20 Síntesis de DNA Días después de la hepatectomía Cambio relativo en RNA m Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 27. I nfección viral hepática promueve apoptósis Guo JT, Zhou H, Liu C, Aldrich C, Saputelli J, Whitaker T, Barrasa MI, Mason WS, Seeger C. (2000). Apoptosis and regeneration of hepatocytes during recovery from transient hepadnavirus infections. . J Virol 74(3):1495-1505. La infección hepática con el virus promueve apoptósis mediada oir linfocitos T CD3 y CD4 positivos y regeneración hepática in vivo. Indice Apoptótico Infiltración de CD4 CD8 0 5 10 Síntesis de PCNA Semanas después de la infección Cambio relativo Interferón gamma Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 28. Sidney Brenner Caenorhabditis elegans Jhon Sulston Nemátodo
- 29. De 1090 células 131 mueren fisiológicamente. Los cuerpos de algunas células muertas por apotosis son visibles a través de la cutícula por poco tiempo. Unos minutos más tarde los cuerpos de las células muertas son reconocido por macrófagos antes de ser fagocitados.
- 30. Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
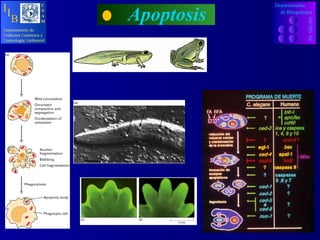
- 31. PMi PMa PMa TNF/CD95 FAS/DR3 NGF/IL3/PDGF PROGRAMA DE MUERTE C. elegans H. sapiens ced 3 ICE/ Casp 3/6 ? crmA / IAPS ced4 APAF2 egl1 BAX / BAD ced 9 BCL2 / BCLX L ? Casp 9 ced 1, 2 , 5-7, 10 ? nuc1 ? PMi ? Casp 8 /10 ? TNF/FasL/CD40L ? APAF1 (Cit C)
- 32. Apoptosis ced9 Bcl-2 Bax Bcl-X L Bad Bak Bcl-2 Bax Bcl-2 Bcl-2 Se previene la apoptosis No se previene la apoptosis Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 33. Apoptosis Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 34. Apoptosis Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 36. Apoptosis
- 37. Apoptosis Programa de Muerte Activo Constitutivamente Programa de Muerte Suspendido Temporalmente NGF PDGF Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 38. Apoptosis Programa de Muerte Activo Constitutivamente Programa de Muerte Suspendido Temporalmente Integrinas Unidas a Componentes de Matriz Extracelular
- 39. Apoptosis Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 40. Apoptosis FADD TRAF FLICE = ProCaspsasa 8/10 Caspsasa 8/10 BID Nativo BID Procesado Activación de la Fase Mitocondrial TNF- FAS CD40 ProCaspsasa 9 ProCaspsasa 3/6 Caspsasa 9 Caspsasa 3/6
- 41. Noxa Puma
- 42. Apoptosis
- 43. Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
- 45. Apoptosis Departamento INCMN SZ de Bioquímica D epartamento de M edicina G enómica y T oxicología A mbiental U N A M I I B
Notas del editor
- The death-receptor pathway (left pathway in the figure opposite) is triggered by members of the deathreceptor superfamily (such as CD95 and tumour necrosis factor receptor I). Binding of CD95 ligand to CD95 induces receptor clustering and formation of a deathinducing signalling complex. This complex recruits, via the adaptor molecule FADD (Fas-associated death domain protein), multiple procaspase-8 molecules, resulting in caspase-8 activation through induced proximity (see Box 2). Caspase-8 activation can be blocked by recruitment of the degenerate caspase homologue c-FLIP (ref. 61). The mitochondrial pathway (right) is used extensively in response to extracellular cues and internal insults such as DNA damage (see review in this issue by Rich et al. , pages 777–783). These diverse response pathways converge on mitochondria, often through the activation of a pro-apoptotic member of the Bcl-2 family. Unlike Bcl-2, which seems to spend most if not all of its life attached to intracellular membranes, many group II and group III members, including Bax, Bad, Bim and Bid, can shuttle between the cytosol and organelles62–65. The cytosolic forms represent pools of inactive, but battle-ready proteins. Pro-apoptotic signals redirect these proteins to the mitochondria, where the fight for the cell’s fate will take place. Activation of pro-apoptotic members can occur through proteolysis, dephosphorylation and probably several other mechanisms35,36. Pro- and anti-apoptotic Bcl-2 family members meet at the surface of mitochondria, where they compete to regulate cytochrome c exit by a mechanism that is still debated (see text). If the pro-apoptotic camp wins, an array of molecules is released from the mitochondrial compartment. Principal among these is cytochrome c , which associates with Apaf-1 and then procaspase-9 (and possibly other proteins) to form the apoptosome. Heat-shock proteins act at multiple steps in the pathway to modulate apoptosis (not shown; see refs. 66, 67). The death-receptor and mitochondrial pathways converge at the level of caspase-3 activation. Caspase-3 activation and activity is antagonized by the IAP proteins, which themselves are antagonized by the Smac/DIABLO protein released from mitochondria. Downstream of caspase-3, the apoptotic programme branches into a multitude of subprogrammes, the sum of which results in the ordered dismantling and removal of the cell. Cross-talk and integration between the death-receptor and mitochondrial pathways is provided by Bid, a pro-apoptotic Bcl-2 family member. Caspase-8-mediated cleavage of Bid greatly increases its pro-death activity, and results in its translocation to mitochondria, where it promotes cytochrome c exit. Note that under most conditions, this cross-talk is minimal, and the two pathways operate largely independently of each other62,68. Clearly, additional death-inducing pathways must exist, as developmental apoptosis is by and large normal in mice defective in the caspase-8 and caspase-9 pathways7,52.
