Concentracion de las soluciones
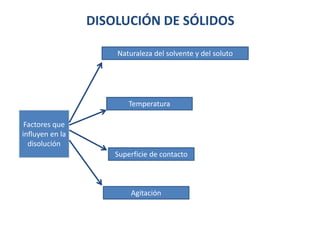
- 1. DISOLUCIÓN DE SÓLIDOS Factores que influyen en la disolución Naturaleza del solvente y del soluto Temperatura Superficie de contacto Agitación
- 2. Concentración de las soluciones Una solución se identifica definiendo el tipo de soluto y de solvente e indicando su concentración, que es la relación numérica que existe entre el soluto y el solvente Una forma de expresar concentración es indicar el porcentaje , que puede ser: masa en masa % m/m masa en volumen % m/v
- 3. • % m/m indica los gramos de soluto que se encuentran en 100 gramos de solución. Por ejemplo: una solución 20 % m/m contiene 20 g de soluto en 100 g de solución. • % m/v indica los gramos de soluto que se encuentran en 100 ml de solución. Por ejemplo: una solución 20 % m/v contiene 20 g de soluto en 100 ml de solución.
- 4. • % m/v expresa los gramos de soluto que se encuentran en 100 mililitros de solución • Entonces si tengo una solución al 5% m/m de sal en agua significa que hay 5 g de sal cada 100 g de solución. • Si tengo una solución 10% m/v de alcohol en agua significa que hay …………………………………… • Si tengo una solución 8 % m/v de vinagre en agua significa que hay …………………………………… • Una solución acuosa de azúcar al 25% m/m contiene ……………………………………
- 5. • ¿Cómo se calcula la concentración? • Si una solución se prepara con 2g de sal en 50ml de solución ¿cuál es su concentración? 2g de soluto 50 ml de solución x = 100 ml de solución
- 6. ¿Cuál es la concentración de una solución que contiene 20 g de azúcar en 80 g de solución? 20g de soluto 80 g de solución x = 100 g de solución
- 7. • Calcula la concentración de una solución que contiene 30 g de alcohol en 50 ml de solución acuosa. • Si preparo una solución con 10 g de sulfato de cobre cada 250 de solución acuosa ¿cuál es su concentración
- 8. • ¿Cómo prepararías una solución al 8% m/m de sal en agua? • Si tengo 12 g de acetona en 120 ml de solución acuosa ¿cuál es su concentración?
- 9. • Calcula la concentración de una solución acuosa que por cada 150 g contiene 30 g de bicarbonato. • ¿Cuántos gramos de soluto contienen 100 ml de una solución 4 % m/v de glucosa en agua?
- 10. RECUERDA: La densidad te permite relacionar la masa de una sustancia con su volumen d = m/v • Si tengo una solución 20% v/v de alcohol en agua ¿Cuántos g de alcohol tengo en 50 ml de solución? (densidad de alcohol 0,9 g/ml)
- 11. • Se mezclan 20 ml de vinagre con 40 ml de agua para formar una solución. ¿Cuál sería su concentración en % v/v? • Si a 8g de ácido cítrico le agregas 40 ml de agua ¿cuál sería el % m/m de esa solución?
- 12. • Una solución contiene 40 g de cloruro de sodio en 160g de agua ¿qué concentración % m/m tiene? • ¿Cuál es la concentración % m/v de alcohol en el vino, si tiene 24 g por vaso de 200 ml? Y su % v/v?