TERMO 16 Unidades 1-2 Ejemplos B.pdf
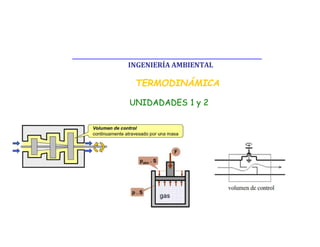
- 1. INGENIERÍA AMBIENTAL UNIDADADES 1 y 2 TERMODINÁMICA
- 2. Prof. José G. Prato Ph.D TERMODINÁMICA UNIDAD 1: PRIEMRA LEY DE LA TERMODINÁMICA TEMA 1.4. La Primera Ley de la Termodinámica TEMA 1.5. Mecanismos de transferencia de calor UNIDAD 2: SUSTANCIAS PURAS, ANÁLISIS DE MASA Y ENERGÍA EN SISTEMAS ABIERTOS Y CERRADOS TEMA 2.1. Sustancia pura. Propiedades, diagramas y tablas TEMA 2.3. Análisis de energía de sistemas cerrados TEMA 2.5. Aplicaciones a algunos dispositivos ingenieriles de flujo estacionario
- 3. Ejercicio # 8: El flujo de masa de vapor a una turbina es 1,5 kg/s, el calor transferido desde la turbina es de 8.5 kW, además se tiene los datos en la figura. UNIDADES I y II: EJERCICIOS DE REPASO m = 1.5 /s T1 = 350 º P1=2 a) Calcular W = ? b) Represente el proceso en un diagrama P-v (1) W Z1 = 6 1 = 50 / m = 1.5 /s x2= 100 % P2=0.1 Z2 = 3 2 = 200 / a) Vapor de agua b) Tablas del agua
- 4. Ejercicio # 8: UNIDADES I y II: EJERCICIOS DE REPASO m = 1.5 /s T1 = 350 º P1=2 (1) W Z1 = 6 1 = 50 / m = 1.5 /s x2= 100 % P2=0.1 Z2 = 3 2 = 200 / Tablas del agua Entrada a la turbina
- 5. Ejercicio # 8: UNIDADES I y II: EJERCICIOS DE REPASO m = 1.5 /s T1 = 350 º P1=2 (1) W Z1 = 6 1 = 50 / m = 1.5 /s x2= 100 % P2=0.1 Z2 = 3 2 = 200 / Tablas del agua Salida a la turbina
- 6. Ejercicio # 8: UNIDADES I y II: EJERCICIOS DE REPASO m = 1.5 /s T1 = 350 º P1=2 (1) W Z1 = 6 1 = 50 / m = 1.5 /s x2= 100 % P2=0.1 Z2 = 3 2 = 200 / De la ecuación 1 se determina el W W = 655670 J/s = 655.67 kW
- 7. Ejercicio # 9: El aire contenido en un recipiente se comprime mediante un pistón cuasiestáticamente. Se cumple durante la compresión la relación Pv1.25 = ctte. La masa de aire es de 0.1 kg y se encuentra inicialmente a 100 kPa, 20 °C y un volumen que es 8 veces el volumen final. Determinar el calor y el trabajo transferido. Considere el aire como gas ideal. UNIDADES I y II: EJERCICIOS DE REPASO m = 0.1 Aire Gas ideal Compresión T1 = 20º P1=100 Pv1.25 = ctte v1 = 8. v2 Q = ? W = ? DU = Q - W (1) P.v = n.R.T (2) Proceso Politrópico n = 1.25
- 8. Ejercicio # 9: UNIDADES I y II: EJERCICIOS DE REPASO Pv1.25 = ctte m = 0.1 Aire Gas ideal Compresión T1 = 20º P1=100 v1 = 8. v2 Q = ? W = ? DU = Q - W (1) P.v = n.R.T (2) Proceso Politrópico n = 1.25 (4) DU = n * CV * DT (3) Es necesario calcula v1 De (2) v1 = n.R.T1/ P1
- 9. Ejercicio # 9: UNIDADES I y II: EJERCICIOS DE REPASO Pv1.25 = ctte m = 0.1 Aire Gas ideal Compresión T1 = 20º P1=100 v1 = 8. v2 Q = ? W = ? DU = Q - W (1) P.V = n.R.T (2) De Proceso Politrópico n = 1.25 (4) DU = n * CV * DT (3) (5) = 0.1 ∗ 8.314 kPa. 3⁄ . l ∗ 293 100 ∗ 1 # 29 = 0.084 3 De (2) v1 = 8. v2 $ = 0.084 3 8 = 0.0105 3 $ = 100 kPa ∗ 0.0105 3 0.084 3 % .$& = 1345.43
- 10. Ejercicio # 9: UNIDADES I y II: EJERCICIOS DE REPASO Pv1.25 = ctte m = 0.1 Aire Gas ideal Compresión T1 = 20º P1=100 v1 = 8. v2 Q = ? W = ? DU = Q - W (1) P.V = n.R.T (2) n = 1.25 (4) DU = n * CV * DT (3) ' = 1 1.25 − 1 ∗ 100 . 0.084 3 − 1345.43 . 0.0105 3 = −)). *+ ,- De (4) Otra forma de calcularlo
- 11. Ejercicio # 9: UNIDADES I y II: EJERCICIOS DE REPASO Pv1.25 = ctte m = 0.1 Aire Gas ideal Compresión T1 = 20º P1=100 v1 = 8. v2 Q = ? W = ? DU = Q - W (1) P.V = n.R.T (2) n = 1.25 (4) DU = n * CV * DT (3) Otra forma de calcularlo
- 12. Ejercicio # 9: UNIDADES I y II: EJERCICIOS DE REPASO Pv1.25 = ctte m = 0.1 Aire Gas ideal Compresión T1 = 20º P1=100 v1 = 8. v2 Q = ? W = ? DU = Q - W (1) P.V = n.R.T (2) n = 1.25 (4) DU = n * CV * DT (3) Hay que calcular el calor (Q) De (1) Q = DU + W Q = n * CV * DT + W . = 0.1 29 / # ∗ 5 2 . 8.314 / #. ∗ 492.76 − 293 − 22.91 kJ = −2. 3* ,-
- 13. m = 300 CO2 Gas ideal Expansión T1 = 50º V1=10 4 V2 = 30 4 Ejercicio # 10: 300 g de CO2, considerado como gas ideal (Cv = (7/2)*R), se expande desde 10 L y temperatura 50 ºC a 30 L. Calcular el trabajo y la variación de entalpía si el proceso se realiza de forma adiabática y reversiblemente. UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: P*Vk = ctte Proceso Adiabático k = g = Cp/Cv (1)
- 14. m = 300 CO2 Gas ideal Expansión T1 = 50º V1=10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: k = g = Cp/Cv (1) Del formulario Trabajo (W) Proceso adiabático (3) (2) (4)
- 15. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: k = g = Cp/Cv (1) El cambio de entalpía para un gas ideal es: (3) (2) P.V = n.R.T DH = n * CP * DT (4) De la Ley de gas ideal (5) Recordar por definición: n: moles n= masa Peso molecular = m PM (6) Es necesario determinar las presiones P1 y P2, la temperatura T2
- 16. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: Es necesario determinar las presiones P1 y P2, la temperatura T2 De la Ec. (5) P1= n*R*P1 V1 = m ∗ R ∗ T1 PM ∗ V1 Sustituyendo valores en la Ec. (5) P1= 300 g∗ 0,08205 5 ∗ 4 # ∗ ∗ 50+273 K 44 # ∗ 10 L = 18,07 5
- 17. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: Es necesario determinar las presiones P1 y P2, la temperatura T2 Para calcular P2 y T2 usamos las relaciones o ecuaciones del proceso adiabático T2 T1 = V1 V2 8% Es necesario calcular k = g por la Ec. (1) (7) P2 P1 = V2 V1 %8 (8) k = g = Cp/Cv (1) Cv es dato, pero es necesario calcular Cp
- 18. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: Es necesario determinar las presiones P1 y P2, la temperatura T2 Cv es dato, pero es necesario calcular Cp k = g = Cp/Cv (1) Del formulario: R = Cp - Cv (9) Sustituyendo Cv en la Ec (9): R = Cp - 7 2 *R Cp = R + 7 2 *R Cp = 2 + 7 2 *R Cp = 9 2 *R
- 19. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: Es necesario determinar las presiones P1 y P2, la temperatura T2 k = g = Cp/Cv (1) Sustituyendo valores en la Ec (7): Sustituyendo Cv y Cp en la Ec (1): k = 9 2 *R 7 2 *R = 9 7 = 1,286 T2 T1 = 10 L 30 L 1,286 -1 T2= 50 + 273 ∗ 10 L 30 L 1,286 -1 T2= 235,98
- 20. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: Es necesario determinar las presiones P1 y P2, la temperatura T2 Sustituyendo valores en la Ec (8): P2= 18,07 5 ∗ 30 L 10 L % 1,286 P2= 4,4 5 P2 P1 = 30 L 10 L %1,286 Sustituyendo la Ec (6) y Cv en la Ec (2) ' = m PM ∗ 7 2 ∗R * T2 − T1 (10)
- 21. m = 300 CO2 Gas ideal Expansión T1 = 50º V1 = 10 4 V2 = 30 4 Ejercicio # 10: UNIDADES I y II: EJERCICIOS DE REPASO El proceso es adiabático Cv = (7/2)*R W = ? DH = ? Datos: Sustituyendo valores en la Ec (10) ' = 300 g 44 ; ;<=> ∗ 7 2 ∗ 8,314 ? @ABC∗D * 235,98 − 323 W = - 17264,2 J Sustituyendo valores en la Ec (4) ∆F = 300 44 / # ∗ 9 2 . 8.314 / #. ∗ 235,98 − 323 = −))+*G. 2 -