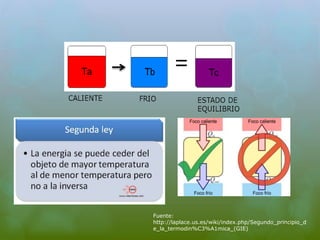
Este documento trata sobre la segunda ley de la termodinámica. Explica conceptos clave como entropía, irreversibilidad y estados de equilibrio. También analiza cómo la segunda ley establece restricciones en la transferencia de energía y la imposibilidad de convertir completamente la energía sin pérdidas.