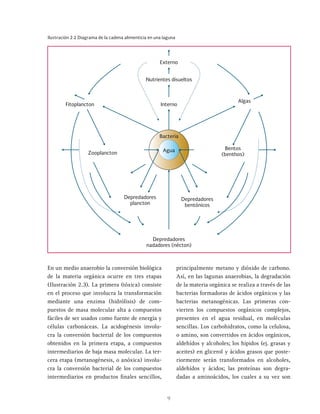
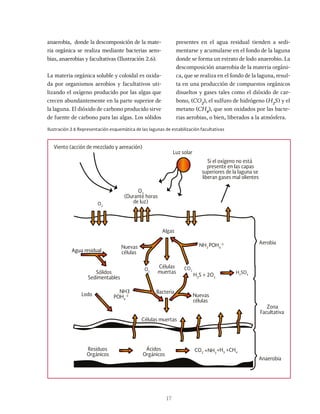
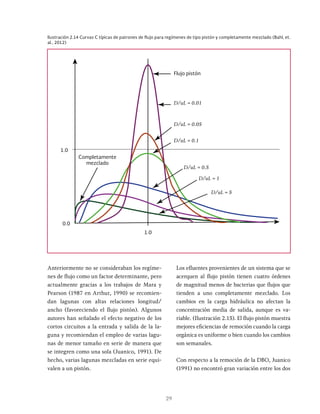
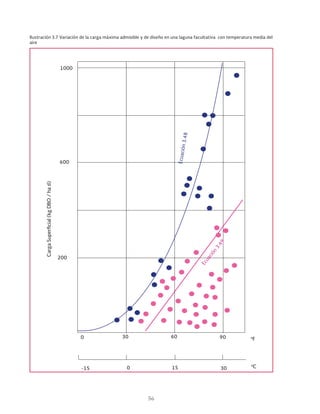
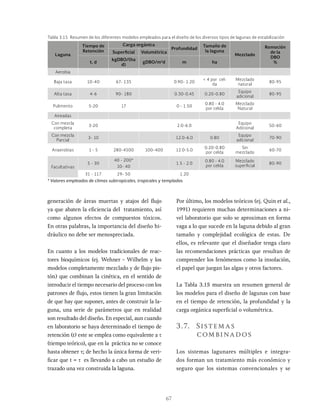
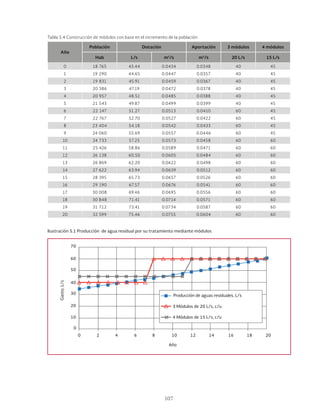
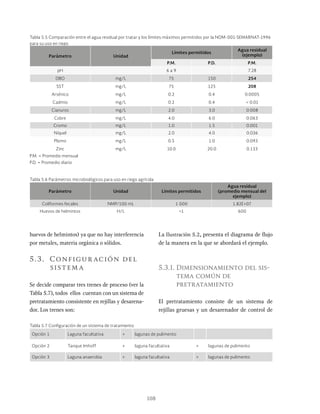
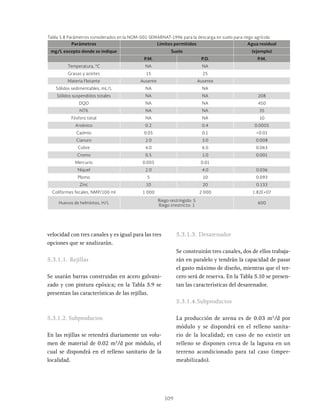
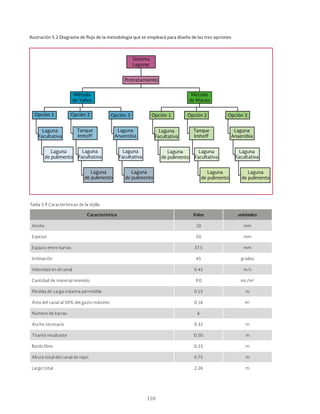
Las lagunas de estabilización son métodos de tratamiento extensivo del agua residual que consisten en el almacenamiento del agua por medio de la actividad bacteriana y las algas. Estas lagunas permiten la estabilización natural de la materia orgánica a través de procesos físicos, químicos y biológicos. Existen diferentes tipos de lagunas como aerobias, anaerobias y facultativas que se clasifican dependiendo de las condiciones de oxígeno presentes.































































![64
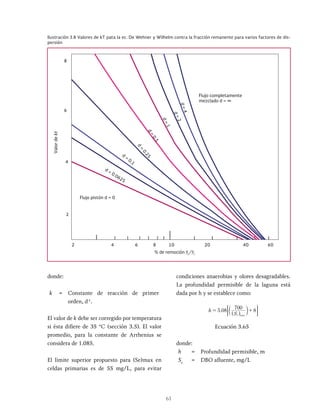
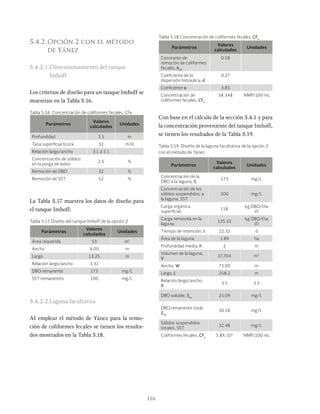
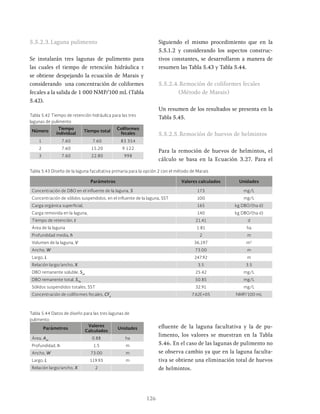
Ilustración 3.9 Fracción de la DBO removida anaerobiamente para diferentes cargas orgánicas (Ouano, 1981)
DBO total removida para una
eficiencia estimada a una
carga dada
900
700
500
300
100
100 300 500 700 900
Aerobia
Anaerobia
DQO
Removida
(kg/ha
d)
Carga (kg/ha d)
DQO del metano producido
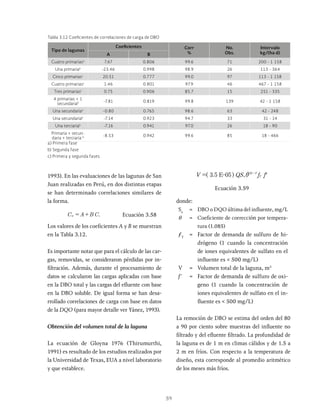
donde:
[Ci
] = concentración del componente i en el
efluente, mg/L
[Cj
] = concentración del componente j en el
influente, mg/L
∑S(j) = suma de todos los mecanismos ciné-
ticos que afectan a dicho componente
Cada uno de estos mecanismos cinéticos se
puede expresar en términos de la concentración
de los diversos componentes en un reactor bio-
químico empleando las constantes específicas.
La combinación de las doce ecuaciones obteni-
das del balance de masa se resuelve mediante
la generación de un sistema de ecuaciones di-
ferenciales de primer orden donde las concen-
traciones de cada compuesto varían a través del
tiempo.
En general, el modelo permite determinar las
constantes o parámetros que generan condiciones
de inestabilidad importantes como son el tiempo
de retención y la carga orgánica. Sin embargo,
la aplicación práctica de este modelo es limitada
debido a que muchas de las constantes deben ser
predeterminadas en laboratorio. Su utilidad prin-
cipal radica en la comprensión de los mecanismos
que intervienen en la operación de las lagunas. La
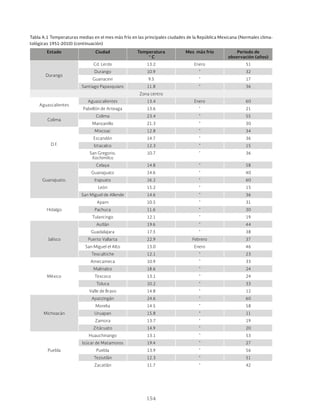
Tabla 3.14 muestra el resumen de los métodos re-
visados para el diseño de las lagunas facultativas.](https://image.slidesharecdn.com/libro27-lagunasdeestabilizacin-230616000414-88dbf8fe/85/Libro27-Lagunas-de-Estabilizacion-pdf-77-320.jpg)















































![142
con reactores biológicos, como reactores anaero-
bios de flujo ascendente o discos biológicos rota-
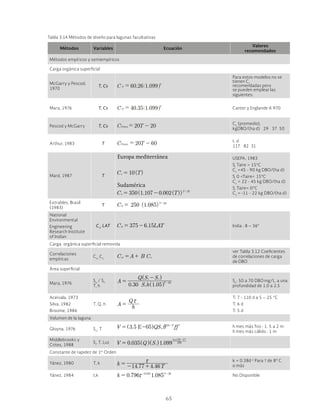
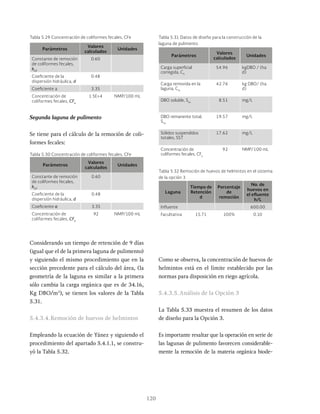
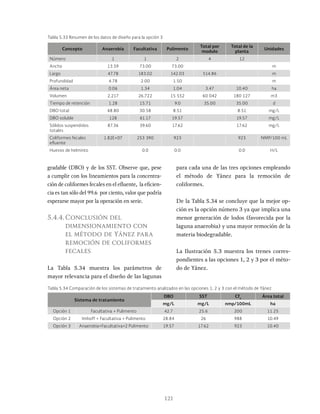
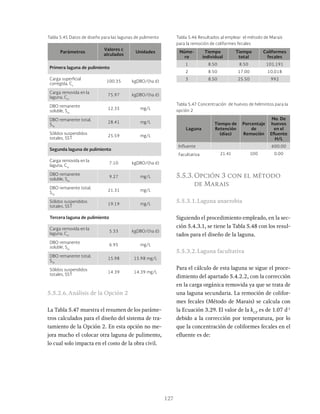
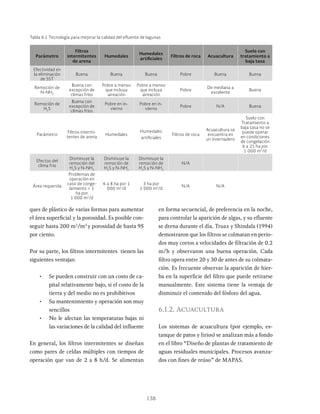
Ilustración 6.5 Concentraciones de nitrógeno total Kjeldahl en un sistema Sutton
Tabla 6.2 Condiciones de operación
Efluente
secundario
Efluente de
laguna
Mes / año
Ago - 81
20
15
10
5
0
Sep - 82 Nov - 83 Dic - 83 Ene - 87 Feb - 88 Abr - 89 May - 90 Jun - 91
Oct - 83
NYK
(mg/L)
Pretratamiento
Operaciones
Desarenación
Cribado
Lagunas Facultativas
Número 2
Superficie 11.1 ha
Tiempo de retención 102 d
Filtración
Número 4
Carga superficial 5625 L/m2
d
Remoción de Fósforo
Reactivos Alúmina
Punto de adición Lagunas o filtros
Características del efluente
DBO 10 10 mg/L
SST 15 15 mg/L
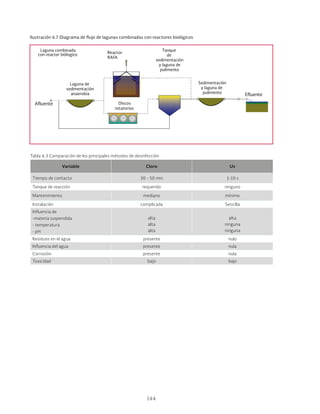
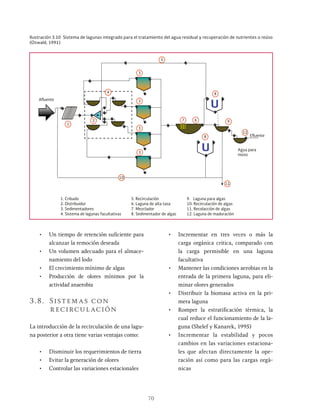
torios. La Ilustración 6.7 muestra el diagrama de
flujo de estos sistemas.
• Una laguna de sedimentación (anaero-
bia) con un volumen equivalente de 0.5
m3
/hab con capacidad para la digestión
anaerobia de los lodos
• Dos unidades de discos biológicos rota-
torios en serie diseñados para nitrificar
[DBO: 4g/(m2
d); N-NH3
: 1 g/(m2
d)]
• Un tanque de sedimentación de alta
tasa para la recirculación de los lodos
biológicos de los discos a la laguna de
sedimentación
• Un sedimentador final y una laguna de
pulimento, con una profundidad de 1 m
y un tiempo de retención hidráulico en-
tre 1 y 5 días](https://image.slidesharecdn.com/libro27-lagunasdeestabilizacin-230616000414-88dbf8fe/85/Libro27-Lagunas-de-Estabilizacion-pdf-155-320.jpg)