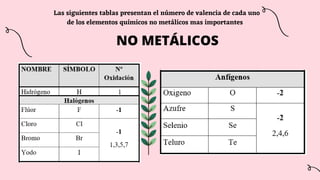
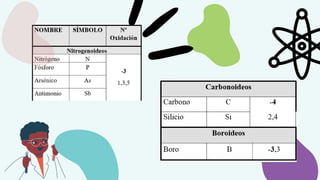
Este documento trata sobre los símbolos químicos, números de oxidación y valencias de los elementos químicos. Explica que los símbolos químicos son abreviaturas del nombre de cada elemento y se derivan principalmente de las letras del nombre en latín. También define las valencias como la capacidad de un átomo para combinarse con otros, y los números de oxidación como la carga que tendría un átomo al combinarse. A continuación, presenta tablas con los números de valencia de elementos no metálicos e información sobre metales y sus números de oxidación