Clase 02 2010 V DesmineralizacióN
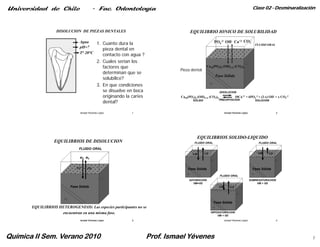
- 1. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización DISOLUCION DE PIEZAS DENTALES EQUILIBRIO IONICO DE SOLUBILIDAD Agua 1. Cuanto dura la PO4-3 OH- Ca+2 CO3- FLUIDO ORAL pH=7 pieza dental en T° 20°C contacto con agua ? 2. Cuales serian los factores que Ca10(PO4)6 (OH)2-X (CO3)X Pieza dental determinan que se Fase Sólida solubilice? 3. 3 En que condiciones se disuelve en boca DISOLUCION originando la caries Ca10(PO4)6 (OH)2-X (CO3)X 10Ca+2 + 6PO4-3 + (2-x) OH- + x CO3-2 dental? SÓLIDO PRECIPITACION SOLUCION Ismael Yévenes López 1 Ismael Yévenes López 2 EQUILIBRIOS SOLIDO-LIQUIDO EQUILIBRIOS DE DISOLUCION FLUIDO ORAL FLUIDO ORAL FLUIDO ORAL V.M V.D V.M V.D M2 M1 F.C F.D Fase Sólida Fase Sólida FLUIDO ORAL SATURACION SOBRESATURACION VM=VD VM > VD Fase Sólida V.M V.D Fase Sólida EQUILIBRIOS HETEROGENEOS: Las especies participantes no se encuentran en una misma fase. HIPOSATURACION VM < VD Ismael Yévenes López 3 Ismael Yévenes López 4 Química II Sem. Verano 2010 Prof. Ismael Yévenes 1
- 2. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización CONSTANTE DEL PRODUCTO DE SOLUBILIDAD [Ca2+] [F-]2 Kps K= [CaF2] [CaF2 ] =cte Ca +2 + 2F- FLUIDO ORAL Kps = [Ca2+] [F-]2 = 3.9 x 10-11 QUE SIGNIFICA ESTE VALOR? SOLUBILIDAD Y Kps CaF2 Solubilidad: cantidad que se disuelve para formar una solución Fase Sólida saturada, se expresa en g/L Solubilidad molar: es el N de moles de soluto que se disuelven Nº en un litro de solución saturada, se expresa en mol/L. Solubilidad Solubilidad Concentración Kps molar molar de iones Ca F2(s) Ca+2 (ac) + 2F -(ac) g/L mol/L. Ismael Yévenes López 5 Ismael Yévenes López 6 SOLUBILIDAD Y Kps FACTORES QUE AFECTAN LA SOLUBILIDAD NaF (ac) ION COMUN Ejercicio: Si el Kps de CaF2 es 3.9 x 10-11 cual es la solubilidad en g/L Ca +2 + 2F- FLUIDO ORAL Ca F2(s) Ca+2 (ac) + 2F -(ac) sM 2s M Kps = [Ca2+] [F-]2 = s x (2s)2 = 4s3 = 3.9 x 10-11 s = 2.1 x 10-4 M solubilidad molar CaF2 Fase Sólida Solubilidad: 2.1 x 10-4 mol CaF2 x 78.1 g CaF2 L mol CaF2 Solubilidad= 1.6 x 10-2 g/L Ca F2(s) Ca+2 (ac) + 2F -(ac) Ismael Yévenes López 7 Ismael Yévenes López 8 Química II Sem. Verano 2010 Prof. Ismael Yévenes 2
- 3. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización La adición de NaF en solución al sistema produce una ¿Qué pasaría en la cavidad bucal con la solubilidad de las piezas modificación desplazando el equilibrio en la reacción hacia la dentales si agregamos o utilizamos fluoruros solubles? izquierda, reduciendo la solubilidad del fluoruro de calcio. En general la adición de un soluto que aporta un ion común Ejercicio 3:Cual es la solubilidad molar del CaF2 en una disolución hace disminuir la solubilidad de una sal poco soluble. ace dis i ui u a que contiene Ca(NO3)2 0 01 M 0.01 ¿Qué pasaría si agregáramos una sal soluble de calcio? Kps = [Ca2+] [F-]2 = 3.9 x 10-11 Solubilidad Ca F2 M 10-4 Ca F2(s) Ca+2 (ac) + 2F -(ac) Inicio 0.01 M 0 10-6 Reacción xM 2x M Equilibrio (0.01 + x) M 2x M 10-8 8 Kps = [Ca2+] [F-]2 = 3.9 x 10-11 = (0.010+x) (2x)2 0 0.1 0.2 Concentración Na F 3.9 x 10-11 = (0.010) (2x)2 M x = 3.1 x 10-5 M La figura nos muestra como disminuye la solubilidad del CaF2 a Solubilidad en agua:2.1 x 10-4 M, la solubilidad molar del CaF2 disminuye 10 medida que se agrega NaF a la solución. veces en presencia de una concentración 0.01 M en calcio. Ismael Yévenes López 9 Ismael Yévenes López 10 SOLUBILIDAD Y pH. ¿Cómo se afectara la solubilidad anterior en presencia de 0.01 M en fluoruro? H+ (ac) Protones Ca F2(s) Ca+2 (ac) + 2F - (ac) Inicio 0 0.01 M Reacción xM 2x M FLUIDO ORAL Equilibrio xM (0.01+2x) M Kps = [Ca2+] [F-]2 = 3.9 x 10-11 = (x) (0.01+2x)2 3.9 x 10-11 = x(0.010)2 x = 3.9 x 10-7 M CaF2 Fase Sólida Solubilidad S l bilid d en agua:2.1 x 10-4 M, se observa entonces que l 2 1 10 4 M b t la solubilidad molar del fluoruro de calcio disminuye 1000 veces en presencia de una concentración 0.01 M en fluoruro. ¿Por qué es mayor el efecto del fluoruro sobre la solubilidad del fluoruro de calcio? Ca F2(s) Ca+2 (ac) + 2F -(ac) Ismael Yévenes López 11 Ismael Yévenes López 12 Química II Sem. Verano 2010 Prof. Ismael Yévenes 3
- 4. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización SOLUBILIDAD Y pH. Ca F2(s) + 2H+ (ac) Ca+2 (ac) + 2HF (ac) La solubilidad de un compuesto iónico cambia si la solución se hace suficientemente acida o básica. Solubilidad Ca F2 x 10-3 M Efecto del pH sobre el CaF2 6 Ca F2(s) Ca+2 (ac) + 2F -(ac) 4 El fluoruro (F -) es la base conjugada del HF , por lo tanto cuando el medio se 2 acidifica, se produce la protonación del anion para formar HF. Al disminuir el F- el sistema tiende a reponerlo disolviendo mas Ca F2(s). 7 3 1 pH El proceso de disolución se puede entender en términos de dos reacciones que ocurren simultáneamente: La figura muestra como cambia la solubilidad del Ca F2(s) con el pH . Otras sales con aniones básicos como el CO3-2, PO4-3, CN- se Ca F2(s) Ca+2 (ac) + 2F -(ac) Ecuación 1 comportaran en forma análoga. F -(ac) + H+ (ac) HF (ac) Ecuación 2 Regla general: la solubilidad de las sales poco solubles que Contienen aniones básicos aumenta a medida que el pH baja. Sumando 1 + 2 Ismael Yévenes López 13 Ismael Yévenes López 14 INTERACCIONES ELEMENTOS DENTARIOS ESMALTE COMO SISTEMA QUIMICO Y FLUIDO BUCAL TRANSPORTE REACCIONES MOL.. E IONES INTERCAMBIO DESMINERALIZACION Interacciones Fco-químicas SALIVA- DENTINA SALIVA-OHA REMINERALIZACION Fluido Bucal Biomoléculas REACCIONES SUP. Fluido Bucal ESMALTE-COMP. Esp. iónicas ORGANICOS Elementos E. covalentes Dentarios Bacterias FASE SÓLIDA Sistema Heterogéneo Ismael Yévenes López 15 Ismael Yévenes López 16 Química II Sem. Verano 2010 Prof. Ismael Yévenes 4
- 5. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización INTERACCIONES FASE SÓLIDA- FUIDO ORAL DISOLUCION DEL ESMALTE FLUIDO ORAL VARIABILIDAD ACIDOS IONES COMPONENTES FASE LIQUIDA F.C F.D FOSFATOS DE CALCIO FDC VARIABILIDAD Ca / P FOSFATOS DE CALCIO FASE MINERAL 1.00 Fase Sólida ESMALTE EQUILIBRIOS Ca / P INSTANTANEOS 1.67 OHA-CO3 Ismael Yévenes López 17 Ismael Yévenes López 18 EQUILIBRIO ACIDO FOSFORICO Y SUS SALES FOSFATOS DE CALCIO PRESENTE EN SALIVA, Y FLUIDOS ORALES CRISTALES MONOCLINICOS FINOS H2PO4- SOLUBILIDAD SE INCREMENTA CON pH < 6 K1 O BRUSHITA SOLUCIONES ACIDAS K2 H3PO4 HO - P - OH HPO42- PRESENTE EN CaHPO4 2H20 Kps = 2.77 x 10-7 HUESOS, HUESOS OH K3 PO43- DIENTES PRESENTE EN CARIES Y Y CALCULOS CALCULOS DENTALES POR HIDRÓLISIS ORIGINA OHA Ismael Yévenes López 19 Ismael Yévenes López 20 Química II Sem. Verano 2010 Prof. Ismael Yévenes 5
- 6. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización DISOLUCION Y EQUILIBRIOS DE FOSFATOS DE CALCIO FOSFATOS DE CALCIO ES UN FOSFATO ACIDO POR EL HPO4-2 Crist. BRUSHITA CaHPO4 2H2O SOLUBILIDAD SE INCREMENTA CON pH < 6 F. OCTOCALCICO Ca8 H2 (PO4)6 5H2O FOSFATO OCTOCALCICO PRESENTE EN CARIES Y WITLOCKITE Ca9 Mg 0,7 Fe0,5 (PO4)6 PO3 OH Ca 8 (HPO4)2 CALCULOS DENTALES (PO4)4 5H2O OHA-CO3 OHA CO3 Ca C 10(PO4)6 (OH)2-X (CO3)X ESTRUCTURA SIMILAR A OHA HIDROXIAPATITA Ca10 (PO4)6 (OH) 2 NO CONTIENE HIDROXILOS FLUORAPATITA Ca10 (PO4) 6 F2 Solub. Ismael Yévenes López 21 Ismael Yévenes López 22 SOLUBILIDAD DE LAS APATITAS PROPIEDADES DE LAS APATITAS 2. FLUORAPATITA S 3. HIDROXIAPATITA O L - 4. BRUSHITA 5. F. OCTOCALCICO U 3 CRISTALES 5 - 1000 nm 5 B 4 I GRAN AREA SUPERFICIAL 2 L - I D SUSTITUCIONES IONICAS A APATITAS D CRISTALES IONICOS - Ca10 (PO4)6 X2 mg/Lt DUROS REFRACTARIOS PTO FUSION ALTO ! ! // ! 0 5 6 7 pH Ismael Yévenes López 23 Ismael Yévenes López 24 Química II Sem. Verano 2010 Prof. Ismael Yévenes 6
- 7. Universidad de Chile - Fac. Odontología Clase 02 - Desminaralización Mecanismo de desmineralización DESMINERALIZACION DE LAS APATITAS Equilibrio sólido-liquido. sólido- Disolución Ca10(PO4)6(OH)2 10 Ca2+ + 6 PO43– + 2 OH– AUMENTACON pH BAJO sólido liquido li id PRODUCTOS REACCIONAN CON H+ Desmineralización Desmineralización PO43– + H+ H PO42– + H+ H2 PO4– Desmineralización MAYOR AFINIDAD DEL H+ POR OH- APATITAS MAYOR DESMINERALIZACION Solubilidad de las apatitas en medios ácidos. DE OHA • En medio ácido se provoca una reacción de neutralización que p q solubiliza material sólido. 1. PO43- + H+ HPO42- + H2P04- • En medio alcalino se desplaza la reacción en sentido contrario, 2. F- + H+ HF depositándose material por precipitación. 3. OH- + H+ H 2O Ismael Yévenes López 25 Ismael Yévenes López 26 VELOCIDAD DE DISOLUCION DE APATITAS Aumenta: - TAMAÑO PARTICULAS - N° IMPERFECCIONES VELOCIDAD DISOLUCION Disminuye: APATITAS IMPUREZAS -IMPUREZAS ESPECIFICAS - MATERIAL DISUELTO PERMANECE Ismael Yévenes López 27 Química II Sem. Verano 2010 Prof. Ismael Yévenes 7
