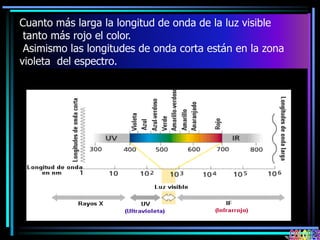
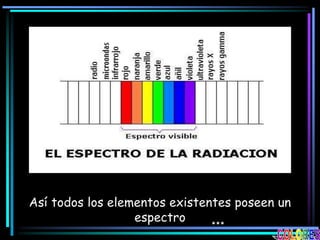
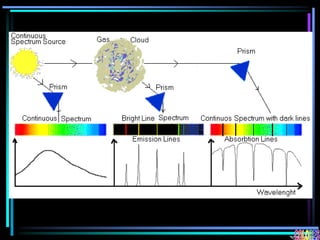
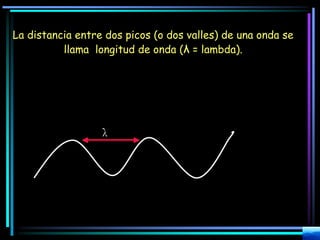
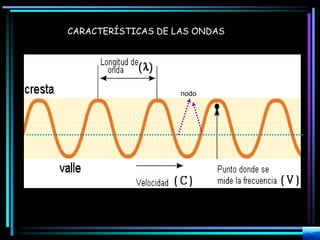
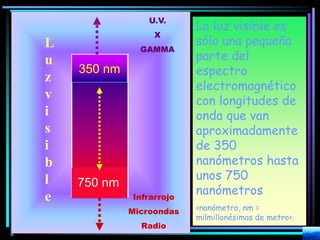
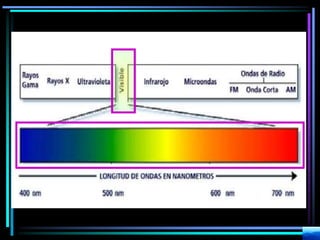
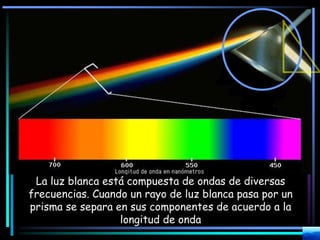
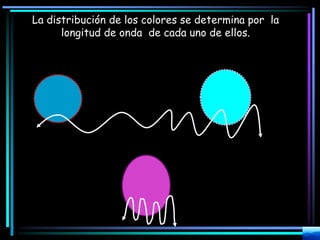
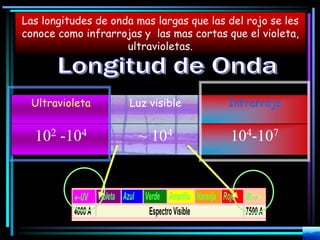
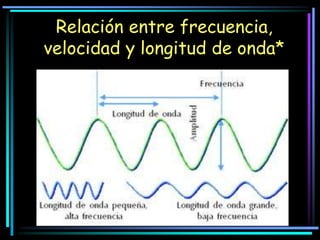
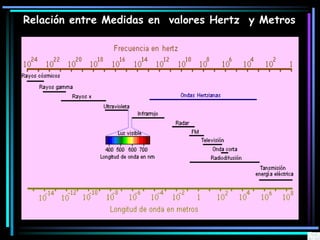
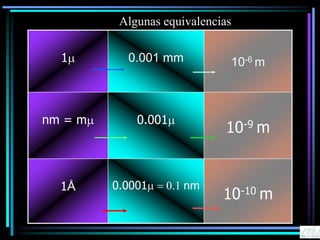
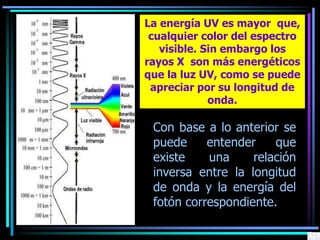
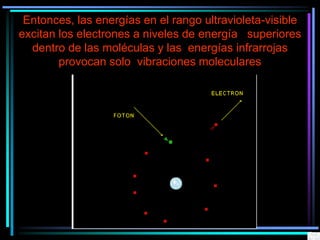
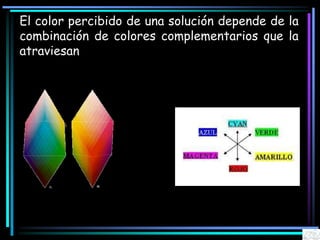
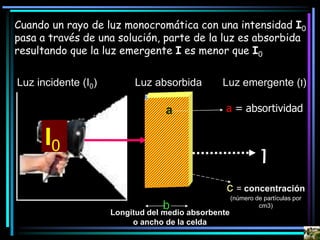
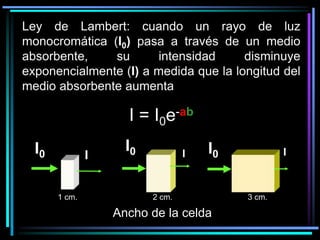
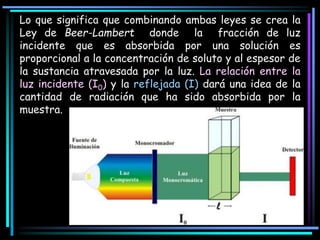
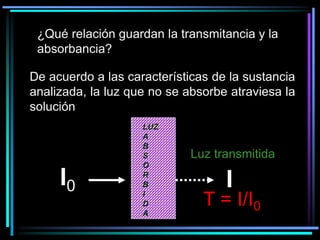
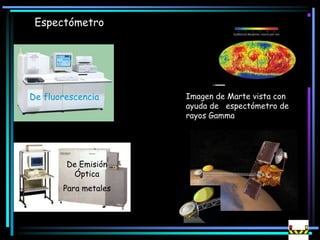
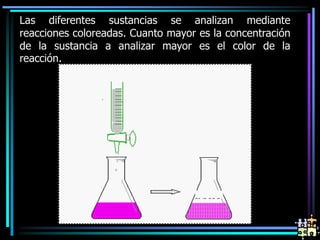
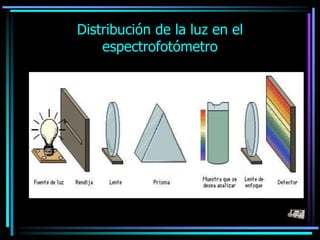
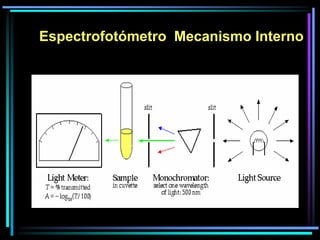
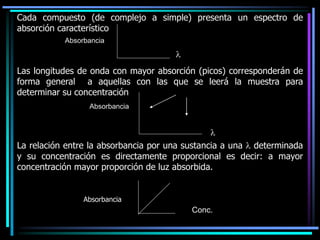
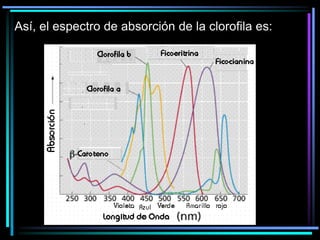
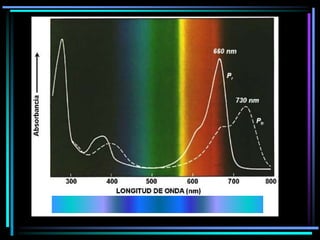
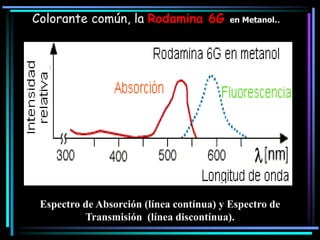
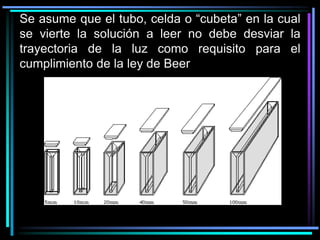
La espectroscopia es el estudio del espectro de la luz emitida por sustancias y elementos. Mediante este estudio se puede conocer la composición de los objetos. La luz tiene naturaleza dual como onda y como partículas llamadas fotones. La longitud de onda y la frecuencia de la luz están inversamente relacionadas. La absorción de la luz depende de la estructura molecular y se rige por las leyes de Beer-Lambert.