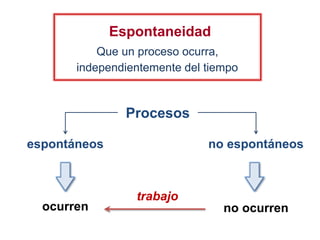
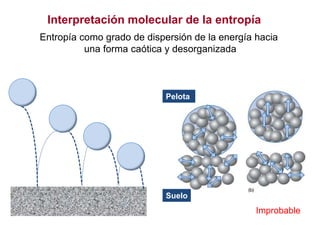
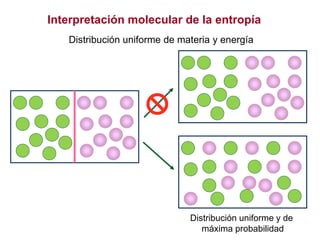
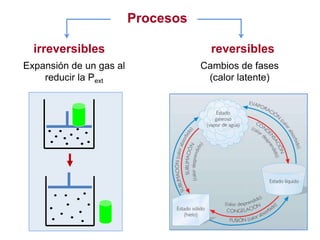
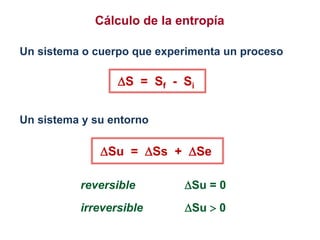
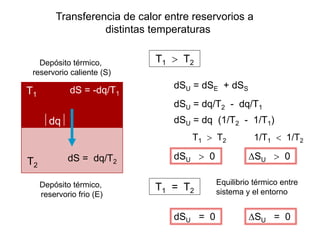
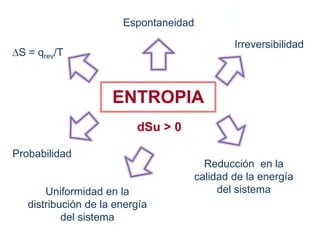
El documento resume los principales conceptos relacionados con la entropía según la termodinámica. Explica que la entropía de un sistema aislado siempre aumenta en los procesos espontáneos e irreversibles, mientras que se mantiene constante en los procesos reversibles. También describe cómo la entropía representa la dispersión o distribución uniforme de la energía de un sistema, lo que reduce la calidad de esta energía y aumenta la probabilidad en el sistema. Además, resume las formulaciones matemáticas del segundo principio de la termod