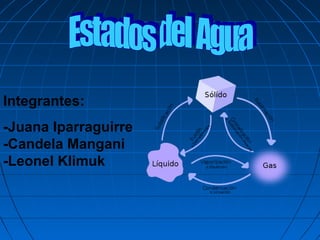
Estados de la materia: sólido, líquido y gas
- 2. El estado líquido es un estado de agregación de la materia intermedio entre el estado sólido y el estado gaseoso. Las moléculas de los líquidos no están tan próximas como las de los sólidos, pero están menos separadas que las de los gases. Las moléculas en el estado líquido ocupan posiciones al azar que varían con el tiempo. Las distancias intermoleculares son constantes dentro de un estrecho margen. En algunos líquidos, las moléculas tienen una orientación preferente, lo que hace que el líquido presente propiedades anisótropas (propiedades, como el índice de refracción, que varían según la dirección dentro del material).
- 3. Un cuerpo sólido es uno de los cuatro estados de agregación de la materia (siendo los otros gas, líquido, Plasma y el Bose-Einstein), se caracteriza porque opone resistencia a cambios de forma y de volumen. Sus partículas se encuentran juntas y correctamente ordenadas. Las moléculas de un sólido tienen una gran cohesión y adoptan formas bien definidas. Existen varias disciplinas que estudian los sólidos: La física del estado sólido estudia de manera experimental y teórica la materiacondensada, es decir, de líquidos y sólidos que contengan más de 1019 átomos en contacto entre sí1 La mecánica de sólidos deformables estudia propiedades microscópicas desde la perspectiva de la mecánica de medios continuos (tensión, deformación, magnitudes termodinámicas, &c.) e ignora la estructura atómica interna porque para cierto tipo de problemas esta no es relevante. La ciencia de los materiales se ocupa principalmente de propiedades de los sólidos como estructura y transformaciones de fase. La química del estado sólido se especializa en la síntesis de nuevos materiales.
- 4. Se denomina gas al estado de agregación de la materia en el cual, bajo ciertas condiciones de temperatura y presión, sus moléculas intereaccionan sólo débilemente entre sí, sin formar enlaces moleculares adoptando la forma y el volumen del recipiente que las contiene y tendiendo a separarse, esto es, expandirse, todo lo posible por su alta energía cinética) . Los gases sonfluidos altamente compresibles, que experimentan grandes cambios dedensidad con la presión y la temperatura. Las moléculas que constituyen un gas casi no son atraídas unas por otras, por lo que se mueven en el vacío a gran velocidad y muy separadas unas de otras, explicando así las propiedades: Las moléculas de un gas se encuentran prácticamente libres, de modo que son capaces de distribuirse por todo el espacio en el cual son contenidos. Las fuerzas gravitatorias y de atracción entre las moléculas son despreciables, en comparación con la velocidad a que se mueven las moléculas. Los gases ocupan completamente el volumen del recipiente que los contiene. Los gases no tienen forma definida, adoptando la de los recipientes que las contiene. Pueden comprimirse fácilmente, debido a que existen enormes espacios vacíos entre unas moléculas y otras. Son gases a temperatura y presión ambientales los siguientes elementos el hidrógeno, el oxígeno el nitrógeno el cloro el flúor y los gases nobles.