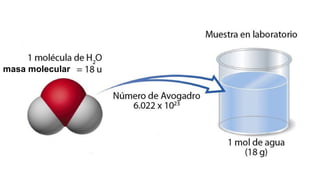
Este documento trata sobre la estequiometría y las unidades químicas. Explica conceptos como masa atómica, isótopos, masa atómica relativa, masa molecular, mol, número de Avogadro, masa molar y volumen molar. También cubre temas como composición porcentual, densidad y análisis cuantitativo para determinar la composición de compuestos. Incluye ejemplos y ejercicios para aplicar estos conceptos.