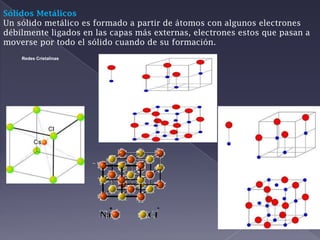
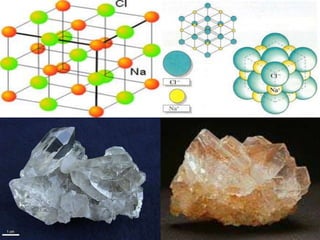
El documento describe varios conceptos clave de la nanotecnología, incluyendo que la nanotecnología involucra el control y manipulación de la materia a escala nanométrica, que un nanómetro equivale a una milmillonésima parte de un metro, y que la nanomedicina permitiría curar enfermedades desde dentro del cuerpo a nivel molecular o celular. También discute aplicaciones como nanotubos de carbono, celdas solares de silicio, y las propiedades de los sólidos cristalinos y amorfos.