Reacciones químicas en nuestra vida
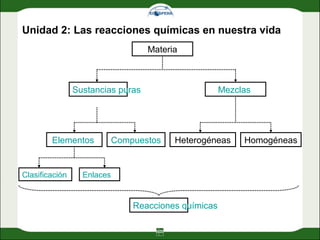
- 1. Unidad 2: Las reacciones químicas en nuestra vida Materia Sustancias puras Homogéneas Mezclas HeterogéneasCompuestosElementos Clasificación Enlaces Reacciones químicas
- 2. Sustancias puras • Son aquellas que tienen propiedades físicas y químicas constantes, una composición fija, y que no se pueden descomponer en sustancias más simples por métodos físicos.
- 3. Elementos químicos • Los elementos químicos son sustancias puras que no pueden descomponerse en sustancias más simples, ya sea por métodos físicos o químicos. • Los elementos son las sustancias más simples de la materia, y es a partir de ellos que se forman todas las demás. A nivel microscópico, cada elemento se compone de un solo tipo de átomo. • Cada elemento se representa mediante un símbolo químico, que corresponde a una, dos o tres letras; generalmente tomadas del nombre de origen del elemento. La primera letra siempre es mayúscula y la o las siguientes, son minúsculas.
- 4. Clasificación de los elementos químicos • Al estudiar los elementos químicos, se ha descubierto que algunos de ellos tienen propiedades en común. Según estas propiedades, los químicos los han agrupado en tres categorías: metales, metaloides y no metales. • Todos los elementos que se conocen actualmente se encuentran ordenados según su número atómico en la llamada tabla periódica o sistema periódico de los elementos. En esta tabla, los elementos están distribuidos en siete filas llamadas períodos, y dieciocho columnas denominadas grupos. Los elementos pertenecientes a un mismo grupo o período presentan propiedades similares.
- 6. Tipo de elementos Características Ejemplos Metales Generalmente son sólidos a temperatura ambiente, poseen brillo metálico, son buenos conductores del calor y la electricidad, son dúctiles y maleables y presentan resistencia a la ruptura. Cobre, zinc, plomo Metaloides Son sólidos a temperatura ambiente, la mayoría posee brillo metálico y, por lo general, son muy duros. Son semiconductores. Silicio, arsénico, antimonio No metales A temperatura ambiente, se presentan como sólidos, líquidos o gases. No son dúctiles ni maleables y son malos conductores del calor y la electricidad. Algunos presentan colorido, pero no brillo metálico. Azufre, yodo, grafito.
- 7. Compuestos químicos • Los compuestos son sustancias formadas por dos o más elementos, que se encuentran unidos entre sí mediante enlaces químicos. • Los elementos que constituyen compuestos, no se pueden distinguir a simple vista y la proporción en que se combinan los elementos es siempre fija o constante. Los compuestos, se pueden descomponer en sus elementos constituyentes por métodos químicos. • Se representan mediante fórmulas químicas, que son una combinación de símbolos químicos que representan los elementos que están presentes en el compuesto. Comúnmente, las fórmulas contienen números para indicar la cantidad de átomos de cada elemento en el compuesto.
- 8. Reacciones químicas • Una reacción química es un proceso a través del cual una o más sustancias se transforman originando nuevas sustancias. • En las reacciones químicas a las sustancias iniciales se les denomina reactantes, y a las nuevas, productos. •
- 9. ¿cuando se producen? Existen algunos fenómenos característicos que indican que una reacción química se está produciendo: liberación de gases cambios de color formación de sólidos liberación de calor
- 10. Teoría de las colisiones • Para que ocurra una reacción química, las moléculas de los reactantes deben colisionar entre sí con la energía suficiente para que se produzca la ruptura de enlaces en los reactantes, y el reordenamiento de los átomos mediante nuevos enlaces que darán origen a los productos.
- 11. Esquema de representación de la Teoría de las colisiones.
- 12. - ¿Qué sucede con las moléculas de los reactantes al ocurrir la reacción? - ¿Cómo es la cantidad de cada elemento (pelotitas de colores) en los reactantes y productos?
- 13. Clasificación de reacciones químicas Según el ordenamiento molecular – Reacciones de combinación: Son aquellas en las que dos o más sustancias se combinan para producir un único compuesto. De manera general, estas reacciones se representan mediante la siguiente expresión: A + B C
- 14. – Reacciones de descomposición: Son aquellas en las que un compuesto se descompone en sustancias más sencillas, generalmente elementos. Estas reacciones se representan, de manera general, a través de la expresión: – Reacciones de sustitución simple: Son aquellas en las que un elemento desplaza a otro elemento que forma parte de un compuesto. Estas reacciones se representan mediante la expresión: AB A + B A + BC AC + B
- 15. – Reacciones de sustitución doble: Son aquellas en las que dos compuestos intercambian elementos para formar nuevas sustancias. Estas reacciones se representan, de manera general, mediante la expresión: AB + CD AC + BD
- 16. Según la energía – Reacciones endergónicas. Son aquellas reacciones químicas que necesitan el aporte de energía externa para que ocurra la transformación de los reactantes en productos. Estas reacciones se representan mediante ecuaciones químicas de la forma: Si la reacción necesita energía en forma de calor (energía térmica), se denomina endotérmica. A + B + Energía C + D
- 17. – Reacciones exergónicas: Son aquellas reacciones químicas que liberan energía al medio durante la transformación de los reactantes en productos. Estas reacciones se representan a través de ecuaciones químicas de la forma: Si la reacción libera energía en forma de calor (energía térmica), se denomina exotérmica. A + B C + D + Energía