Carbono
•Descargar como PPTX, PDF•
0 recomendaciones•196 vistas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (18)
Propiedades físicas y químicas del carbono e hidrogeno

Propiedades físicas y químicas del carbono e hidrogeno
Propiedades físicas y químicas del carbono e hidrogeno

Propiedades físicas y químicas del carbono e hidrogeno
Destacado
Destacado (20)
Instalación y Configuración : Bases de datos fuera del asistente 

Instalación y Configuración : Bases de datos fuera del asistente
Flavio Cattaneo: la Presentazione 1H 2010 Consolidated Results

Flavio Cattaneo: la Presentazione 1H 2010 Consolidated Results
Incentivando o uso de jogos com auxilio de novas tecnologias (TICs).

Incentivando o uso de jogos com auxilio de novas tecnologias (TICs).
Similar a Carbono
Similar a Carbono (20)
El diamante es uno de los alótropos del carbono mejor conocidos

El diamante es uno de los alótropos del carbono mejor conocidos
Clasificacion de los elementos quimicos Mayra Chadán UCE

Clasificacion de los elementos quimicos Mayra Chadán UCE
Más de Pamela Villarroel Palacios
Más de Pamela Villarroel Palacios (10)
Carbono
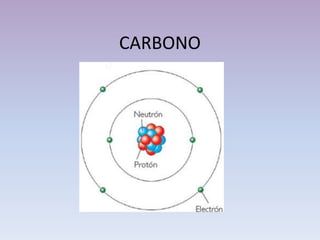
- 1. CARBONO
- 2. • Podemos encontrar el carbono en tres variedades alotrópicas: diamante, grafito y carbono amorfo que son sólidos con puntos de fusión sumamente altos y son insolubles en todos los disolventes a temperaturas ordinarias. Las propiedades físicas de las tres formas difieren ampliamente a causa de las diferencias en la estructura cristalina. En el diamante, una de las sustancias más duras conocidas, cada átomo se vincula a otros cuatro átomos en una estructura tridimensional. Es incoloro y no conduce la electricidad.
- 3. Masa Atómica 12,0107 uma Punto de Fusión 3800 K Punto de Ebullición 5100 K Densidad 3513 kg/m³ Dureza (Mohs) 0,8 (grafito) Potencial Normal de Reducción + 0,52 V CO | C solución ácida Conductividad Térmica 1,59 J/m s ºC Conductividad Eléctrica 0,7 (mOhm.cm)-1 Calor Específico 689,70 J/kg ºK Calor de Vaporización 355,8 kJ/mol Calor de Atomización 717,0 kJ/mol de átomos Estados de Oxidación -4, -3, -2, -1, +1, +2, +3 , +4 1ª Energía de Ionización 1086,4 kJ/mol 2ª Energía de Ionización 2352,6 kJ/mol 3ª Energía de Ionización 4620,4 kJ/mol Afinidad Electrónica 153,9 kJ/mol Radio Atómico 0,914 Å Radio Covalente 0,77 Å Radio Iónico C-4 = 2,60 Å C+4 = 0,15 Å Volumen Atómico 4,58 cm³/mol Polarizabilidad 1,8 ų Electronegatividad (Pauling) 2,55 Valores de las Propiedades Regresar
