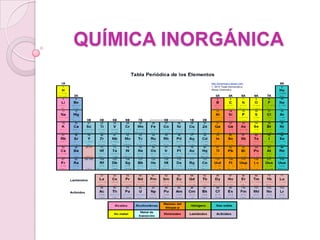
Química inorgánica
- 2. Introducción Historia En 1780 Lavoisier junto con otros tres químicos franceses, Guyton de Morveau, Berthollet y Fourcony inician la creación de un sistema de nomenclatura más lógico y racional que sustituya al heredado de los alquimistas. La empresa ve la luz cuando Lavoisier publica su Tratado Elemental de Química en el que expone de forma organizada y sistemática la nueva nomenclatura. A principios del siglo XIX, Berzelius asigna a cada elemento un símbolo que coincide con la inicial del nombre en latín. Así pues, las fórmulas de las sustancias consistirían en una combinación de letras y números que indican el número de átomos de cada elemento.
- 3. ANTOINE LAVOISIER Químico francés, padre de la química moderna. Orientado por su familia en un principio a seguir la carrera de derecho, recibió una magnífica educación en el Collège Mazarino, en donde adquirió no sólo buenos fundamentos en materia científica, sino también una sólida formación humanística. Ingresó luego en la facultad de derecho de París, donde se graduó en 1764, por más que en esta época su actividad se orientó sobre todo hacia la investigación científica. La especulación acerca de la naturaleza de los cuatro elementos tradicionales (aire, agua, tierra y fuego) lo llevó a emprender una serie de investigaciones sobre el papel desempeñado por el aire en las reacciones de combustión. Lavoisier presentó a la Academia los resultados de su investigación en 1772, e hizo hincapié en el hecho de que cuando se queman el azufre o el fósforo, éstos ganan peso por absorber «aire», mientras que el plomo metálico formado tras calentar el plomo mineral lo pierde por haber perdido «aire». La ley de conservación de la masa o primera ley ponderal lleva su nombre.
- 4. Nomenclatura Es el lenguaje empleado para designar a los cuerpos simples y compuestos. Nomenclatura Tradicional Nomenclatura STOCK Indica la función y el nombre especifico que indica el metal. Usa prefijos como hipo, per, meta, piro, orto y sufijos como oso, ico, ito, ato, uro. Ejm: All3 Yoduro de Aluminio Utilización de números romanos escritos a continuación del metal. Ejm: All3 Yoduro de Aluminio (III) Nomenclatura Sistemática Indica el número de átomos en la fórmula, por medio de prefijos como: mono, di, tri, tetra, penta, hexa, etc. Ejm: FeCl3 tricloruro de hierro
- 5. Número de Oxidación y Valencia Valencia Número de Oxidación Es el número que expresa la capacidad de combinarse con otros para formar un compuesto. Es siempre un número positivo. Es un número entero que representa el número de electrones que un átomo gana o pierde cuando forma un compuesto determinado.
- 6. Número de oxidación por elementos: Metales de Valencia Fija Número de Oxidación +1 Número de Oxidación +2 Número de Oxidación +3 Número de Oxidación +4 Número de Oxidación +6 Hidrogeno (H) Litio(Li) Berilio (Be) Calcio (Ca) Aluminio (Al) Bismuto (Bi) Hafnio (Hf) Osmio (Os) Molibdeno (Mo) Sodio (Na) Potasio (K) Bario (Ba) Radio (Ra) Disproncio(Dy ) Erbio (Er) Iridio (Ir) Platino (Pt) Uranio (U) Rubidio (Rb) Cesio (Cs) Estroncio (Sr) Magnesio (Mg) Europio (Eu) Escandio (Sc) Paladio (Pd) Rutenio (Ru) Wolframio (W) Francio (Fr) Plata (Ag) Zinc (Zn) Cadmio (Cd) Galio (Ga) Gadolinio (Gd) Rodio (Rh) Torio (Th) Lantano (La) Lutencio (Lu) Zirconio (Zr) Radical Amonio (NH4) Neodimio (Nd) Indio (In) Iterbio (Yb) Itrio (Y)
- 7. Metales de Valencia Variable Número de Oxidación +1, +2 Número de Oxidación +1, +3 Número de Oxidación +2, +3 Número de Oxidación +2, +4 Número de Oxidación +3, +4 Número de Oxidación +3, +5 Número de Oxidación +4, +6 Cobre (Cu) Mercurio (Hg) Oro (Au) Talio(Ta) Hierro (Fe) Níquel (Ni) Plomo (Pb) Estaño (Sn) Cerio (Ce) Praseodimi o (Pr) Niobio (Ni) Tantalio (Ta) Tecnecio (Tc) Cromo (Cr) Cobalto (Co) Polonio (Po) Manganes o (Mn) Vanadio (V)
- 8. No Metales Halógenos (-1), +1, +3, +5, +7 Anfígenos (-2), +4, +6 Nitrogenoides (-3), +3, +5 Carbonoides (-4), +4 Flúor (F) Cloro (Cl) Oxígeno (O) Azufre (S) Nitrógeno (N) Fosforo (P) Carbono (C) Silicio (Si) Bromo (Br) Yodo (I) Selenio (Se) Teluro (Te) Arsénico (As) Antimonio (Sb) Germanio (Ge) Ástato (At) Ciano (CN) Boro (B)
- 9. Compuestos Binarios Óxidos Óxidos Ácidos (Anhídridos) Óxidos Básicos Formación: No metal + oxígeno Formación: Metal + oxígeno Peróxidos Formación: Un oxido metálico + un átomo de oxígeno. Hidruros Metálicos Formación: Metal + hidrogeno Hidruro de litio Óxido de carbono (IV) Anhídrido carbónico Hidruros no metálicos (Volátiles) Formación: Hidrogeno + elementos del grupo nitrógeno, del carbono o el boro
- 10. Compuestos Binarios Óxidos Salino s Formación: Sumatoria de 2 óxidos metálicos de un mismo metal de valencia variable Ácidos Hidrácidos Formación: No metales (monovalente s-divalentes) + hidrogeno Compuestos Especiales Formación: No metales (tri-tetra) + Hidrogeno Aleacione s Sales Binarias Formación: Suma de 2 metales diferentes Formación: Un metal + un no metal o dos metales entre sí.
- 11. Ácidos Oxácidos Sal Oxisal Neutra Compuesto s Terciarios Formación: Anhídrido + Agua Formación: Ácidos Oxácidos + hidrácidos o Radicales Halogenicos + metales Sal Halógena ácida Formación: Ácidos Hidrácidos de la familia VIA + Hidróxido Sal Halógena doble Formación: 1ácido hidrácido + 2 hidróxidos de diferentes metal Sales Oxisales Neutras Formación: Ácido oxácido + hidróxido Hidróxidos Metálicos Formación: Metales + (OH) o óxidos metálicos + agua
- 12. Compuestos Cuaternarios Sales Ácidas Sales Básicas Formación: Ácidos oxácidos con 2 o más hidrógenos + hidróxidos metálicos Formación: Ácidos oxácidos + hidróxidos metálicos Sal de Mohr Bicarbonato de sodio NaHCO3
- 13. Reacción Química Es el proceso en el que una o más sustancias (reactivos) se transforman en una u otras sustancias (productos) que presentan características diferentes a los reactivos. La forma gráfica de representar una reacción química es por medio de una ecuación química. Ejm: Quemar carbón en el aire. Reacción del hidrogeno con el oxigeno para formar agua. Oxidación del hierro en el aire húmedo. Componentes de una Reacción Química H2SO4(l) + 2NaOH(s) Reactivos Na2SO4(s) + 2H 2O(l) Productos Reactantes o reactivos: Son las sustancias que intervienen en el cambio químico. Productos: Son las sustancias originadas por el cambio de los reactivos
- 14. Tipos de Reacciones Químicas Combinación ÓxidoReducció n Desplazamiento Descomposició n Precipitación Según el intercambio de calor Neutralización Reversibl e Irreversibl e
- 15. Reacciones de Combinación • Es la unión de dos o más sustancias simples para formar otra más compleja. Ejm: • Fe (s) + S (s) FeS (s) Reacciones de Descomposición • Una sustancia se descompone en otras más sencillas. Ejm: • CaCO3 (s) CaO (s) + CO2 (g) Reacciones de doble desplazamiento • Llamadas también metátesis, son reacciones en que se realiza un intercambio entre los átomos o radicales de los reactantes. Ejm: • AgNO3 + NaCl NaNO3 + AgCl Reacciones de desplazamiento • Llamadas también de simple sustitución. Son aquellas en las que un átomo reemplaza a otro de un compuesto. Ejm: • H2SO4 + Zn ZnSO4 + H2 Reacción Exotérmica • Es aquella que se realiza liberando calor. Ejm: • H2SO4 + Zn ZnSO4 + H2 + 37,630 kcal
- 16. Reacción Endotérmica • Es aquella que se realiza absorbiendo calor. Ejm: • 6CO2 + 6H2O + calor C6H12O6 + 6O2 Reacciones Irreversibles • Es cuando tiene tendencia a producirse sólo en un determinado sentido. Ejm: • HCl + NaOH H2O + NaCl Reacciones Reversibles • Son aquellas que se realizan en los dos sentidos. Ejm: • 4HCl + O2 2Cl2 + 2H2O Reacciones de neutralización • Son aquellas que tienen lugar entre un cuerpo de pH ácido con otro de pH básico, dando como resultado una sal de pH neutro (pH= 7). Ejm: • HCl + NaOH NaCl + H2O Reacciones de precipitación • Son reacciones de doble desplazamiento que produce una sustancia insoluble que se denomina precipitado. Ejm: • AgNO3 + NaCl AgCl + NaNO3
