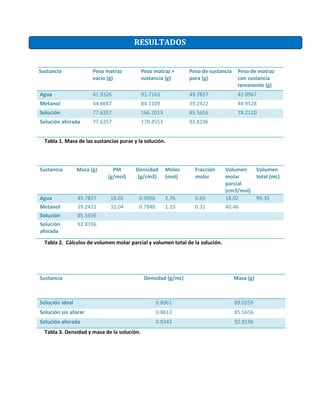
Análisis de resultados de masa, volumen y densidad de sustancias puras y solución
- 1. RESULTADOS Tabla 1. Masa de las sustancias puras y la solución. Tabla 2. Cálculos de volumen molar parcial y volumen total de la solución. Tabla 3. Densidad y masa de la solución. Sustancia Peso matraz vacio (g) Peso matraz + sustancia (g) Peso de sustancia pura (g) Peso de matraz con sustancia remanente (g) Agua 41.9326 91.7163 49.7837 42.0967 Metanol 44.8687 84.1109 39.2422 44.9528 Solución 77.6357 166.2013 85.5656 78.2120 Solución aforada 77.6357 170.4553 92.8196 Sustancia Masa (g) PM (g/mol) Densidad (g/cm3) Moles (mol) Fracción molar Volumen molar parcial (cm3/mol) Volumen total (mL) Agua 49.7837 18.02 0.9956 2.76 0.69 18.02 99.35 Metanol 39.2422 32.04 0.7848 1.23 0.31 40.46 Solución 85.5656 Solución aforada 92.8196 Sustancia Densidad (g/mL) Masa (g) Solución ideal 0.8961 89.0259 Solución sin aforar 0.8613 85.5656 Solución aforada 0.9343 92.8196
- 2. ANEXOS
- 3. Analisis de resultados Los volúmenes molares parciales de las sustancias puras coinciden con el valor de la propiedad molar. Así, en base a los datos obtenidos con cálculos relativamente simples, el volumen molar parcial del agua pura a temperatura ambiente de 26.1C en este caso y 1 atm de presión; Densidad=1g.cm-3 y M=18,015 g.mol-1 es Vmol parc=18,015 cm3mol-1 que es lo mismo que su volumen molar.
- 4. Conclusión El volumen molar de una sustancia pura depende de la naturaleza de las moléculas que rodean a la misma. Por ejemplo, cuando x EtOH = 1 el volumen molar aparente de H2O es de 14 mL/mol y no 18 mL/mol. Entonces 14 mL/mol es el volumen molar parcial del H2O en EtOH. Esto demuestra el postulado inicial de que el volumen molar parcial del soluto está definido y no es nulo aún en el caso del solvente puro, es decir cuando su concentración es cero. Así, por ejemplo, el volumen molar parcial del alcohol en el agua pura no es cero. Estos volúmenes molares parciales, puede decirse que estos dependen de la temperatura y la presión. En este caso se observo que además dependen de la composición de la solución (la fracción molar), pero no de la cantidad de solución puesto que es una propiedad intensiva, definida por mol.
