1 Estequimetria diapositivas.pdf
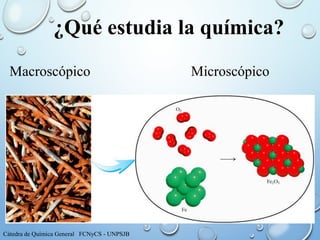
- 1. ¿Qué estudia la química? Macroscópico Microscópico Cátedra de Química General FCNyCS - UNPSJB
- 2. Clasificación de la materia
- 3. Leyes fundamentales de la química Cátedra de Química General FCNyCS - UNPSJB Ley de conservación de la masa (Lavoisier) En toda transformación química la masa se conserva, lo que implica que la suma de las masas de los reactivos es igual a la suma de las masas de los productos de la reacción. Ley de proporciones definidas (Proust) Los elementos se combinan para formar compuestos en una proporción de masa fija y definida
- 4. Cátedra de Química General FCNyCS - UNPSJB Leyes fundamentales de la química Ley de proporciones múltiples (Dalton) Cuando dos elementos se combinan para formar mas de un compuesto, las diferentes masas de un elemento que se combina con una masa fija del otro, guardan entre si una relación de números sencillos
- 5. Teoría de atómica de Dalton Cátedra de Química General FCNyCS - UNPSJB Los elementos están formados por partículas extremadamente pequeñas llamadas átomos Los átomos de un mismo elemento son idénticos, tienen igual tamaño, masa y propiedades químicas. Los átomos de un elemento son diferentes a los átomos de todos los demás elementos Los compuestos están formados por átomos de más de un elemento. Una reacción química incluye solo la separación, combinación o reordenamiento de los átomos; nunca supones la creación o destrucción de los mismos
- 6. Cátedra de Química General FCNyCS - UNPSJB Ley de Avogadro Volúmenes iguales de gases diferentes contienen el mismo número de partículas, a la misma presión y temperatura
- 7. Un mol contiene el número de Avogadro ( 6,02×1023) de unidades de materia físicas reales ( átomos, moléculas o iones) Una molécula es una partícula más pequeña de 1 elemento o compuesto que tiene existencia estable e independiente H2, O2, H2O
- 8. Masa atómica: Es el número que indica las veces que un átomo de un elemento es más pesado que un doceavo del átomo del isótopo de C12. Masa molecular Es el número que indica cuántas veces una molécula es más pesada que un doceavo del átomo del isótopo de C12. Cátedra de Química General FCNyCS - UNPSJB Carbono, Patrón 12,0000 UMA
- 10. Cátedra de Química General FCNyCS - UNPSJB Ejemplo H2O
- 11. Cátedra de Química General FCNyCS - UNPSJB Los elementos se representan mediante símbolos Símbolos, fórmulas Au, Ag, O, H Fórmula de un compuesto indica su composición química H2O, CO2 Fórmulas Moleculares Fórmula Empírica Composición porcentual en masa Composición porcentual de un elemento= n × masa molar del elemento × 100 masa molar del compuesto
- 12. El análisis del propeno gaseoso dio los siguientes resultados: elementos C e H y la composición centesimal C: 85,71% H: 14,29% ¿Cuál será la fórmula empírica y molecular del compuesto?. Se sabe que su masa molar es 42g/mol. En 100 g del compuesto hay: 85,71 g de C 1mol C = 7,14 moles C 12,00 g de C 14,29 g de H 1mol H = 14,29 moles H 1,00 g de H 42 = 3 14 CH2 Fórmula mínima n = g masa molar g formula mínima C3H6 Fórmula molecular 7,14/7,14 = 1 y 14,29/7,14 = 2
- 13. Reacciones y ecuaciones químicas A + B C + D reactivos productos H2 + Cl2 HCl 2 Coeficiente estequiométrico Balanceo Método por tanteo NaHCO3 Na2CO3 + H2O + CO2 2
- 14. Estequiometría
- 15. Cátedra de Química General FCNyCS - UNPSJB 1 mol = MM en gramos
- 16. Aprendemos a convertir moles en moléculas y moles en gramos MASA MOLAR GRAMOS NÚMERO DE AVOGADRO MOL FÓRMULA QUIMICA MOLECULA ÁTOMOS 18 g/mol 90 g de agua 6,02 x 10 23 Mol H2O Molécula Átomos de H y Átomos de O 5 mol 90 g de agu a 3,01 x 10 24 moléculas Mol 6,02 x 10 24 3,01 x 10 24 Moléculas Átomos de H y Átomos de O Cátedra de Química General FCNyCS - UNPSJB
- 17. Método del mol Cátedra de Química General FCNyCS - UNPSJB
- 18. Método del mol Cátedra de Química General FCNyCS - UNPSJB
- 19. Reactivo limitante Es el que se consume completamente Se dispone de 9 moles de sodio y un mol de cloro diatómico. Se pueden formar 2 moles de cloruro de sodio y sobran 7 moles de sodio Reactivo en exceso es el que sobra después que se produce la reacción química Cátedra de Química General FCNyCS - UNPSJB
- 20. 1 mol de reactivo Rendimiento de la reacción El cálculo está basado alrededor del concepto de moles de reactivos vs moles de producto formado !! El rendimiento ignora el uso o la generación de productos indeseables 1 mol de producto rendimiento es del 100% Zn (s) + H2SO4 (aq) ZnSO4(aq) + H2 (g) 1 mol 1 mol 1 mol 1 mol 65,4 g 98 g 161,4 g 2 g Cátedra de Química General FCNyCS - UNPSJB
- 21. Rendimiento ¿Porque el rendimiento teórico no es igual al experimental? Impurezas en los reactivos Pérdidas mecánicas reacciones químicas colaterales Reacciones reversibles reacciones reversibles Reacciones químicas colaterales % de rendimiento = rendimiento real × 100 rendimiento teórico
- 22. Economía atómica Mide en qué medida la totalidad de los átomos disponibles son incorporados al producto final Si todos los reactivos se incorporan al producto final tiene 100% de economía atómica. Se indica así % EA =100
- 23. Cátedra de Química General FCNyCS - UNPSJB