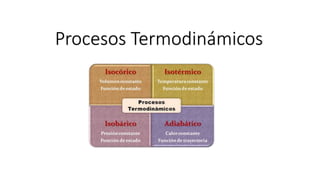
Procesos termodinámicos
- 2. En física, se denomina proceso termodinámico a la evolución de determinadas magnitudes (o propiedades) propiamente termodinámicas relativas a un determinado sistema físico. Desde el punto de vista de la termodinámica, estas transformaciones deben transcurrir desde un estado de equilibrio inicial a otro final; es decir, que las magnitudes que sufren una variación al pasar de un estado a otro deben estar perfectamente definidas en dichos estados inicial y final.
- 3. Proceso Isotérmico Un proceso isotérmico es un cambio de un sistema, en el que la temperatura se mantiene constante. Esto se produce normalmente cuando un sistema está en contacto con un depósito térmico exterior, y el cambio se produce lo suficientemente lento como para permitir que el sistema ajuste continuamente a la temperatura del depósito a través de intercambio de calor. “A una temperatura constante y para una masa dada de un gas, el volumen del gas varia de manera proporcional a la presión absoluta que recibe” Robert Boyle (1627- 1691)
- 4. Aplicaciones en la vida cotidiana La fiebre Cuando prendemos el Hielo derritiéndose aire acondicionado La temperatura del sistema permanece constante, para que permanezca constante las variaciones de presión y volumen deben de realizarse muy lentamente a fin de que el estado se próxima al equilibrio térmico durante todo el proceso.
- 5. Poner agua en hielo Los contenedores isotérmicos permiten conservar diversos productos del mismo tipo a una temperatura constante
- 6. Su formula y despejes son: Formula general Despejes = Presión inicial = Volumen inicial = Presión final = Volumen final
- 7. Ejercicios. Un gas recibe una presión de 2 atmosferas y ocupa un volumen de 125 cm³. Calcular la presión que debe soportar para que su volumen sea de 95 cm³. Datos: Formula: Calculos: Un gas ocupa un volumen de 580 cm³ a una presión de 890 mmHg ¿Cuál será su volumen si la presión recibida aumenta a 920 mmHg? Datos: Formula: Calculos: = 2 atm = 125 cm³ = 95 cm³ = ? = 2atm (125 cm3) 95 cm³ =2.6315 atm = 580 cm³ = 890 mmHg = 920 mmHg = ? = 890 mmHg (580 cm³) 920 mmHg = 561.086 cm³
- 8. Proceso isobárico Es cuando hay una variación del volumen o temperatura y la presión permanece constante, no importando si el gas sufre una comprensión o una expansión. “ A una presión constante y para una masa dada de un gas, el volumen del gas varia de manera directamente proporcional a su temperatura absoluta “ Jacques Charles.
- 9. En la vida cotidiana… Cuando hierve el agua La presión permanece constante, de forma tal que entre mayor sea la temperatura el volumen desprendido aumenta. La variación de volumen que experimenta una pelota conforme los rayos del sol indicen sobre ella. Al inicio de la mañana presenta cierta presión, volumen y temperatura, conforme se calienta el aire en su interior aumenta la presión, pero esta no varia debido al aumento de su volumen. El aumento de 1 atmosfera por cada 10 metros que se sumerge un buzo La fabricación de los diamantes artificiales. Se realizan al transformar las piedras en un horno a presión constante. La fisión nuclear del sol y las estrellas
- 10. Formula y despejes: Formula general Despejes: = Temperatura inicial = Volumen inicial = Temperatura final = Volumen final * Debido a que la ley de Charles menciona que la temperatura debe de ser absoluta, se debe cuidar que este en grados kelvin.
- 11. Ejercicios Calcula la temperatura absoluta ala cual se encuentra un gas que ocupa un volumen de 0.4 litros a una presión de 1 atm, si a una temperatura de 45°C ocupa un volumen de 1.2 litros ala misma presión. Datos: Formula: Calculos: Se tiene un gas a una temperatura de 25°C y con un volumen de 70 cm³ a una presión de 586 mm de Hg. ¿Qué volumen ocupara este gas a una temperatura de 0°C si la presión permanece constante? Datos: Formula: Calculos: = 45°C + 273 = 318°K = 0.4 litros = 1.2 litros = ? = 1.2 lt. (318°K) 0.4 lt. = 954°K = 25°C + 273 = 298°K = 0°C + 273 = 273°K = 70 cm³ = ? = 273°K (70 cm³) 298°K = 64.13 cm³
- 12. Proceso isocórico También llamado isométrico o isovolumétrico, es aquel que se realiza a volumen constante “A un volumen constante y para un masa determinada de un gas, la presión absoluta que recibe el gas es directamente proporcional a su temperatura absoluta” Joseph Louis Gay-Lussac (1778-1850)
- 13. En la vida cotidiana: Cuando cocinamos en una olla de presión Disminuye el tiempo de cocción, pues sirve como deposito para que la temperatura y la presión aumenten en el interior conforme transcurre el tiempo manteniendo su volumen constante. Un cilindro cerrado, cuyo pistón este fijo, si aumentamos la temperatura, lo que aumentara será la presión, sin embargo el volumen permanecerá constante.
- 14. Los aerosoles Disolver azúcar en el café La temperatura gas atrapado en el interior de la llanta aumenta, y el volumen permanece constante.
- 15. Formula y despejes Formula general Despejes = Presión inicial = Temperatura inicial = Presión final = Temperatura final
- 16. Ejercicios Una masa dada de gas recibe una presión absoluta de 2.3 atm, su temperatura es de 33°C y ocupa un volumen de 850 cm³. Si el volumen del gas permanece constante y su temperatura aumenta a 75°C ¿Cuál será la presión absoluta del gas? Datos Formula Cálculos Un gas encerrado en un recipiente mantiene una temperatura de 22°C y tiene una presión absoluta de 3.8 atm ¿Cuál es la temperatura del gas si su presión absoluta es de 1.4 atm? Datos Formula Cálculos = 33°C + 273 = 306°K = 75°C + 273 = 348°K = 2.3 atm = ? = 348°K (2.3 atm) 306°K = 2.6 atm = 22°C + 273 = 295°K = ? = 3.8 atm = 1.4 atm = 295°K (1.4 atm) 3.8 atm = 108.68 °K
- 17. Proceso Adiabático En termodinámica se designa como proceso adiabático a aquél en el cual el sistema (generalmente, un fluido que realiza un trabajo) no intercambia calor con su entorno. El término adiabático hace referencia a elementos que impiden la transferencia de calor con el entorno.
- 18. Vida cotidiana Al abrir una botella de champán El champán tiene disuelto dióxido de carbono producido de forma natural. Cuando abrimos la botella disminuye la presión y el gas se expande adiabáticamente, de nuevo disminuyendo su temperatura y causando que el aire que se encuentra ahí disminuya su temperatura, alcanzando su punto de rocío y produciendo microscópicas gotas que dan ese aspecto de "humo" al vapor que emerge de la botella. Los procesos adiabáticos son comunes en la atmósfera: cada vez que el aire se eleva, llega a capas de menor presión, como resultado se expande y se enfría adiabáticamente. El estampido sónico producido cuando un avión sobrepasa la barrera del sonido, es decir, cuando se mueve más deprisa de la velocidad del sonido en ese medio.
- 19. Un termo para el café Experimento
- 20. Formula y despejes ∆U = Q – W (en un proceso adiabático Q = 0) ∆U = -W Q = ∆U + W W = P ( - ) W = Q - ∆U 1 cal = 4.2 J ó 4.186 1J = 0.24 cal ∆U = Cambio de energía interna en Joules (J) o calorías (cal) Q = Calor suministrado al sistema en (J, cal) W = Trabajo realizado en (J, cal) P = Presión en (N/m²) = Volumen inicial en m³ = Volumen final en m³
- 21. Ejercicios Determine la variación en la energía interna de un sistema al recibir 500 calorías y realizar un trabajo de 800 Joules. Datos Formula Calculos Un sistema varia su energía interna en 300 J al efectuarse un trabajo de -700 J. Determinar la cantidad de calor que se transfiere en el proceso. Datos Formula Calculos Q = 500 cal W = - 800 J ∆U = ? Q = 500 cal * 4.2J/cal = 2,100 J ∆U = (2,100 J - (- 800 J)) ∆U = 2,900 J ∆U = Q – W W = -700 J ∆U = 300 J Q = ? Q = ∆U + W Q = 300 J + (-700 J) Q = -400 J
- 22. Proceso Diatérmico Un proceso diatérmico quiere decir que deja pasar el calor fácilmente. Una interacción térmica es cualquier otro tipo de intercambio de energía, en este caso la pared se denomina diatérmica. Una pared diatérmica es aquella que permite la transferencia de energía térmica (calor) pero, sin que haya transferencia de masa. El opuesto es una pared adiabática que es la que impide la transferencia de energía en forma de calor. Un proceso diatérmico quiere decir que deja pasar el calor fácilmente.
- 23. En la vida cotidiana: Al calentar agua o comida en una olla El fuego que se encuentra por debajo calienta el metal de la olla, en este caso el metal es el que permite el paso de calor y se lo transmite al agua que esta dentro de la olla. Quemaduras por contacto con algo caliente El calentamiento de los alimentos al cocinarlos o el enfriamiento de ellos, por ejemplo el del té o café Cuando en un termómetro sube la temperatura
- 24. Formulas y despejes ∆U = Q – W Q = ∆U + W W = P ( - ) W = Q - ∆U 1 cal = 4.2 J ó 4.186 1J = 0.24 cal +Q = Cede -Q = Recibe ∆U = Cambio de energía interna en Joules (J) o calorías (cal) Q = Calor suministrado al sistema en (J, cal) W = Trabajo realizado en (J, cal) P = Presión en (N/m²) = Volumen inicial en m³ = Volumen final en m³ N/m² (m³) = Nm = J
- 25. Ejercicios Determina la variación de energía interna de un sistema cuando sobre el se realiza un trabajo de 50 J, liberando 20 cal al ambiente. En joules. Datos Formula Calculos En una maquina de vapor la caldera cuenta con 2 litros de agua (1 m³ = 1000 lt) se convierte en 3234 litros de vapor cuando hierve a una presión constante de 0.1 atm, Calcular el trabajo realizado por el sistema: Datos Formula Calculos Q = 20 cal = (-20cal)(4.186) = -83.72 J W = 50 J = - 50 J ∆U = ? ∆U = Q – W ∆U = (-83.72 J) – (-50 J) ∆U = -33.72 = 2 lit, (2/1000) = 0.002 m³ = 3234 lit (3234/1000) = 3.234 m³ P = 0.1 atm = 1013 N/m² W = P ( - ) W = 1013 N/m² ( 3.234 m³ – 0.002 m³ ) W = 32740.16 J
