Modelos atómicos
•
0 recomendaciones•134 vistas
Teoría modelos atómicos
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
Más contenido relacionado
Similar a Modelos atómicos
Similar a Modelos atómicos (20)
Cuadro-comparativo-de-los-Modelos-Atomicos-6 (1).pptx

Cuadro-comparativo-de-los-Modelos-Atomicos-6 (1).pptx
Más de marcocherly
Más de marcocherly (13)
Último
Centros Multigrados Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...Katherine Concepcion Gonzalez
Unidad de aprendizaje del mes de mayo para trabajar con estudiantes de primer grado de primariaUNIDAD DE APRENDIZAJE DE PRIMER GRADO DEL MES DE MAYO PARA TRABAJAR CON ESTUD...

UNIDAD DE APRENDIZAJE DE PRIMER GRADO DEL MES DE MAYO PARA TRABAJAR CON ESTUD...rosalindatellodelagu
Último (20)
Tema 19. Inmunología y el sistema inmunitario 2024

Tema 19. Inmunología y el sistema inmunitario 2024
Concepto y definición de tipos de Datos Abstractos en c++.pptx

Concepto y definición de tipos de Datos Abstractos en c++.pptx
Louis Jean François Lagrenée. Erotismo y sensualidad. El erotismo en la Hist...

Louis Jean François Lagrenée. Erotismo y sensualidad. El erotismo en la Hist...
Código Civil de la República Bolivariana de Venezuela

Código Civil de la República Bolivariana de Venezuela
PINTURA DEL RENACIMIENTO EN ESPAÑA (SIGLO XVI).ppt

PINTURA DEL RENACIMIENTO EN ESPAÑA (SIGLO XVI).ppt
Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...
UNIDAD DE APRENDIZAJE DE PRIMER GRADO DEL MES DE MAYO PARA TRABAJAR CON ESTUD...

UNIDAD DE APRENDIZAJE DE PRIMER GRADO DEL MES DE MAYO PARA TRABAJAR CON ESTUD...
Desarrollo y Aplicación de la Administración por Valores

Desarrollo y Aplicación de la Administración por Valores
La Sostenibilidad Corporativa. Administración Ambiental

La Sostenibilidad Corporativa. Administración Ambiental
PLAN LECTOR 2024 integrado nivel inicial-miercoles 10.pptx

PLAN LECTOR 2024 integrado nivel inicial-miercoles 10.pptx
ACERTIJO LA RUTA DEL MARATÓN OLÍMPICO DEL NÚMERO PI EN PARÍS. Por JAVIER SOL...

ACERTIJO LA RUTA DEL MARATÓN OLÍMPICO DEL NÚMERO PI EN PARÍS. Por JAVIER SOL...
Los avatares para el juego dramático en entornos virtuales

Los avatares para el juego dramático en entornos virtuales
Modelos atómicos
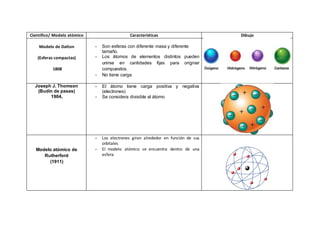
- 1. Científico/ Modelo atómico Características Dibujo Modelo de Dalton (Esferas compactas) 1808 - Son esferas con diferente masa y diferente tamaño. - Los átomos de elementos distintos pueden unirse en cantidades fijas para originar compuestos. - No tiene carga Joseph J. Thomson (Budín de pasas) 1904, - El átomo tiene carga positiva y negativa (electrones) - Se considera divisible al átomo Modelo atómico de Rutherford (1911) - Los electrones giran alrededor en función de sus orbitales - El modelo atómico se encuentra dentro de una esfera
- 2. El modelo de Bohr Modelo del sistema solar 1913 - Los electrones giran alrededor del núcleo - Los electrones que se encuentran distribuidos en cantidades especificas por cada nivel de energía - El núcleo se encuentra conformado por protones y neutrones. - Las orbitas presentan una forma circular - Un átomo gana o pierde energía dependiendo del movimiento de los electrones en las orbitas. Modelo de Sommerfeld 1915 - Los electrones se desplazan en orbitas circulares o elípticas - No se puede conocer con exactitud la posición de un electrón debido a la gran velocidad con la cual se desplaza - El tamaño del átomo dependerá del número de orbitales. - Postulo el numero cuántico principal (n)
- 3. Modelo atómico mecánico cúantico 1926 En 1924, Louis de Broglie, postuló que los electrones tenían un comportamiento de onda. En 1927, Erwin Schrödinger, establece una ecuación matemática Esta describe probabilisticamente el comportamiento de un electrón enel átomo En 1927 Heisenberg, sugiere que es imposible conocer con exactitud la posición, el momento y la energía de un electrón.