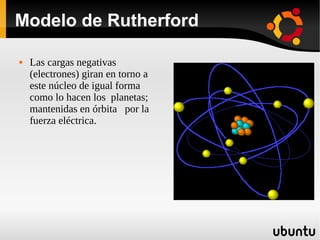
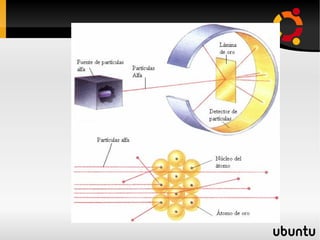
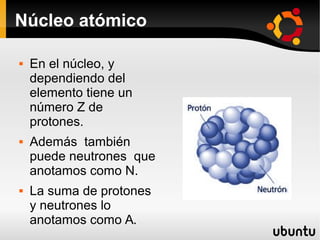
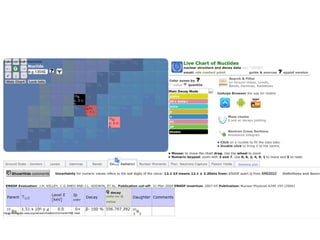
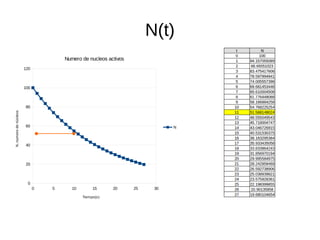
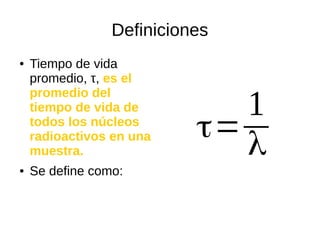
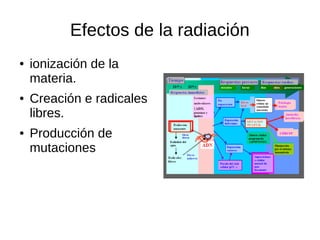
Este documento presenta información sobre física nuclear. Explica los modelos atómicos de Thomson, Rutherford y Bohr, así como conceptos como los niveles de energía, emisión y absorción de radiación. También describe la estructura del núcleo atómico, los diferentes tipos de radiación, la estabilidad nuclear, los modos de decaimiento radiactivo y las leyes que rigen la desintegración. Finalmente, introduce conceptos como actividad radiactiva y vida media de isótopos radiactivos.