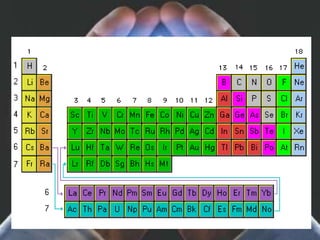
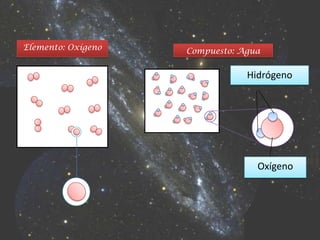
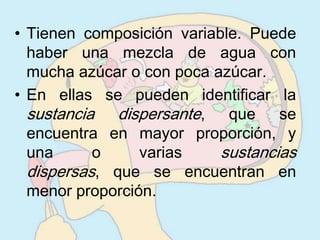
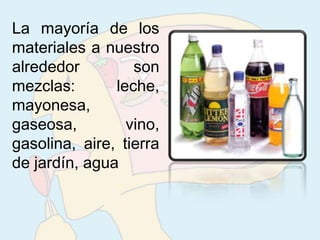
Existen dos tipos de materia: sustancias puras y mezclas. Las sustancias puras son elementos químicos o compuestos químicos que tienen propiedades específicas, mientras que las mezclas son combinaciones de dos o más sustancias que permanecen juntas pero no se combinan. Las mezclas se pueden clasificar como homogéneas o heterogéneas dependiendo de si sus componentes son distinguibles o no.