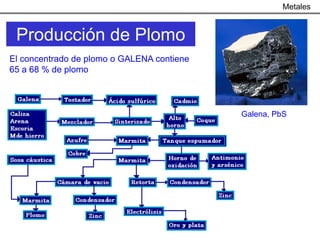
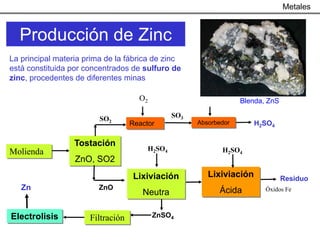
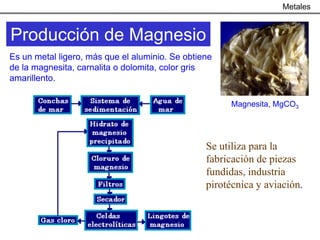
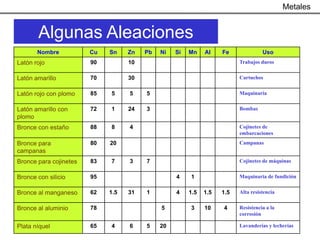
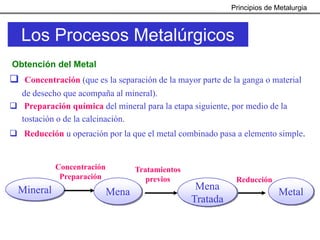
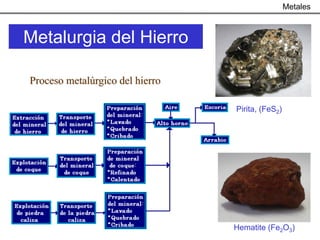
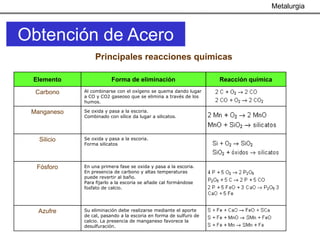
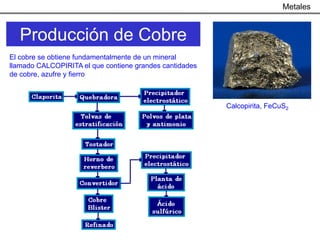
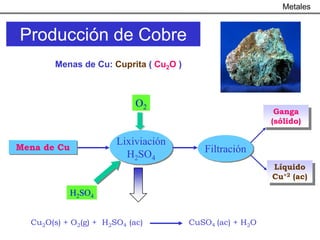
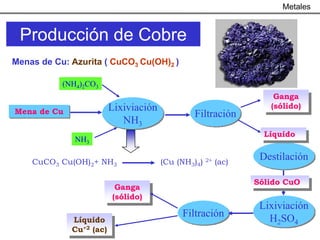
Este documento trata sobre los procesos metalúrgicos para la obtención de diferentes metales como el hierro, cobre, aluminio y zinc. Explica que el hierro se obtiene mediante la reducción química de minerales como la pirita y la hematita en un alto horno, y que el acero se produce eliminando impurezas del hierro y añadiendo carbono. También describe los procesos de lixiviación y electrolisis para la producción de cobre a partir de minerales como la calcopirita, y el proceso Bayer y la























![Metales
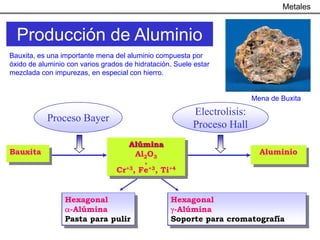
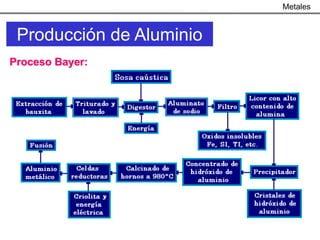
Producción de Aluminio
Electrolisis: Proceso Hall
Impuro Al2O3 (s) + 2OH- (aq) 2AlO2- (aq) + H2O (l)
AlO2- (s) + H3O+ (aq) Al(OH)3 (s)
D
2Al(OH)3 (s) Al2O3 (s) + 3H2O (g)
Ánodo de carbono
Cátodo
de
carbono Ánodo: 3[2O2- O2 (g) + 4e-]
Cátodo: 4[Al3+ + 3e- Al (l)]
Aluminio
fundido 2Al2O3 4Al (l) + 3O2 (g)
Al2O3 en criolita fundida, Na3AlF6](https://image.slidesharecdn.com/metalurgiaenpowerpoint-120511141945-phpapp02/85/Metalurgia-en-power-point-34-320.jpg)