Proteinas i i
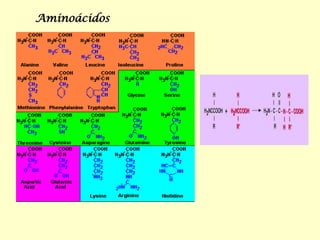
- 1. Aminoácidos
- 2. Estructura de las proteínas
- 3. Amino ácido Estructura primaria Estructura secundaria Estructura terciaria azar α hélice β láminar α hélice Estructura primaria, secundaria y terciaria
- 5. Clasificación de las proteínas Holoproteínas: Globulares: Prolaminas (glianina), Gluteninas (orizanina), albuminas, Hormonas, enzimas, actina, miosina Fibrosas: Colágenos, queratinas, Fibroinas, elastinas. Heteroproteínas: Glucoproteínas, (anticuerpos), lipoproteinas, Nucleoproteínas (ribosomas), Cromoproteínas, hemoglobina, mioglobina.
- 6. Sistemas alimentarios Componentes Huevo entero (%) Yema (%) Clara (%) Agua 74.0 49 87.8 Proteínas 12.9 16 10.9 Carbohidratos 0.4 0.6 0.2 Lipidos 11.5 30.6 0.2 Cenizas 0.7 2.0 0.3 Composición del huevo
- 7. Componente % Agua 70 Proteínas 20 Grasa 6 Sustancias no proteícas 1.5 Carbohidratos 1.5 Sales inorgánicas 0.7 Composición de la carne
- 8. Composición de la leche (%) Raza Agua Grasa Proteínas Lactosa Cenizas Suiza 87.31 3.97 3.37 4.63 0.72 Jersey 85.66 5.15 3.70 4.75 0.74 Proteinas grasa carbohidratos cenizas 40 21 34 4.9 Composición de la soya (%)
- 9. Agua proteínas Grasa carbohidratos ceniza fibra vitaminas 87 0.8 0.2 10.5 0.4 0.8 0.3 Composición quimica de una fruta (naranja %)
- 10. Importancia tecnológica de las proteínas
- 11. Proteínas de la clara de huevo Proteína Punto isoelectrico Caracteristicas Ovalbumina 4.7 Espumante y gelificante Ovotranferrina 6.0 Antimicrobiana, enlaces con hierro Ovomucoide 4.1 Inhibidor de tripsina Ovomucina 4.5-5.0 Lysozyma 10.7 antimicrobiana G2 globulina 5.5 ? G3 globulina 5.8 ? Ovoglicoproteina 3.9 ? Ovoinhibidor 5.1 Inhibidor Ovoflavoproteina 4.0 Enlaces con riboflavina Ovomacroglobulina 4.5-4.7 antigenico Cystatina 5.1 Inhibidor de proteinasa
- 12. Proteina Caracteristicas Lipovitelinas Emulsificante * Fosvitina Lipoproteina de baja densidad (LDL) Emulsificante Livetinas Emulsificante Riboflavina Biotina Proteínas de la Yema
- 13. Proteinas de la carne Proteina Caracteristicas Actina Gelificante, emulsificante Miosina Gelificante, emulsificante Colágeno gelifica Elastina - Proteinas sarcoplasmaticas - Proteínas del trigo Gluteninas y Prolaminas (gliadinas) Cohesividad y viscoelasticidad
- 14. Proteínas de la leche Caseinas α, ß,γ, Proteínas del suero α lactalbumima, ß lactoglobulina, Seroalbuminas, inmunoglobulinas, lactoferrinas Proteínas de soya Globulinas y albuminas Geles Emulsiones, emulsificantes
- 15. Interacciones de las proteínas Interacción Covalente Ionica Puentes de hidrógeno Hidrofóbas Proteína-proteína + + ++ +++ Proteína-lípido + + + +++ Proteína-polisacárido - +++ ++ - Proteína-disolvente - + +++ - Proteína-iones - +++ + -
- 16. Región hidrofóbica Región hidrofílica Reagrupamiento Región hidrofóbica Región hidrofílica
- 17. Interacciones proteína -agua Factores extrínsecos: Factores Intrinsecos Peso molecular, estructura primaria y secundaria Forma, composición de aminoácidos pH, fuerza ionica, temperatura Las interacciones agua-proteína se efectúan por medio de aminoácidos polares (catiónica, aniónica o no iónica). La capacidad de retención de agua es mayor cuando se encuentra en forma ionizada.
- 18. Interacción proteína-proteína Temperatura y concentración salina Ejemplos de interacciones proteína-proteína. La estructura cuaternaria, las micelas de la leche, la contracción muscular, los complejos anticuerpo- antigeno, enzima-sustrato. Interacción de las proteínas con los carbohidratos Gomas: carrageninas función de pH Carbohidratos neutros (almidon y celulosa) no existen moleculas ionizables y los enlaces son principalmente por puentes de hidrógeno. Reacción de Maillard: uniones covalentes al aplicar calor
- 19. Interacción de las proteínas con los lípidos Mediante enlaces hidrofóbicos entre cadenas alifáticas apolares de los lípidos y regiones apolares de las proteínas, aun cuando existen iones divalentes como el calcio. LIPOPROTEINAS DONDE SE ENCUENTRAN? Las lipoproteínas del glóbulo de grasa de la leche se pueden producir mecani- camente. ¿Cómo? POR HOMOGENIZACION. Las caseínas y las proteínas de la soya se usan en la elaboración de productos cárnicos por su capacidad de asociarse y emulsionar grasas. La formación de espuma cuando la interacción proteína-lipido es fuerte. La asociación de una proteína con los lípidos protege a la proteína contra la desnaturalización por la acción de calor.
- 20. Qué es la desnaturalización de las proteínas? Es un cambio que sufre la proteína en su estructura tridimensional Reversible: Cuando es posible restablecer su estructura nativa Irreversible: La estructura original no puede ser reestablecida.
- 21. Cómo se puede desnaturalizar una proteína? Agentes Fisicos Calor El frío Tratamientos mecánicos La irradiación Las interfaces Agentes Químicos Acido-base Metales Solventes orgánicos Compuestos orgánicos
- 22. Desplegamiento de una proteína en la interface
- 23. Interacciones Grupos implicados Agentes desnaruralizantes Electrostática R-COO - + NH3-R Carboxilo Amino Imidazole Guanidina Soluciones de sal pH extremos Hidrógeno R-C=O ---- HO-R Hidroxil Amida Fenol Carbonilo Calor Soluciones de urea Hidrofóbico Cadenas alifaticas Aminoácidos aromáticos Frio Detergentes Disulfuro R- S – S - R Cisteina Agentes reductores ß-mercapto etanol O O Agentes desnaturalizantes según el tipo de enlace
- 24. Efectos de la desnaturalización 1.- Descenso de la solubilidad a consecuencia del desenmascaramiento de grupos hidrofobicos. 2.- Modificación de la capacidad de fijación de agua 3.- Perdida de actividad biológica (enzimática o inmunológica) 4.- Incremento al ataque de proteasas a causa del enmascaramiento de enlaces peptidicos. 5.- Incremento de la viscosidad intrinseca. 6.- Incapacidad de cristalizar.
- 25. Alteración de las proteínas (tratamiento a altas temperaturas) A Desnaturalización de la proteína Exposición de a.a. escondidos Aumento de la disponibilidad de a.a. Destrucción de inhibidores de tripsina y quimotripsina Inactivación de enzimas Inactivación de otros compuestos indeseables. C Desulfuración Oxidación Ciclización Racemización Deshidratación Maillard Enlaces entrecruzados
- 26. UNIVERSIDAD AUTONOMA DE SAN LUIS POTOSI FCQ Es una Propiedad Fisicoquímica que permite que los alimentos exhiban características deseables.
- 27. Propiedades funcionales de las proteínas ¿Qué es una propiedad funcional? Es una propiedad fisicoquímica que permite contribuir a que los alimentos exhiban caracteristicas deseables. “Funcionalidad” cualquier propiedad distinta a la nutritiva que condicione su utilidad en los alimentos. Las propiedades funcionales afectan las características sensoriales y fisicoquímicas de los alimentos Propiedades funcionales Propiedades de hidratación (interacción proteína-agua). Propiedades relacionadas con las interacciones proteína proteína. Propiedades de superficie.
- 28. UNIVERSIDAD AUTONOMA DE SAN LUIS POTOSI FCQ Propiedades de hidratación interacción proteína-proteína Propiedades de superficie Capacidad de retención de agua, humectabilidad Formación de masas geles Características espumantes
- 29. Interacciones implicadas Propiedades funcionales Proteína-agua Proteína-Proteína Proteina-interface Hidratación Precipitación Gelificación Textura Emulsificación Espuma Solubilidad Absorción de agua Retención de agua Hinchamiento Adhesión Dispersibilidad Viscosidad
- 30. Alimento Funcionalidad Bebidas Solubilidad a diferentes pHs, estabilidad al calor, viscosidad. Sopas y salsas Viscosidad, emulsificación, retención de agua. Formación de masa (productos de panadería pan, cakes, etc.) Formación de una matriz con propiedades viscoelasticas, cohesión, desnaturalización por calor, formación de gel, absorción de agua, emulsificación, formación de espuma, pardeamiento. Productos lacteos (queso fundido, helados, etc. Emulsificación, retención de agua, viscosidad, formación de espuma, formación de gel, coagulación Productos cárnicos, (salchichas, etc.) Emulsificación, retención de agua y grasa, formación de gel, cohesión Extensores o sustitutos de carne (proteínas vegetales texturizadas) Absorción retención de agua y grasa, insolubilidad, dureza, carácter masticable cohesión y desnaturalización por calor. Recubrimientos Cohesión, adhesión Productos de repostería (chocolate) Dispersibilidad y emulsificación.
- 31. PROTEINA SECA Enlace de las moléculas de agua con las proteínas Monocapa Etapa 1 Enlace de las moléculas de agua con las proteínas Multicapa Etapa 2 Condensación de agua líquida Hinchamiento Etapa 3 Etapa 4 DispersiónSolución Vía A Vía BParticulas hidratadas insolubles
- 32. Factores que influyen sobre las propiedades de hidratación • La concentración proteíca • pH • Tipo y concentración de iones *A bajas concentraciones la hidratación de las proteínas se incrementa. *A altas concentraciones la hidratación de las proteínas disminuye (deshidratación)
- 33. Precipitación de las proteínas
- 34. Porqué es importante que la proteína sea soluble? • Permite una alta y rápida dispersión de las partículas, para formar coloides, finamente dispersos con estructuras macroscopicas y textura fina. • Facilita la difusión de las proteínas a la interfase agua/aire o agua/aceite. • Son mejores emulgentes, formadores de espuma, gelificantes.
- 35. Qué es la reología? • Estudia la deformación y el flujo de la materia. Sólidos Hookeanos Líquidos Newtonianos VISCOELASTICO
- 36. Viscosidad: Tasa de flujo por unidad de fuerza. La viscosidad de un fluido refleja su resistencia a fluir. coeficiente de viscosidad = = / = gradiente de velocidad = esfuerzo cortante Las disoluciones, dispersiones (suspensiones) emulsiones, pastas o geles de moléculas hidrófilas, y entre ellas las proteínas no se comportan como fluidos newtonianos. El coeficiente de viscosidad desciende a medida que la velocidad de flujo aumenta. = m n m= es el coeficiente de consistencia n= índice del comportamiento del flujo
- 37. Fluido móvil Fluido viscoso Fluido intermediario γ X γ Fluido móvil Fluido intermediario Fluido viscoso Comportamiento de un fluido Newtoniano en relación entre la fuerza de cizallamiento o el coeficiente de viscosidad y la Velocidad de fluído
- 38. Diámetro A) Características intrínsecas de la molécula peso molecular, tamaño, volumen, estructura y asimetría cargas eléctricas, facilidad de deformación B) Interacciones proteína-disolvente Hinchamiento, solubilidad de la molécula C) Interacciones proteína-proteína Determinan el tamaño de los agregados proteicos FACTORES QUE INFLUYEN LA VISCOSIDAD DE LOS FLUIDOS PROTEICOS
- 39. Plasticos: salsa catsup, mayonesa Pseudoplasticos: vinagretas, aderezos Dilatante: suspensiones de almidón y algunos jarabes de chocolate. [] proteica µ