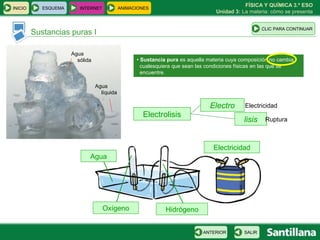
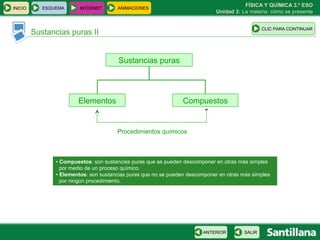
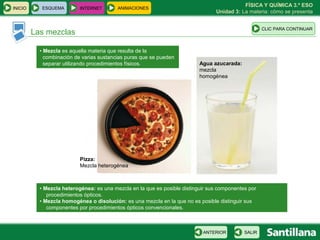
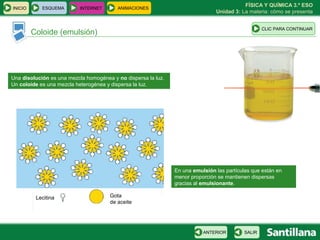
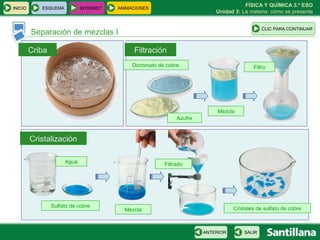
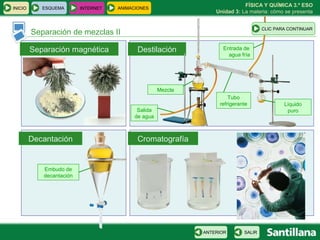
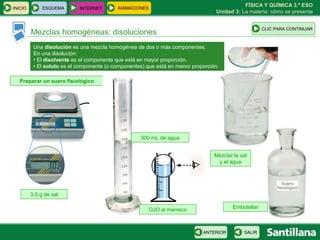
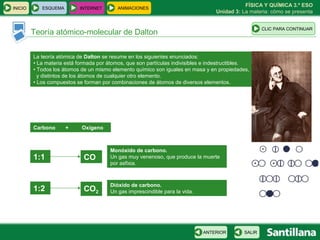
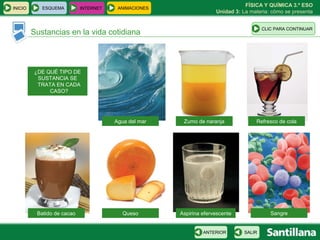
Este documento presenta la unidad 3 sobre la materia y cómo se presenta. Explica conceptos clave como sustancias puras, mezclas homogéneas y heterogéneas, y diferentes métodos para separar mezclas como filtración, destilación y cromatografía. También introduce la teoría atómica de Dalton sobre la composición de la materia a nivel atómico.