Toxicidad aguda oral días
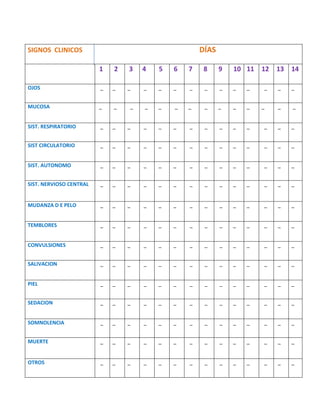
- 1. DÍAS SIGNOS CLINICOS 1 2 3 4 5 6 7 8 9 10 11 12 13 14 OJOS _ _ _ _ _ _ _ _ _ _ _ _ _ _ MUCOSA _ _ _ _ _ _ _ _ _ _ _ _ SIST. RESPIRATORIO _ _ _ _ _ _ _ _ _ _ _ _ _ _ SIST CIRCULATORIO _ _ _ _ _ _ _ _ _ _ _ _ _ _ SIST. AUTONOMO _ _ _ _ _ _ _ _ _ _ _ _ _ _ SIST. NERVIOSO CENTRAL _ _ _ _ _ _ _ _ _ _ _ _ _ _ MUDANZA D E PELO _ _ _ _ _ _ _ _ _ _ _ _ _ _ TEMBLORES _ _ _ _ _ _ _ _ _ _ _ _ _ _ CONVULSIONES _ _ _ _ _ _ _ _ _ _ _ _ _ _ SALIVACION _ _ _ _ _ _ _ _ _ _ _ _ _ _ PIEL _ _ _ _ _ _ _ _ _ _ _ _ _ _ SEDACION _ _ _ _ _ _ _ _ _ _ _ _ _ _ SOMNOLENCIA _ _ _ _ _ _ _ _ _ _ _ _ _ _ MUERTE _ _ _ _ _ _ _ _ _ _ _ _ _ _ OTROS _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _
- 2. ENSAYOS DE TOXICIDAD AGUDA ORAL PRODUCTO: EXTRACTO DE MORINGA DOSIS: 300 mg/kg de Peso FECHA DE INICIO:10/01/14FECHA DE TERMINACION:24/01/14 Grupo Peso inicial Volumen(ml) Pesadas en gramos (días) 7 14 1 210 300 221 223 2 218 300 224 225 3 192 300 205 210 216.66 219.33 Media y desviación Estándar 206.66
- 3. CALCULOS Datos: 1era. Rata: 210 gr ST=9% 2da. Rata: 218 gr 3era. Rata: 196 gr Volumen de toxico: 300 mg/kg PRIMERA RATA 300 mg 1000 gr X 210gr X= 63mg 63mg x 90mg 1ml X=0,7ml SEGUNDA RATA 300 mg 1000 gr X 218gr X= 65.4mg 65.4mg x 90mg 1ml X=0,72ml TERCERA RATA 300 mg 1000 gr X 196 gr X= 58.8mg 58.8mg 90mg X=0,64ml x 1ml
- 4. UNIVERSIDAD TECNICA DE MACHALA FACULTAD DE CIENCIAS QUIMICA Y LA SALUD ESCUELA DE BIOQUIMICA Y FARMACIA TOXICOLOGIA PROFESOR: Bioq. Farm. Ricardo León ESTUDIANTE: Verónica Farez Orellana FECHA: 24 de enero del 2013 CURSO: 5to. Bioquímica y farmacia TÍTULO DE LA PRÁCTICA: PARALELO: “B” GRUPO: 1 10 TOXICIDAD AGUDA ORAL OBJETIVOS DE LA PRÁCTICA: Determinar se la dosis empleada de extracto de moringa en las ratas resulta toxicas al ser evaluadas por 14 días. Conocer los signos que presentan las ratas con las dosis empleado (300mg/Kg). MATERIALES: Campana Mascarilla Mandil Jeringuilla #10 Tabla de disección Instrumentos de disección Bisturí #11 Guantes de látex SUSTANCIAS: Extracto de moringa PROCEDIMIENTO: 1.-Los animales deben estar en ayunas antes de la administración (3 ratones) 2.-Se administra una sola dosis a cada rata.
- 5. 3.-La administración es por gavage utilizando una cánula de administración intragástrica. 4.-Terminado la dosificación la comida se volverá a colocar de 3 a 4 horas después. 5.-Durante 14 días se registrara el peso y los signos que presentan cada rata. 6.-Despues de 14vo día se procederá a la disección de las ratas para verificar el estado de sus órganos. GRÁFICOS: OBSERVACION: Se pudo observar el estado de los órganos de las ratas a las cuales se les administraron extracto de moringa. CONCLUSIÓN: Se pudo comprobar que la dosis única (300mg/kg) aplicada en las ratas no implica un grado de toxicidad aguda letal pues el buen estado de los órganos y los signos clínico que se registraron días anteriores demuestran su nivel bajo de toxicidad de la moringa en esta dosis. CONSULTA: TOXICIDAD AGUDA ORAL La toxicidad aguda tiene por objeto determinar los efectos de una dosis única y muy elevada de una sustancia. Usualmente, el punto final del estudio es la muerte del animal y la
- 6. toxicidad aguda se expresa por la dosis letal 50, que viene a representar más o menos la dosis de la sustancia que produce la muerte en el 50% de los animales. La observación de los animales se lleva a cabo después de la administración de la sustancia y dura hasta 14 días, después de los cuales los animales son sacrificados y autopsiados. En general, el test se realiza con 5 grupos de 10 animales de cada sexo, aunque existen algunos métodos abreviados que intentan reducir el número de animales a sacrificar. La determinación de la DL50 se suele llevar a cabo en rata y ratón por al menos dos vías de administración entre las cinco posibles. En el perro y otros animales de tamaño parecido, el punto final del estudio no suele ser la muerte del animal, sino la determinación de la dosis que produce unos severos efectos adversos El potencial tóxico de un extracto acuoso liofilizado fue evaluado mediante el ensayo de toxicidad aguda oral y sub- crónica a 90 días en ratas Wistar de ambos sexos. Los métodos empleados fueron los descritos por las normas OECD. En el ensayo agudo se administró por vía oral la dosis de 2000 mg/kg y en el ensayo subcrónico 250, 500 y 1000 mg/kg/día durante 13 semanas. Se evaluaron los signos tóxicos y peso corporal en ambos ensayos. En el estudio subcrónico además se evaluó el consumo de alimentos, indicadores hematológicos (hemoglobina, hematocrito, recuento diferencial de leucocitos, recuento total de leucocitos y recuento total de eritrocitos) y bioquímica clínica (glucosa, alanino amino transferasa, aspartato amino transferasa, colesterol, urea, bilirrubina y creatinina). También se realizó necropsia y examen histopatológico de órganos y tejidos (corazón, riñón, hígado, bazo, cerebro, pulmón, estómago intestino, timo, glándulas suprarrenales, tiroides, paratiroides, páncreas, glándulas salivales, ganglio cervical, testículos, vesí culas seminales, próstata y ovarios) y se determinó el peso relativo de órganos (corazón, riñón, hígado, bazo, cerebro, pulmón, timo, glándulas suprarrenales, próstata, testículos y ovarios). No se apreciaron signos tóxicos ni mortalidad como consecuencia de la administración del liofilizado de Ocimumtenuiflorum L. en ninguno de los ensayos. Los parámetros analizados de peso corporal, consumo de alimentos, hematología, bioquímica, peso relativo de órganos y análisis histopatológico de órganos y tejidos no evidenciaron toxicidad significativa atribuible a la sus tancia de prueba. BIBLIOGRAFÍA:http://www.iqb.es/cbasicas/farma/farma05/tox/tox02.htm
