Configuración electrónica
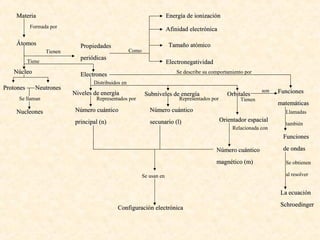
- 1. Materia Energía de ionización Formada por Afinidad electrónica Átomos Propiedades Tamaño atómico Tienen Como periódicas Tiene Electronegatividad Núcleo Electrones Se describe su comportamiento por Distribuidos en Protones Neutrones son Niveles de energía Subniveles de energía Orbitales Funciones Se llaman Representados por Representados por Tienen matemáticas Nucleones Número cuántico Número cuántico Llamadas principal (n) secunario (l) Orientador espacial también Relacionada con Funciones Número cuántico de ondas magnético (m) Se obtienen Se usan en al resolver La ecuación Schroedinger Configuración electrónica
- 2. A u m e n ta Aumenta Aumenta A u m e n ta Es la mitad de la distancia ínter nuclear Es la energía necesaria para arrancar por completo un electrón a un átomo aislado en entre dos átomos enlazados. fase gaseosa. 1s1 1s0 H 1e- H1+ Aumenta Aumenta A u m e n ta A u m e n ta Es la energía liberada en formación de un anión a partir de un átomo neutro aislado en estado gaseoso. Es la capacidad que tiene un átomo de 1e- atraer electrones hacia él en un enlace 1s2 2s2 2p2 1s2 2s2 2p6 F F1- químico.
- 3. Max Plank (1900) La energía, como la materia, es discontinua. La energía de la radiación del cuerpo negro está cuantizada (varía como múltiplo entero de una unidad fundamental llamada cuanto o quiantum) Maxwell (1864) predijo la existencia de unas ondas que viajarían a la velocidad de la luz, las ondas electromagnéticas. Una onda es una perturbación que transmite energía a través de un medio. Radiación electromagnética es la transmisión de energía a través del espacio, en laque los campos eléctricos y magnéticos actúan como una onda. A un conjunto ordenado de radiaciones electromagnéticas con base en su energía se le llama espectro electro – magnético.
- 6. • Para poder hablar de los orígenes de esta nueva área de investigación nos remontamos a 1959, con el Premio Nobel de Física Richard Feynman. Éste da una conferencia titulada "Hay mucho sitio por debajo" en la que destacó los beneficios que puede aportar a la sociedad la capacidad de atrapar y situar átomos y moléculas en posiciones determinadas y fabricar artefactos con una precisión de pocos átomos. Pero el suceso impactante y determinante en la motivación del impulso del mundo de la nanotecnología fue la "manipulación atómica" realizada por parte del equipo de IBM bajo la directriz de Don Eigler. • En el año 1981 crean un instrumento llamado "Microscopio de barrido de efecto túnel" el cual permitía captar una imagen de la estructura atómica de la materia. • En el área de la nanotecnología se diferencian dos tipos: Top-down, reducción del tamaño, se logra la miniaturización de estructuras a escala nanométrica siendo el tipo de nanotecnología más frecuente en la actualidad. Y la denominada Bottom-up Auto ensamblado. Se parte de una estructura nanométrica y se comienza un proceso de montaje que crea un mecanismo mayor. Este auto ensamblado se la nombra comúnmente Nanotecnología molecular y ha sido desarrollada por el investigador Eric Drexel, el cual dijo • "Puestos en orden de una manera, los átomos componen aire, tierra, agua. Con otro diseño, los átomos forman unas fabulosas fresas frescas"
- 7. Einstein (1905) propuso que la radiación electromagnética esta formada de partículas (corpuscular) a las que llamó fotones. Bohr (1913) propuso su modelo atómico en los que los electrones sólo pueden estar en los niveles en los que su energía está cuantizada. Número cuántico principal n = 1,2,3 El número máximo de electrones en un nivel de energía se calcula 2n2 Broglie (1924) sugirió que los electrones en movimiento tenían propiedades ondulatorias (se comportan como una onda) y corpusculares (se comportan como partículas). Dualidad onda – partícula de la materia. Heisenberg (1928) es imposible conocer en forma exacta y simultánea la posición y el momento del electrón. Incorrecto “electrones moviéndose en órbitas definidas” Schrödinger (1926) propuso un modelo matemático que contiene la información necesaria sobre el estado energético de los electrones en un átomo.
- 8. Números Cuánticos -Número cuántico principal (n )- nivel de energía que se encuentra el electrón n = 1,2,3,4... -Número cuántico secundario o azimutal (l )- subnivel que puede ocupar el electrón l = 0,...(n-1) El valor de l designa la forma del orbital (s,p,d,f) -Número cuántico magnético o de orientación espacial (m )- orientación de un orbital atómico m = - l ……0 …….. + l -Número cuántico de spin (s)- momento magnético intrínseco del electrón s = +1/2 Este número cuántico lo introdujo Dirac (1928).
- 9. Forma de los orbitales
- 10. Valor de l Tipo de subnivel Número máximo de electrones 0 s 2 1 p 6 2 d 10 3 f 14 4 g 18 n=3 l = 0 (subnivel s) l = 1 (subnivel p) l = 2 (subnivel d) m=0 m = -1 m=0 m = +1 m = -2 m = -1 m=0 m = +1 m = +2 3s 3p 3p 3p 3d 3d 3d 3d 3d 1 orbital 3 orbitales 5 orbitales
- 11. Combinaciones permitidas de números cuánticos n l m Notación Cantidad de Cantidad de e- Total de subcapa orbitales en la necesarios para de e- subcapa llenar la subcapa por nivel 1 0 0 1s 1 2 2 2 0 0 2s 1 2 8 2 1 1,0,-1 2p 3 6 3 0 0 3s 1 2 18 3 1 1,0,-1 3p 3 6 3 2 2,1,0,-1,-2 3d 5 10 4 0 0 4s 1 2 32 4 1 1,0,-1 4p 3 6 4 2 2,1,0,-1,-2 4d 5 10 4 3 3,2,1,0,-1,- 4f 7 14 2,-3
- 12. Principios de Aufbau o de edificación progresiva: en un átomo, cuando los electrones se introducen dentro de los orbitales atómicos, ellos ocuparan el orbital con menor energía.
- 13. Configuración electrónica: Es la forma en que se representa como se encuentran acomodados los electrones en un átomo. Simbólica 1s2 2s2 2p6 Gráfica: 1s 2s 2p 2p 2p
- 14. Principios de exclusión de Pauli: en un átomo no puede existir dos electrones con sus cuatro números cuánticos iguales. (en un orbital sólo pueden estar dos electrones con spin opuesto) Principio de máxima multiplicidad o regla de Hund: el acomodo de electrones en orbitales degenerados será de tal forma que su multiplicidad sea máxima. 1s2 2s2 2p3 1s 2s 2p 2p 2p
