Presentacion quimica
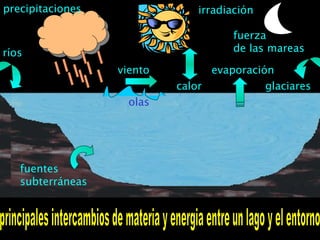
- 1. principales intercambios de materia y energia entre un lago y el entorno precipitaciones viento ríos fuerza de las mareas calor irradiación glaciares fuentes subterráneas olas evaporación
- 4. Compuestos disueltos en el agua: .gases .orgánicos .elementos mayores .elementos menores .elementos traza
- 5. Perfil de O2 en relación a la profundidad (oxiclina)
- 6. - O 2 - CO 2 - N 2 - H 2 - CH4 gases
- 8. Coeficiente a a distintas temperaturas en agua pura T° N 2 O 2 CO 2 0 0,02354 0,04889 1,713 10 0,01861 0,03802 1,194 20 0,01546 0,03102 0,878 30 0,01342 0,02608 0,665 40 0,01184 0,01644 0,530
- 10. Oxígeno: La tasa de O 2 disuelto condiciona: AEROBIOSIS ANAEROBIOSIS
- 11. macronutrientes, micronutrientes, y elementos mayores, menores y trazas De los aproximadamente 20 elementos que constituyen los tejidos vegetales, se llaman MACRONUTRIENTES a los que constituyen ≥ 0,1% del peso seco libre de cenizas: C, O, H, N, P, S, K, Mg, Ca, Na, Cl (N, P, S = elementos menores) MICRONUTRIENTES ≤0,1%: Fe, Mn, Cu, Zn, B, Si, Mo, V, Co
- 12. Elementos mayores, menores y trazas y compuestos orgánicos y gases en una “media” en aguas naturales Concentraciones: E.mayores : 0.1-10 meq./ l, media 2.4 meq./l; E.menores : menos 1 mg/ l. Elementos mayores Elementos menores Trazas y compuestos org á nicos Ca + 2 (64%) HCO 3 - N (73%) (NO 3 - o NH 4 + ) Fe, Cu, Co, Mo, Mn, Zn, B, V (µgl 1- ) Mg 2+ (17%) SO 4 2- P (16%) (HPO 4 2- o H 2 PO 4 - ) Compuestos orgánicos como ácidos húmicos, productos de excreción, vitaminas, otros metabolitos Na+ (3%) Cl - Si (10%) (SiO 2 o HSiO 3 - ) K + H + (Fe 2 + ) NH 4 +
- 16. NITRIFICACIÓN-DENITRIFICACIÓN 2 NH 4 + + 3 O 2 ----- nitrosomonas ----> 4 H + + 2 H 2 O 2 NO 2 - + O 2 ----- nitrobacter ----> 2 NO 3 - seguido por formación de nitrógeno (denitrificación) 4 NO 3 - + 5 (CH 2 O) + 4 H+ ----bacterias denitrificantes----> 2 N 2 (gas) + 5 CO 2 (gas) + 7 H 2 O
- 17. Las proporciones nitrato, nitrito, amonio, suelen mostrar un gradiente vertical: NO 3 - 89 % NO 2 - 2% NH 4 + 9% NO 3 - 2 0% NO 2 - 1 % NH 4 + 7 9% en superficie en profundidad
- 19. La conductividad s e expresa en ohmios o siemens por cm y va desde 25 µs cm -1 en aguas muy puras hasta varios miles (1000-3000) en aguas contaminadas o muy mineralizadas. Margalef expresa: “ Los elementos o iones cuyas concentraciones muestran una buena correlación positiva con la salinidad, se pueden considerar como componentes principales de proporcionalidad relativamente constante, que dan al agua su carácter y cuyas proporciones son poco influidas por la actividad de los organismos”. Tiene dichos atributos los metales alcalinotérreos divalentes Ca ++ y Mg ++ , los alcalino monovalentes Na + , los iones ‘ácidos fuertes Cl - y SO 4 = y el ácido débil HCO 3 - . 1000 µs cm -1 corresponde aproximadamente a una concentración salina de 0,6 g/l. La relación entre conductividad y salinidad depende del tipo de sales presentes, pero se acepta qfue la salinidad es igual a la conductividad multiplicada por un factor comprendido entre 0 ,00055 y 0,0009.
- 21. La MOD es un componente clave en los procesos tróficos en el agua. Las bacterias, usándola como sustrato, juegan un papel importante en la dinámica de nutrientes, el flujo de C y las interacciones tró- ficas. Tanto en las zonas pelágicas como en los sedimentos se distinguen por lo menos 2 o 3 fracciones funciona- les distintas de MO, con diferente importancia para los microheterótrofos. La mayor parte del pool de CO lábil disuelto es principalmente de bajo peso molecular y representa sólo el 1-20% del COD. La mayoría del COD es de naturaleza polímera, y el 80-90% tiene alto peso molecular. Esta fracción es una mezcla de diferentes biopolímeros (proteinas, polinucleótidos, poliscáridos, lípidos, ligninas) y geopolímeros, tal como los compuestos húmicos disueltos. Esta fracción de alto peso molecular no es directamente disponible para las bacterias.
- 22. Esta fracción de alto peso molecular se llama “recal- citrante”, y tiene un reciclaje de 2000 a 6000 años, con un papel poco conocido en las cadenas tróficas. El COD más lábil, en cambio, tiene un reciclaje de 1-10 hs. El COD y el COP (particulado) han sido definidos como “detritus”, pudiendo se autóctonos o alóctonos. Los detritos y las bacterias son el puente del C, los nutrien- tes y el flujo de E entre los productores primarios y la clásica cadena de alimentos vía el “microbial loop”. La MO acarreada por ríos es modificada durante el transporte, parte es transformada química y micro- biológicamente, y la fracción restante, en general recalcitrante, se mezcla con la MOD autóctona.
- 24. Entre los solutos orgánicos de la MOD, los aminoácidos disueltos, los hidratos de C y los ácidos orgánicos disueltos, han sido los más estudiados. Conocer las cantidades en que se encuenran y su contribución a la MOD es necesario para calcular el flujo de C, los estudios de degradación y entender los procesos de la heterotrofia micriobiana.
